8.2: Hidroboración, Hidroaluminación e Hidrostanación de Alquenos
- Page ID
- 73160
8.2.1 Hidroboración de Alquenos
La hidroboración quiral catalizada por Rh de alquenos proporciona un método eficaz para la síntesis de organoboranos ópticamente activos, los cuales son intermedios versátiles en la síntesis orgánica. El enlace carbono-boro se puede convertir en varios grupos funcionales mediante posteriores reacciones de formación de enlaces carbono-carbono, carbono-oxígeno, boro-carbono o carbono-nitrógeno con retención de estereoquímica (Esquema\(\PageIndex{1}\)).
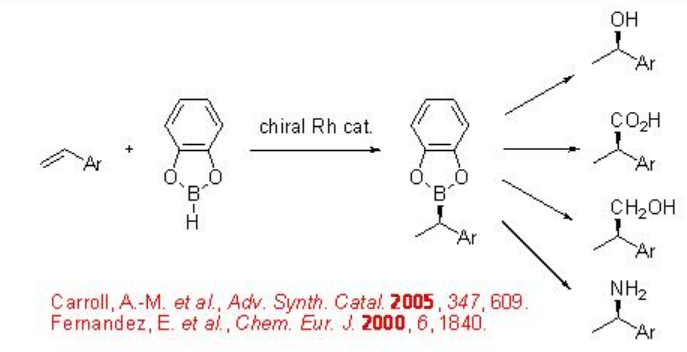
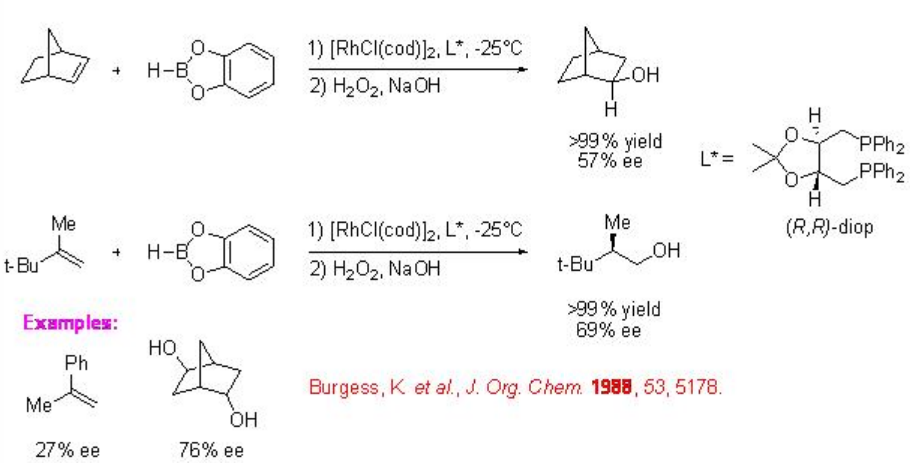
La primera hidroboración asimétrica catalítica de norborneno y 2-terc- butilpropeno con catecolborano apareció en presencia del complejo Rh- (R, R) -diop (Esquema 2). Los productos, 2-hidroxinorbornano y 2,3,3-trimetilbutanol se obtienen después del tratamiento con solución alcalina de peróxido de hidrógeno.
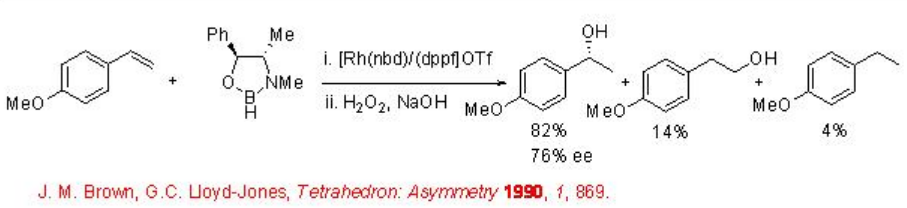
Se ha demostrado el uso de la combinación de borano quiral y catalizador aquiral para la hidroboración asimétrica. Por ejemplo, la hidroboración de 4-metoxiestireno procede con borano quiral derivado de pseudoefedrina en presencia de complejo de rodio aquiral al alcohol secundario correspondiente con 76% ee después de la oxidación (Esquema\(\PageIndex{3}\)).
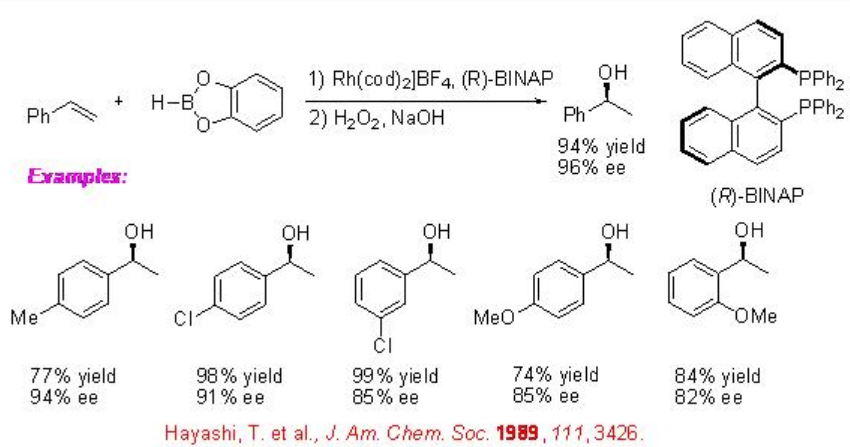
La reacción de los vinilarenos con el catecolborano ha sido ampliamente estudiada utilizando el complejo quiral Rh. Por ejemplo, el catiónico Rh- (R) -BIANP cataliza la hidroboración del estireno con selectividad de ramificación completa para proporcionar 1-feniletanol con 96% ee después de la oxidación. La regioselectividad es opuesta a la observada con reacciones no catalizadas (Esquema\(\PageIndex{4}\)).
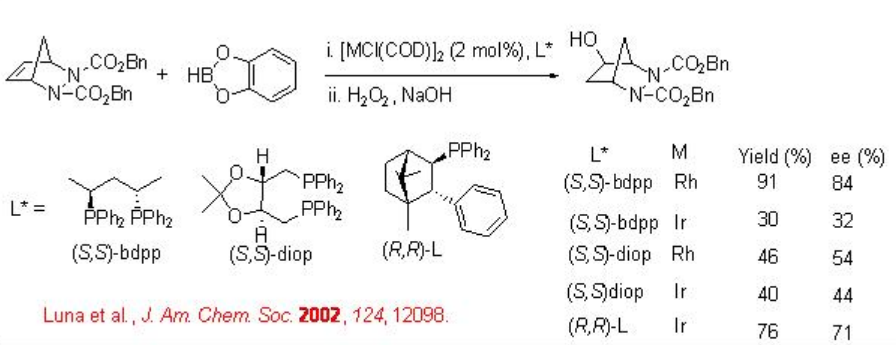
La desimetrización asimétrica de hidrazinas meso-bicíclicos se ha mostrado con catecolborano usando complejos quirales basados en Rh e IR (Esquema\(\PageIndex{5}\)). Se observa una inversión de la enantioselectividad entre los catalizadores Rh e Ir.
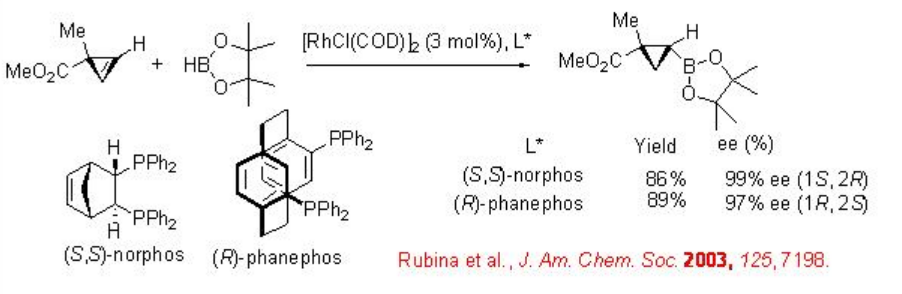
La reacción del ciclopropeno se estudia con pinacolborano como nuevo agente hidroborante en presencia de una serie de complejos quirales de Rh fosfina (Esquema\(\PageIndex{6}\)). La reacción con pinacolborano mostró mayor selectividad en comparación con la del catecolborano debido al control estérico entre los sustratos y el agente hidroborante.
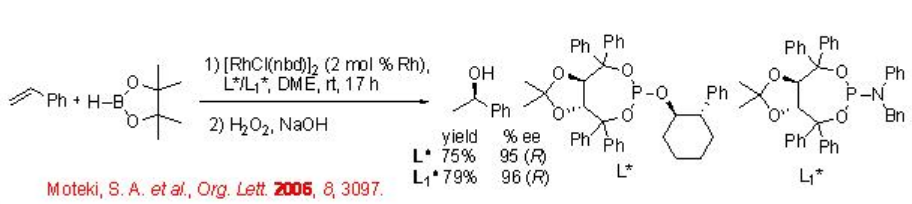
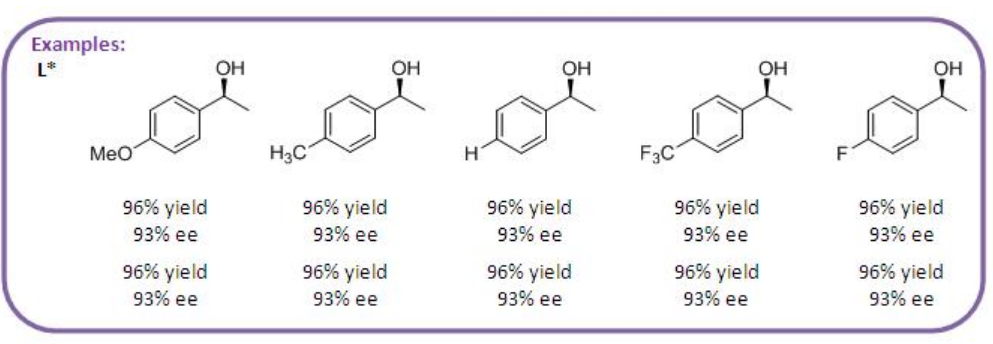
Se estudian complejos Rh con fosfato monodentado quiral y fosforamidita derivada de taddol para la hidroboración de vinilarenos con pinacolborano (Esquema\(\PageIndex{7}\)). Las reacciones de una serie de vinilarenos que tienen electrones sustituidos por extracción y donación proceden con alta enantioselectividad.
8.2.2 Hidroaluminación e Hidrostanación de Alquenos
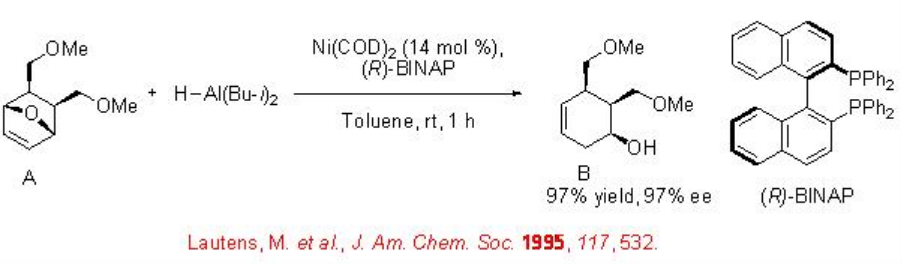
Si bien las reacciones de hidrosililación e hidroboración asimétricas catalíticas son bien conocidas, la hidroaluminación catalítica y la hidroestanización de alquenos son raras. El complejo quiral de níquel se utiliza para la hidroaluminación asimétrica de alquenos oxabicíclicos. Por ejemplo, Ni- (R) -BINAP cataliza la reacción de A con iso -Bu 2 AlH para dar B con 97% ee (Esquema\(\PageIndex{8}\)).
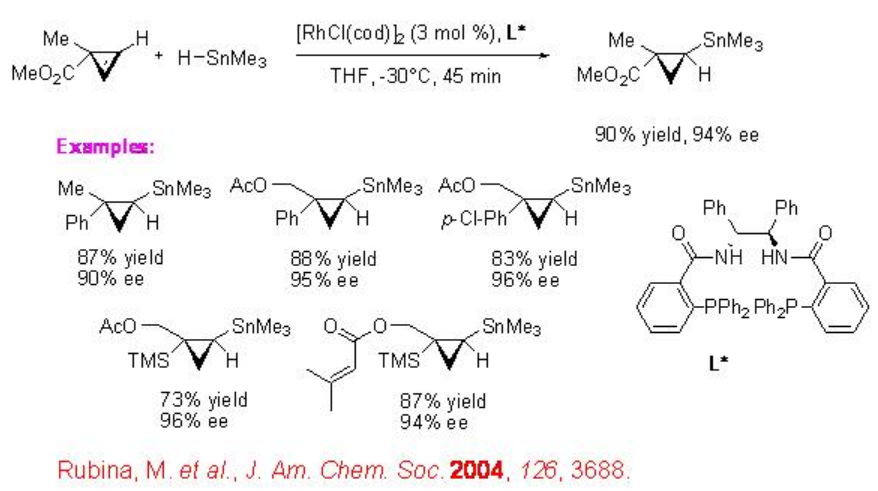
El primer ejemplo para la hidroestanización asimétrica de ciclopropenos se presenta utilizando L* derivado de ácido difenilfosfinbenzoico quiral portador de complejo Rh (Esquema\(\PageIndex{9}\)). El producto trans-ciclopropilestannano se obtiene con 94% ee. El procedimiento es general y en la reacción se demuestra una serie de ciclopropenos sustituidos.


