11.4: Oxidaciones Enantioselectivas
- Page ID
- 73268
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Los biocatalizadores también se vuelven útiles para oxidaciones asimétricas. Se ha explorado una amplia gama de oxidaciones asimétricas utilizando sistemas biocatalíticos.
Oxidación Baeyer-Villiger
La reacción de Baeyer-Villiger es conocida desde hace más de 100 años. Sin embargo, la versión asimétrica de esta reacción sigue siendo un desafío para los químicos orgánicos. Dependiendo de la naturaleza de las cetonas, la reacción se puede llevar a cabo como una resolución de cetonas racémicas así como una reacción de desimetrización asimétrica a partir de cetonas proquirales. Se conocen las enzimas utilizadas para esta reacción
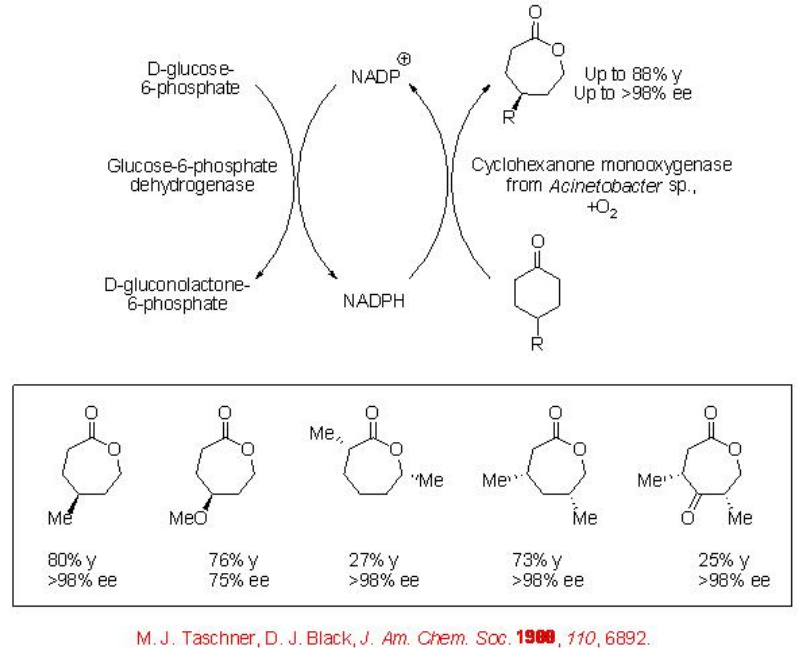
como monooxigenasas de Baeyer-Villiger. Estas enzimas son dependientes de cofactores y generalmente se obtienen de fuentes microbianas. Por ejemplo, las ciclohexanonas monocíclicas 4-sustituidas pueden oxidarse en las lactonas con buen rendimiento y con altas enantioselectividades (Esquema\(\PageIndex{1}\)). En este proceso, se necesita la forma reducida del cofactor (NADPH) bajo la formación de NADP + que se recicla in situ utilizando una reproducción de cofactor acoplado enzimático.
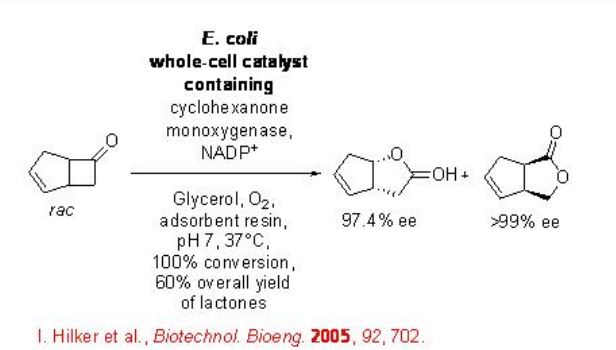
También se ha explorado la ampliación del proceso. Por ejemplo, la biciclo [3.2.0] hept-2-enona racémica con aporte de 25g/L procede a la oxidación en presencia de un biocatalizador recombinante de células enteras para proporcionar lactonas regioisoméricas con alta enantioselectividad (Esquema\(\PageIndex{2}\)).
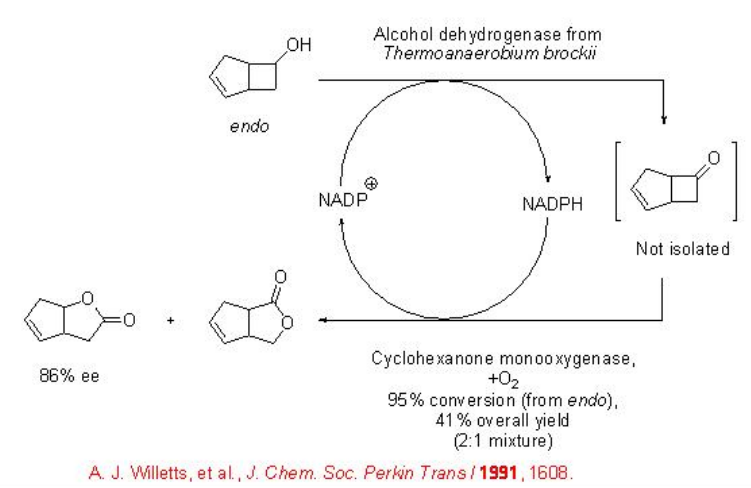
Otra mejora del proceso es el acoplamiento de una ciclohexanona monooxigenasa con una ADH de T. brockii, una “doble oxidación” libre de cosustrato de un alcohol en lactonas (Esquema\(\PageIndex{3}\)). En este sistema, la forma oxidada del cofactor (NADP +) se consume en la etapa inicial catalizada por ADH, mientras que la forma reducida del cofactor (NADPH) es necesaria para la segunda etapa de oxidación catalizada por monooxigenasa. En el segundo paso, se vuelve a producir la forma oxidada del cofactor (NADP +), que luego se necesita para el primer paso.
Epoxidación
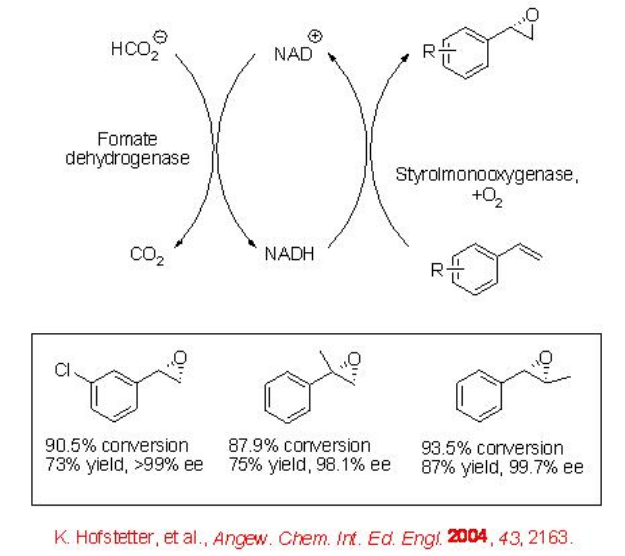
Los epóxidos ópticamente activos sirven como bloques de construcción versátiles en la síntesis orgánica. Además de metales y organocatalizadores, la monooxigenasa dependiente del cofactor resultó ser un catalizador valioso para la epoxidación de alquenos. Por ejemplo, la epoxidación de estireno se ha demostrado usando una monooxigenasa de estireno dependiente de FAD/NADH recombinante estable en emulsiones acuosa-orgánicas (Esquema\(\PageIndex{4}\)). La condición de reacción también es efectiva para la oxidación de otros derivados de estireno.
Oxidación de Aminoácidos
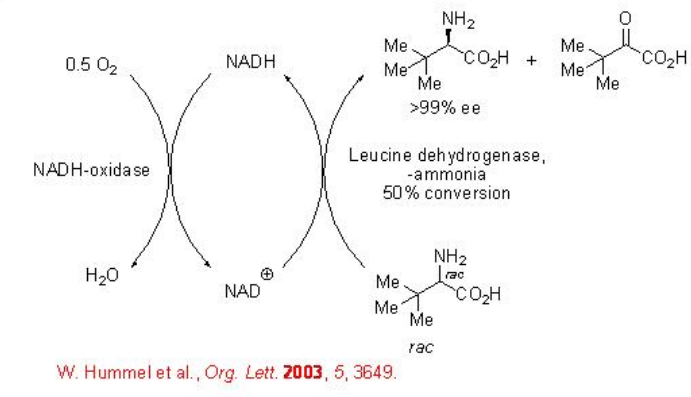
La oxidación asimétrica del grupo amina en aminoácidos proporciona un método eficaz para la síntesis de aminoácidos no naturales que es importante en la síntesis de fármacos. Por ejemplo, la terc - leucina racémica puede oxidarse a D-terc - leucina usando una leucina amino deshidrogenasa y una NADH-oxidasa de E-coli con excelente enantioselectividad (Esquema\(\PageIndex{5}\)).
Oxidación de Alcoholes
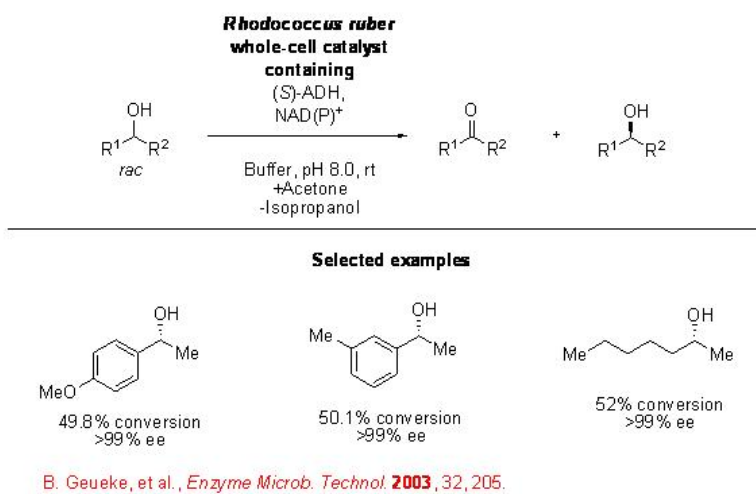
También se ha investigado la oxidación de alcoholes secundarios en cetonas utilizando sistemas biocatalíticos. Por ejemplo, la oxidación de alcoholes secundarios racémicos procede en presencia de un ADH de R. ruber (Esquema\(\PageIndex{6}\)). El reciclaje del cofactor NADPH se realiza in situ utilizando acetona, la cual se reduce a 2-propanol bajo la formación de NADP +.
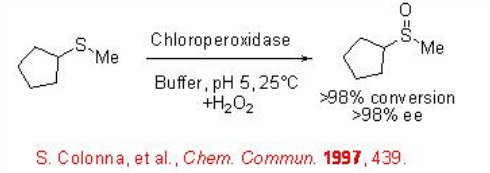
Sulfoxidación
Los sulfóxidos ópticamente activos desempeñan un papel importante en la síntesis orgánica como auxiliares quirales, así como intermedios para la construcción de moléculas ópticamente activas. El sulfóxido ópticamente activo también está presente como unidad estructural en muchos compuestos biológicamente activos. La oxidación enzimática de sulfuros proporciona un método eficaz para la síntesis de sulfóxidos ópticamente activos. Por ejemplo, el sulfuro de ciclopentil metilo sufre oxidación en presencia de cloroperoxidasa con excelente conversión y enantioselectividad.