13.1: Introducción a la Estructura y Síntesis de Alcoholes
- Page ID
- 76922
Introducción
Los alcoholes, fenoles, enoles y ácidos carboxílicos contienen un grupo hidroxilo. Sin embargo, la química de estos cuatro grupos funcionales diferentes es diferente.
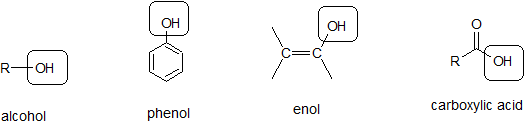
Alcoholes
Las moléculas de alcoholes contienen uno o más grupos hidroxilo (grupos OH) sustituidos por átomos de hidrógeno a lo largo de la cadena de carbono.
La estructura del alcohol más simple, el metanol (alcohol metílico), puede derivarse de la del metano poniendo un OH en lugar de uno de los H's:
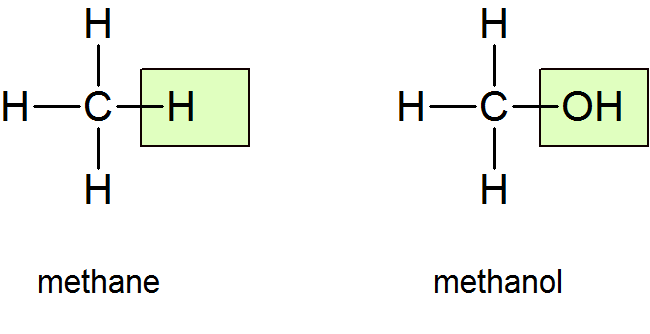
El metanol también se llama alcohol de madera porque se puede obtener calentando la madera en ausencia de aire, un proceso llamado destilación destructiva. El vapor de metanol que se desprende cuando se calienta la madera se puede condensar a un líquido enfriando por debajo de su punto de ebullición de 65°C. El metanol es altamente tóxico. En 1986, hubo seis muertes de residentes de Peerless Lake, Alberta, provocadas por el consumo de líquido de fotocopiadora que contenía metanol (o hidrato de metilo como suele llamarse en los informes de prensa). En 2000, más de 100 personas murieron en El Salvador luego de que los mercaderes negros vendieran botellas de licor desechadas que habían sido rellenadas con una mezcla de metanol. De hecho, el problema se ha repetido globalmente y tantas veces que en 2014 la Organización Mundial de la Salud publicó una nota informativa advirtiendo de brotes de intoxicación por metanol que “ocurren cuando se agrega metanol a bebidas alcohólicas producidas ilícitamente o informalmente”.
El segundo miembro de la familia del alcohol es el etanol (alcohol etílico), la sustancia que comúnmente llamamos alcohol. El etanol también se conoce como alcohol de grano porque se obtiene cuando el grano o el azúcar fermenta.
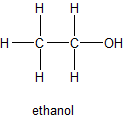
La fermentación se refiere a una reacción química que es acelerada por las enzimas y ocurre en ausencia de aire. (Enzimas, catalizadores que ocurren naturalmente en levaduras y otros organismos vivos, se discuten con más detalle en otra parte.) Casi todos son conscientes de que el alcohol presente en las bebidas alcohólicas es el etanol (también llamado alcohol etílico o alcohol de grano). No obstante, muchas personas no se dan cuenta de que en su estado puro, o en soluciones de alta concentración, esta sustancia es venenosa. En el laboratorio se pueden encontrar recipientes etiquetados como “etanol absoluto”, “etanol 95%” y “etanol desnaturalizado”. La adquisición de etanol por parte de los laboratorios, y su posterior eliminación, es monitoreada cuidadosamente por las autoridades provinciales. En ningún caso se debe considerar beber etanol de laboratorio, incluso después de haber sido diluido a una concentración equivalente a la que se encuentra en la cerveza. El alcohol desnaturalizado es el etanol al que se le han agregado cantidades apropiadas de sustancias venenosas o nauseabundas (como el metanol). El etanol se utiliza como solvente, en algunos combustibles especiales, en anticongelante y para fabricar una serie de otros productos químicos. Probablemente estés más familiarizado con él como componente de las bebidas alcohólicas. El etanol constituye del 3 al 6 por ciento de la cerveza, del 12 al 15 por ciento de la mayoría de los vinos y del 49 al 59 por ciento del licor destilado. (La “prueba” de una bebida alcohólica es apenas el doble del porcentaje de etanol.) Los efectos intoxicantes del alcohol son bien conocidos, y es un depresor leve. El uso excesivo prolongado puede provocar daño hepático.
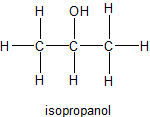
Un tercer alcohol comúnmente encontrado, el alcohol isopropílico (“alcohol para frotar” o 2-propanol), también es tóxico. Tiene la capacidad de matar gérmenes y tiene un efecto lubricante temporal durante el proceso de frotamiento. A diferencia del metanol, el 2-propanol no se absorbe a través de la piel; por lo tanto, representa menos peligro para la salud.
Fenoles
Un fenol es un compuesto orgánico en el que un grupo hidroxilo está unido directamente a uno de los átomos de carbono de un anillo aromático. El comportamiento químico de los fenoles es diferente en algunos aspectos del de los alcoholes, por lo que es sensato tratarlos como un grupo similar pero característicamente distinto.
Hasta finales del siglo XIX, una persona sometida a cirugía tuvo que enfrentar el hecho de que podría sufrir las consecuencias de lo que ahora sabemos que es una infección bacteriana, contraída durante el transcurso de la operación. Los médicos de la época desconocían que las bacterias existían, y no tenían forma de contrarrestar los problemas que causaban las bacterias. En 1867, Joseph Lister, quien se había enterado de la existencia de bacterias como resultado de una investigación realizada por Louis Pasteur, comenzó a utilizar soluciones de fenol para limpiar heridas e instrumentos quirúrgicos. La solución de fenol fue un antiséptico eficaz, matando bacterias, y como resultado, las posibilidades de supervivencia de un paciente mejoraron mucho. El fenol en sí era bastante fuerte para estos fines, quema tejido saludable, y finalmente se encontraron sustitutos. Uno de esos sustitutos, que se utiliza hoy en día en las pastillas para la garganta y los enjuagues bucales, es el 4-n-hexilresorcinol.
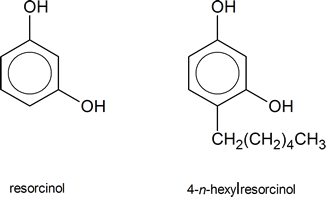
Enols
Cuando un grupo hidroxilo está unido a un carbono vinílico, el grupo funcional se llama enol. Como se discute en el Capítulo 10, la hidratación de alquinos puede resultar en la formación de enol. Los enoles se someten a tautomerización para formar cetonas, en la mayoría de los casos, la ceto-forma es más estable y predomina el equilibrio. El fenol es una excepción importante a esta tendencia.
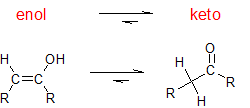
Ácidos Carboxílicos
En los ácidos carboxílicos, el grupo hidroxilo está unido a un carbono carbonilo. Como su nombre lo indica, este grupo funcional es ácido y puede donar fácilmente el protón en el grupo hidroxilo.

Ejercicio
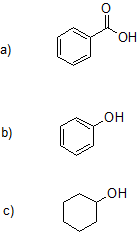
1. Clasificar los siguientes compuestos como alcoholes, fenoles, enoles o ácidos carboxílicos. Un compuesto se puede clasificar por dos de las opciones.
- Contestar
-
1.
a) ácido carboxílico
b) fenol y enol
c) alcohol
Colaboradores y Atribuciones
Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
Ed Vitz (Kutztown University), John W. Moore (UW-Madison), Justin Shorb (Hope College), Xavier Prat-Resina (University of Minnesota Rochester), Tim Wendorff, and Adam Hahn.

