21.1: Estructura y propiedades de los ácidos carboxílicos y sus sales
- Page ID
- 76935
Estructura del grupo ácido carboxílico
Los ácidos carboxílicos son compuestos orgánicos que incorporan un grupo funcional carboxilo, CO 2 H. El nombre carboxilo proviene del hecho de que un grupo carbonilo y un grupo hidroxilo están unidos al mismo carbono.
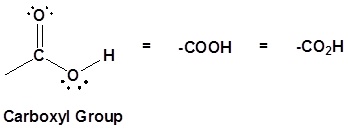
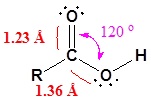
El carbono y el oxígeno en el carbonilo son ambos sp 2 hibridados, lo que le da a un grupo carbonilo una forma trigonal básica. El oxígeno hidroxílico también se hibrida sp 2 lo que permite que uno de sus electrones de pares solitarios conjugar con el sistema pi del grupo carbonilo. Esto hace que el grupo carboxilo plano sea una lata representada con la siguiente estructura de resonancia.
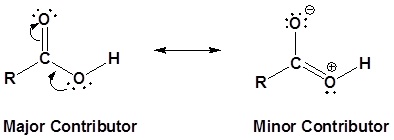
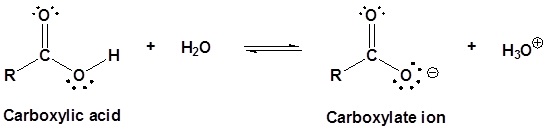
Los ácidos carboxílicos se llaman así porque pueden donar un hidrógeno para producir un ion carboxilato. Los factores que afectan la acidez de los ácidos carboxílicos se discuten en la siguiente sección de este capítulo.
Propiedades físicas de algunos ácidos carboxílicos
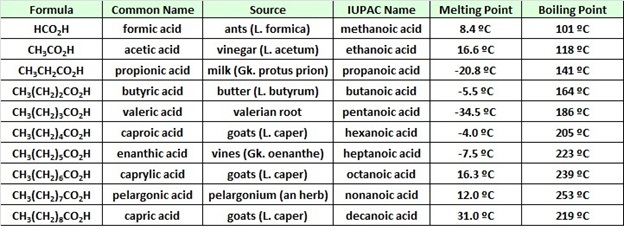
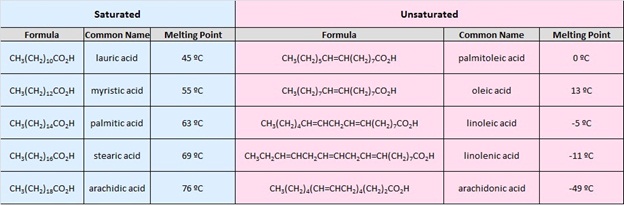
La tabla al inicio de esta página daba los puntos de fusión y ebullición para un grupo homólogo de ácidos carboxílicos que tienen de uno a diez átomos de carbono. Los puntos de ebullición aumentaron con el tamaño de manera regular, pero los puntos de fusión no. Los ácidos no ramificados constituidos por un número par de átomos de carbono tienen puntos de fusión superiores a los homólogos impares que tienen uno más o uno menos de carbono. Esto refleja diferencias en las fuerzas de atracción intermoleculares en el estado cristalino. En la tabla de ácidos grasos vemos que la presencia de un doble enlace cis-disminuye significativamente el punto de fusión de un compuesto. Así, el ácido palmitoleico se funde por encima de 60º más bajo que el ácido palmítico, y se producen disminuciones similares para los compuestos C 18 y C 20. Nuevamente, los cambios en el empaque de cristales y las fuerzas intermoleculares son los responsables.
Los factores que influyen en los puntos de ebullición relativos y las solubilidades en agua de diversos tipos de compuestos se discutieron anteriormente. En general, las fuerzas de atracción dipolares entre moléculas actúan para aumentar el punto de ebullición de un compuesto dado, siendo los enlaces de hidrógeno un ejemplo extremo. Los enlaces de hidrógeno también son un factor importante en la solubilidad en agua de los compuestos covalentes Para refrescar su comprensión de estos principios Haga clic aquí. La siguiente tabla enumera algunos ejemplos de estas propiedades para algunos compuestos polares de tamaño similar (el hidrocarburo no polar hexano se proporciona para comparación).
Las primeras cinco entradas tienen grupos funcionales de oxígeno, y los puntos de ebullición relativamente altos de las dos primeras se deben claramente a los enlaces de hidrógeno. Los ácidos carboxílicos tienen puntos de ebullición excepcionalmente altos, debido en gran parte a asociaciones diméricas que involucran dos enlaces de hidrógeno. Aquí se muestra una fórmula estructural para el dímero de ácido acético. Cuando el puntero del ratón pasa sobre el dibujo, aparecerá un diagrama de nubes de electrones. Los altos puntos de ebullición de las amidas y nitrilos se deben en gran parte a fuertes atracciones dipolares, complementadas en algunos casos por enlaces de hidrógeno.

|
Fórmula |
Nombre de la IUPAC |
Peso molecular |
Punto de ebullición |
Solubilidad en Agua |
|---|---|---|---|---|
| CH 3 (CH 2) 2 CO 2 H | ácido butanoico | 88 | 164 ºC | muy soluble |
| CH 3 (CH 2) 4 OH | 1-pentanol | 88 | 138 ºC | ligeramente soluble |
| CH 3 (CH 2) 3 CHO | pentanal | 86 | 103 ºC | ligeramente soluble |
| CH 3 CO 2 C 2 H 5 | etanoato de etilo | 88 | 77 ºC | moderadamente soluble |
| CH 3 CH 2 CO 2 CH 3 | propanoato de metilo | 88 | 80 ºC | ligeramente soluble |
| CH 3 (CH 2) 2 CONH 2 | butanamida | 87 | 216 ºC | soluble |
| CH 3 CON (CH 3) 2 | N, N-dimetiletanamida | 87 | 165 ºC | muy soluble |
| CH 3 (CH 2) 4 NH 2 | 1-aminobutano | 87 | 103 ºC | muy soluble |
| CH 3 (CH 2) 3 CN | pentannitrilo | 83 | 140 ºC | ligeramente soluble |
| CH 3 (CH 2) 4 CH 3 | hexano | 86 | 69 ºC | insoluble |
Sales de carboxilato
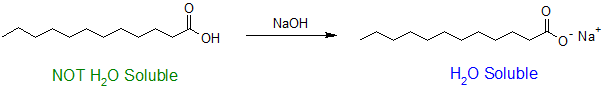
La solubilidad en agua de los ácidos carboxílicos está determinada por la relación de grupos carboxilo al número de átomos de carbono en la molécula siguiendo la “Regla 4 a 6”. Como se ve con las aminas, la solubilidad en agua de los ácidos carboxílicos se puede incrementar cuando se ionizan. Típicamente, se usa una base fuerte para desprotonar el ácido carboxílico e impulsar la reacción hasta su finalización como se muestra a continuación.
Ejercicio
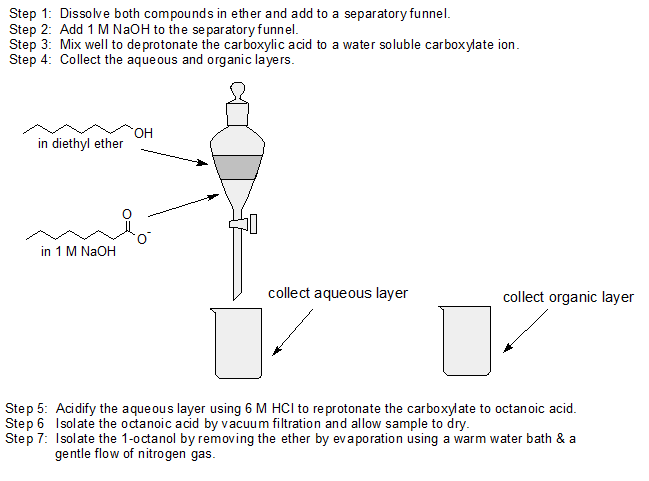
1. Use la química ácido-base y las diferencias en la solubilidad en agua para separar 1-octanol del ácido octanoico usando las siguientes soluciones: NaOH 1 M, éter y HCl 6 M y cualquier equipo de laboratorio.
- Contestar
-
1.
Colaboradores y Atribuciones
Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
Prof. Steven Farmer (Sonoma State University)
William Reusch, Professor Emeritus (Michigan State U.), Virtual Textbook of Organic Chemistry

