22.5: Química de Anhídrido de Ácido
- Page ID
- 76543
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
Síntesis de Anhídridos de Ácido
Los cloruros de ácido reaccionan con ácidos carboxílicos para formar anhidros como se muestra en la reacción a continuación.

Algunos anhidridos cíclicos se pueden sintetizar a partir del ácido dicarboxílico correspondiente con calentamiento suave. El siguiente ejemplo muestra la reacción del ácido glutárico para formar un anhídrido cíclico.
Ejemplo: Síntesis de Anhídrido de Ácido

Reactividad de anhídrido de ácido
Los anhidridos de ácido experimentan reacciones de hidrólisis y sustitución de acilo nucleofílico.

Hidrólisis de anhídrido ácido
Los anhidridos de ácido se hidrolizan fácilmente a ácidos carboxílicos. En muchos casos, esta reacción es una reacción secundaria no deseada y se tomarán medidas en el laboratorio para mantener el sistema “seco” (también conocido como libre de agua). La presencia de piridina facilita las transferencias de protones durante la reacción. A continuación se muestra la reacción de hidrólisis para anhídrido benzoico.

El mecanismo es análogo al mecanismo para la síntesis de ésteres a partir de los anhidridos de ácido y se muestra a continuación se detalla.
Reacciones de sustitución de acilo nuclefílico a partir de anhídrido de ácido
Los derivados de ácido carboxílico se pueden sintetizar a partir de los anhidros de ácido a través del mecanismo de sustitución de acilo nucleofílico previamente discutido.
Síntesis de Éster
Los anhidridos de acido reaccionan con alcoholes para producir esteres como se muestra en la reaccion a continuación. Las reacciones de los anhidridos frecuentemente usan piridina como solvente.
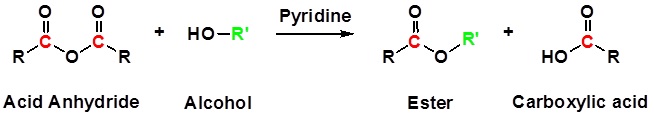
También se produce un ácido carboxílico, pero no se considera un producto sintético. El éster es considerado el “producto de interés”.
En el ejemplo se muestra la síntesis de benzoato de metilo a partir de anhídrido benzoico y metanol.
Ejemplo: Sítesis de éster

El mecanismo sigue el mecanismo de sustitución de acilo nucleofílico como se discutió previamente y se revisó a continuación.
1) El alcohol nucleofílico reacciona con el carbonilo electrofílico
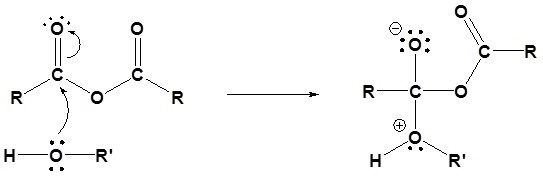
2) Desprotonación por piridina

3) Dejando la eliminación del grupo

4) Protonación del carboxilato
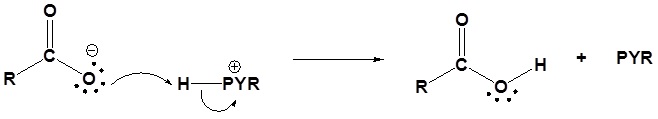
Síntesis de Amidas
Los anhidridos de ácido reaccionan con aminas para formar amidas. Como se ve con las reacciones de haluro de ácido, debe estar presente un segundo equivalente de la amina para que la reacción continúe.

Ejemplo: Síntesis de amida

El mecanismo para la síntesis de amidas es análogo al mecanismo para la formación de ésteres. La única diferencia menor es que se usa un segundo equivalente de la amina o amoníaco en lugar de la piridina.
1) La amina nucleofílica reacciona con el carbonilo electrofílico

2) Desprotonación por la amina
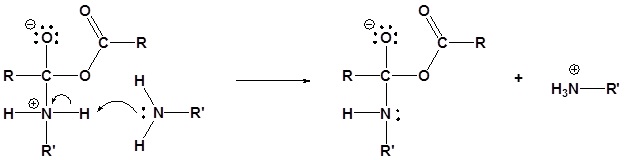
3) Dejando la eliminación del grupo

Ejercicio
6. Extraer el mecanismo para la siguiente reacción.

7. Dibuja el producto de la reacción entre estas dos moléculas.

- Contestar
-
6.

7.

Colaboradores y Atribuciones
Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
Prof. Steven Farmer (Sonoma State University)

