18.5: Alquilación y acilación de benceno - Las reacciones EAS de Friedel-Crafts
- Page ID
- 76066
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Alquilación Friedel-Crafts
La reacción de alquilación de Fridedel-Crafts a partir de alquilbencenos a partir de haluros de alquilo. La utilidad de esta reacción es limitada, ya que puede ser difícil detener la reacción en una sola alquilación. Adicionalmente, en el Paso 1 se produce un intermedio de carbocationes que trae el potencial de reordenamientos de carbocationes (música temática ominosa).
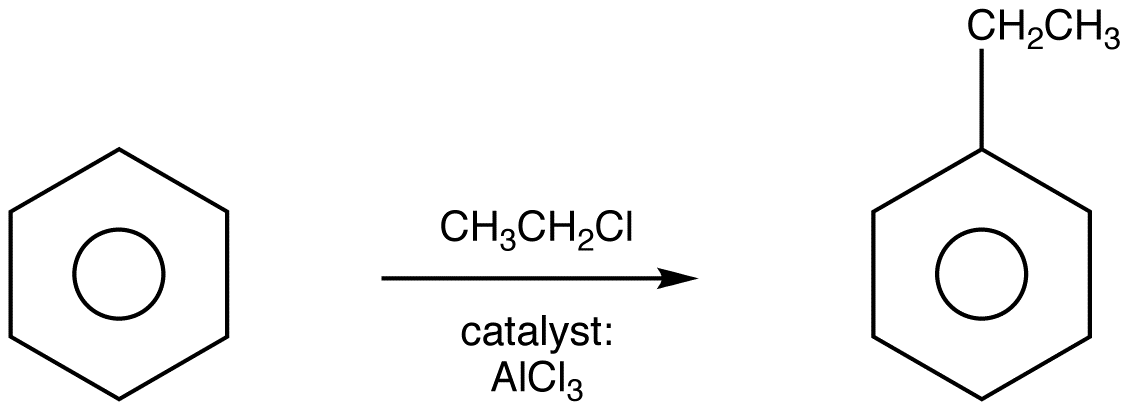
El mecanismo se lleva a cabo de la siguiente manera:
Paso 1: Se crea un carbocatión para formar el electrófilo. Estos pasos activan el haloalcano. Los haluros secundarios y terciarios solo forman el carbocatión libre en esta etapa.
.png)
Paso 2: Los electrones pi del benceno reaccionan con el electrófilo para formar el ion alquilbencenio estabilizado por resonancia.
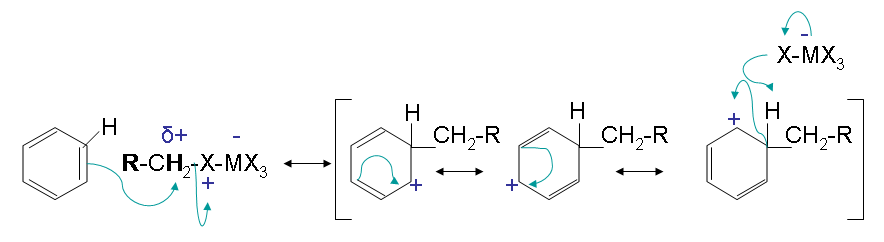
Paso 3: Cualquier Base Lewis reacciona recoge el hidrógeno del ion alquilbenceno para reformar el anillo aromático.
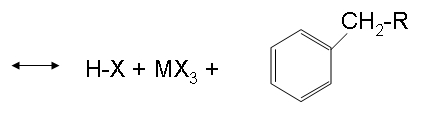
El paso de acabado que se muestra arriba son los dos productos.
La reactividad de los haloalcanos aumenta a medida que subes en la tabla periódica y aumenta la polaridad. Esto significa que un haloalcano RF es el más reactivo seguido de RCl luego RBr y finalmente RI. Esto significa que los ácidos de Lewis utilizados como catalizadores en las reacciones de alquilación de Friedel-Crafts tienden a tener combinaciones de halógenos similares como BF 3, SbCl 5, AlCl 3, SbCl 5 y AlBr 3, todos los cuales se usan comúnmente en estas reacciones.
Algunas limitaciones de la alquilación Friedel-Crafts
Hay posibilidades de reordenamientos de carbocationes cuando se intenta agregar una cadena de carbono mayor a dos carbonos. Los reordenamientos ocurren debido a cambios de hidruro y cambios de metilo. Por ejemplo, el producto de una Alquilación Friedel-Crafts mostrará un reordenamiento iso al agregar una cadena de tres carbonos como sustituyente. Una forma de resolver estos problemas es a través de la acilación Friedel-Crafts.
Además, la reacción solo funcionará si el anillo al que le está agregando un sustituyente no está desactivado. Friedel-Crafts falla cuando se usa con compuestos como nitrobenceno y otros sistemas de desactivación fuertes.
Las reacciones de Friedel-Crafts no se pueden preformar entonces el anillo aromático contiene un sustituyente NH 2, NHR o NR 2. Los electrones de par solitario en las aminas reaccionan con el ácido de Lewis AlCl 3. Esto coloca una carga positiva junto al anillo de benceno, que se activa tan fuertemente que la reacción de Friedel-Crafts no puede ocurrir.
Por último, la alquilación de Friedel-Crafts puede sufrir polialquilación. La reacción agrega un grupo alquilo donador de electrones, que activa el anillo de benceno para una posterior alquilación.
Este problema no ocurre durante la acilación de Friedel-Crafts porque un grupo acilo se está desactivando. El evita más acilaciones.
Acilación Friedel-Crafts
Hay una etapa de reacción adicional para la acilación de Fridel-Crafts. El grupo acilo del producto se compleja con el cloruro de aluminio. Se agrega agua para aislar el producto final de acil benceno.
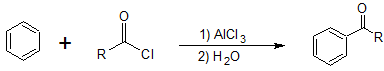
1 st Reacción
Mecanismo Paso 1: Formación de iones de acilio
Mecanismo Paso 2: Los electrones Pi del benceno reaccionan con el ion acilio para formar el complejo sigma, intermedio de acilbenceno estabilizado por resonancia:
.jpg)
Mecanismo Paso 3: Desprotonación del sigma comlex para restaurar la aromaticidad.
Durante la tercera etapa, el AlCl 4 regresa para eliminar un protón del anillo de benceno, lo que permite que el anillo vuelva a la aromaticidad. Al hacerlo, el AlCl 3 original se regenera para su uso nuevamente, junto con HCl. Lo más importante es que tenemos la primera parte del producto final de la reacción, que es una cetona. El producto forma un complejo con cloruro de aluminio como se muestra a continuación.
.jpg)
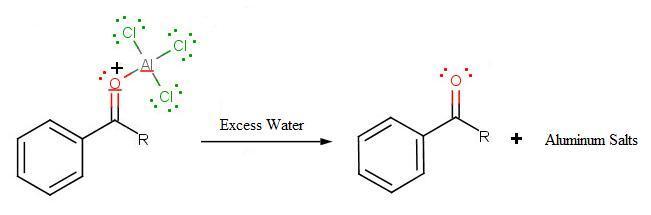
2 nd Reacción: Se añade agua para liberar el producto final como el acilbenceno:
.jpg)
Las acilaciones Friedel-Crafts ofrecen varias ventajas sintéticas sobre la alquilación Friedel-Crafts. Estas ventajas proporcionan un mayor control sobre la producción de productos de reacción. El ion acilio se estabiliza por resonancia, por lo que no se produce ningún reordenamiento de carbocationes. Adicionalmente, los grupos acilo se están desactivando con para reacciones EAS, por lo que el producto no experimenta reacciones adicionales. Sin embargo, las acilaciones Friedel-Crafts no funcionan con nitrobencenos u otros anillos de benceno desactivados. El concepto de desactivado se explorará más a fondo en las dos secciones siguientes de este capítulo.
Ejercicio
11. ¿Cuál de los siguientes NO sufrirá un reordenamiento en una reacción de Friedel-Crafts?

12. Sugerir un cloruro de acilo que se utilizó para elaborar los siguientes compuestos:

- Contestar
-
11. A, B y E no sufrirán un reordenamiento.
12.
.png)
Colaboradores y Atribuciones
Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
Prof. Steven Farmer (Sonoma State University)
William Reusch, Professor Emeritus (Michigan State U.), Virtual Textbook of Organic Chemistry


.jpg)
.jpg)