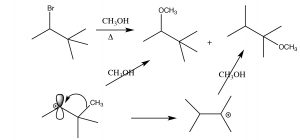
4.3: Reordenamientos: una consecuencia de generar carbocationes inestables
- Page ID
- 76927
Las reacciones que generan carbocationes pueden experimentar vías de reacción además de la sustitución.
Considera esta reacción:
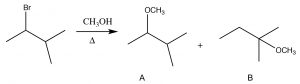
El sustrato es un haluro de alquilo secundario, y dado que el disolvente es metanol, un disolvente prótico polar, y con un nucleófilo débil, esperaríamos que se produzca una\(\mathrm{S}_{\mathrm{N} 1\) reacción, a través de un carbocatión en el carbono secundario. El primer producto (A) es exactamente eso, pero ¿cómo se formó el segundo producto (B)? Para entender esto, veamos el mecanismo de la reacción. el primer paso es la ionización de\(\mathrm{Br}^{-}\) dejar atrás el carbocatión secundario (que produce el producto A). El producto B debe haberse formado por ataque nucleófilo del\(\mathrm{O}\) metanol sobre un carbocatión diferente. El precursor de B es un carbocatión terciario, que es más estable que el secundario, y está formado por lo que se conoce como un desplazamiento de hidruro en el que el hidrógeno se desplaza con su par de electrones.
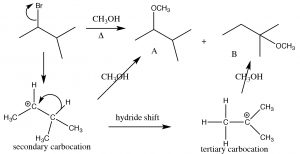
La formación de carbocationes suele ir acompañada de un reordenamiento esquelético: Aquí ocurre un desplazamiento de hidruro 1,2
Este reordenamiento produce un intermedio más estable que luego experimenta reacción; también puede implicar el desplazamiento de un grupo alquilo con sus electrones de un carbono al siguiente.