9.4: Descarboxilato de β-Cetoácidos
- Page ID
- 77010
Todas estas reacciones de condensación de Claisen producen un compuesto difuncional en el que se localiza un grupo carbonilo en la posición beta de un éster. Existe una reacción útil que se puede llevar a cabo si el éster se hidroliza al ácido correspondiente. Si el\(\beta\) -cetoácido resultante se calienta, se descarboxila (pierde\(\mathrm{CO}_{2}\)) en una reacción pericíclica que implica el reordenamiento cíclico de seis electrones como se muestra a continuación.
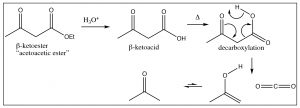
El\(\beta\) -cetoéster aquí se conoce como éster acetoacético. El\(\mathrm{CH}_{2}\) grupo entre los dos carbonilos es fácilmente desprotonado, y el anión resultante puede hacer un ataque nucleófilo sobre cualquier sustrato susceptible: por ejemplo, un haluro de alquilo. Una posterior hidrólisis y descarboxilación da como resultado un compuesto que tiene tres carbonos más en él que el haluro de alquilo original, como se muestra a continuación.
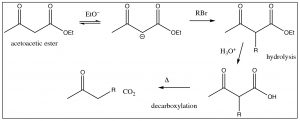
La síntesis de “éster acetoacético” es una forma poderosa de agregar una unidad de 3 carbonos. Una reacción similar involucra éster malónico (abajo), que puede usarse para agregar una unidad de 2 carbonos.
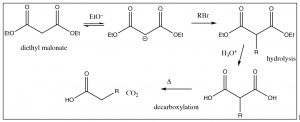
En la etapa de descarboxilación, solo uno de los ácidos carboxílicos descarboxilatos y el grupo alquilo se extiende por dos átomos de carbono. Curiosamente, los ácidos grasos (ácidos carboxílicos de cadena larga) son sintetizados por un mecanismo que es análogo a esta síntesis de éster malónico.


