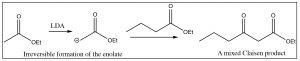
9.3: La Condensación de Claisen
- Page ID
- 76997
Como hemos señalado, todos los compuestos carbonílicos son capaces de formar enoles y aniones enolatos, y así como los aldehídos y cetonas experimentan reacciones de condensación entre sí, así entonces a ésteres. La versión éster del aldol se llama condensación de Claisen, pero los detalles esenciales son muy similares en términos de la secuencia mecanicista inicial.
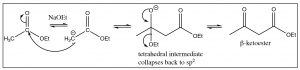
El anión enolato del éster ataca al carbonilo de otra molécula y el intermedio tetraédrico resultante colapsa de nuevo al carbonilo regenerando el anión etóxido que se utilizó para iniciar la formación de enolato. La diferencia entre las reacciones de Claisen y aldol es que el producto Claisen es un\(\beta\) -cetoéster, que puede ser una especie útil por derecho propio. Las condensaciones de Claisen también pueden formar anillos a través de condensaciones intramoleculares (que se conocen como ciclaciones Dieckmann).
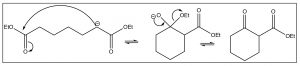
Tanto las condensaciones de Aldol como de Claisen se pueden realizar entre dos compuestos carbonílicos diferentes: sin embargo, si ambos son capaces de formar enolatos, existe la posibilidad de formar cuatro productos diferentes. Consideremos dos compuestos carbonílicos A y B, si el enol A reacciona con el carbonilo B, obtenemos el producto AB, pero si el enol B reacciona con el carbonilo A obtenemos el producto BA (que tendría una estructura diferente). A también se puede condensar con otra A para formar el producto AA, y de manera similar podríamos obtener BB. Por lo tanto, es importante controlar cuidadosamente las condiciones de reacción: por ejemplo, usando una base irreversible como LDA para formar primero el enolato. Esto excluye la posibilidad de que el enolado reaccione consigo mismo. Después, el otro componente se puede añadir lentamente a la mezcla de reacción y se puede llevar a cabo la condensación.