9.6: Michael Reacciones
- Page ID
- 77022
Recordemos que las condensaciones aldólicas dan como resultado compuestos carbonílicos\(\alpha ,\beta\) -insaturados, una funcionalidad que ya hemos discutido con cierta extensión.

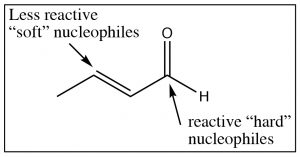
Estos grupos carbonilo conjugados pueden sufrir un ataque nucleófilo en el carbono carbonilo o en el\(\beta\) carbono, dependiendo de la naturaleza del nucleófilo. Por ejemplo: nucleófilos altamente reactivos (o “duros”) como Grignards o alquil-litios tienden a reaccionar en el carbono carbonilo, mientras que nucleófilos menos reactivos (blandos) como cupratos de dialquilo o nucleófilos reversibles como aminas o alcoholes tienden a reaccionar en el\(\beta\) carbono.
Los aniones formados a partir de\(\beta\) -dicetonas son relativamente poco reactivos (están estabilizados) y, por lo tanto, podríamos predecir que atacarán al carbonilo conjugado en la\(\beta\) posición — ¡y estaríamos en lo correcto! Esta reacción se llama la reacción de Michael.
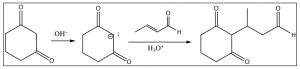
De hecho, podemos condensar la misma\(\beta\) -dicetona con una cetona conjugada diferente (no formada a partir de una condensación aldólica) para producir un intermedio que luego puede sufrir una condensación intramolecular de aldol como se muestra a continuación. Este procedimiento de dos pasos se llama la Anulación Robinson.
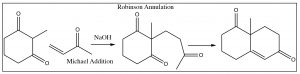
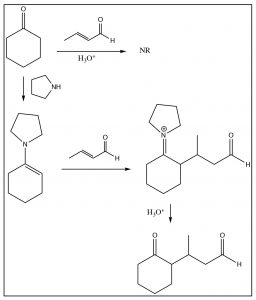
Desafortunadamente, esta reacción solo funciona bien con beta-dicetonas; una cetona simple no ataca el sistema conjugado. Sin embargo, hay una solución relativamente simple a esto, que es modificar la cetona para formar una enamina, que luego reaccionará como se muestra a continuación. Esta variación se conoce como la síntesis de enamina de cigüeña.


