9.7: Glicólisis
- Page ID
- 77004
La glucólisis es el nombre que le damos al grupo de reacciones que resultan en la división de una molécula de\(\mathrm{C-} 6\) glucosa en dos\(\mathrm{C-} 3\) unidades, la cual se acompaña de la producción global de\(\mathrm{ATP}\), la molécula que puede ser utilizada para proporcionar energía para impulsar reacciones químicas desfavorables como la construcción de biopolímeros como péptidos, polímeros de ácido nucleico (\(\mathrm{DNA}\)y\(\mathrm{RNA}\)), y la producción de grasas. Este proceso suele ser representado esquemáticamente, particularmente en textos de biología, pero cada paso del proceso es una reacción orgánica relativamente simple que se puede entender en términos de los principios que hemos aprendido durante el último año. El esquema general para la glucólisis se da a continuación [2], pero nuestra intención aquí no es que memorices cada paso para que pueda ser regurgitado; es para permitirte entender cómo y por qué estas reacciones ocurren de la manera en que lo hacen (o al menos la forma en que lo hacen en los sistemas biológicos).
Estaremos tratando estas reacciones desde una perspectiva de química orgánica, pero es importante señalar que en el cuerpo todas estas reacciones están mediadas por enzimas y cofactores que disminuyen la energía de activación para cada reacción. La primera parte de la vía de la glucólisis implica la conversión de la glucosa de azúcar, a un azúcar diferente, la fructosa. Por lo tanto comenzaremos por mirar brevemente la estructura y propiedades de los azúcares.
Glucosa:
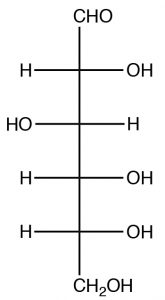
Si bien la glucosa parece compleja, ya hemos investigado los grupos funcionales presentes y todas las reacciones que aquí son importantes. La glucosa pertenece a la familia de compuestos llamados azúcares que forman parte de un grupo más grande, conocidos como carbohidratos, denotados por el sufijo -ose. Dado que tiene seis carbonos, la glucosa se conoce como hexosa (de manera similar, un azúcar de cinco carbonos se conocería como pentosa). La glucosa puede existir en varias formas; tanto de cadena abierta como cerrada. Consideramos primero la forma de cadena abierta. La forma más fácil de representar los azúcares es mediante el uso de una proyección Fischer (de hecho estas representaciones fueron inventadas solo para este propósito). Recuerda que en una proyección Fischer, los enlaces horizontales están apuntando fuera del plano y todos están eclipsados. La forma natural de glucosa es D-Glucosa\(\rightarrow\).
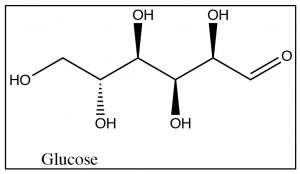
Obsérvese que hay cuatro centros quirales en la glucosa, y por lo tanto existen\(16\) (\(2^{4}\)) posibles estereoisómeros, muchos de los cuales ocurren de forma natural. La designación D tiene que ver con la estereoquímica en la posición 5 y no se refiere a la dirección de rotación de la luz polarizada en el plano. (Si bien es posible designar R o S para cada centro quiral [3], no es posible designar R o S para la molécula como un todo). Nótese que la glucosa también tiene un grupo aldehído (en la posición 1) y, por lo tanto, también pertenece a la clase de azúcares llamados aldosis.
En su forma de cadena abierta, la glucosa tiene un grupo aldehído y cinco grupos hidroxilo y, como cabría esperar, aquí hay un gran potencial de reacciones, tanto inter- como intramoleculares. En una solución, la glucosa comúnmente existe en la forma hemiacetal, en la que el\(\mathrm{OH}\) grupo en\(\mathrm{C-} 5\) ha atacado al grupo carbonilo para formar un anillo de seis miembros que se conoce como la forma de piranosa (el pirano es un anillo heterocíclico de seis miembros con un átomo de oxígeno en él). La forma de piranosa generalmente se dibuja en forma de silla como se muestra a continuación.
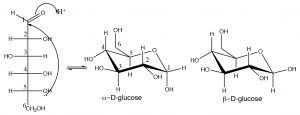
La formación de hemiacetales produce dos configuraciones posibles, pero en lugar de llamarlas R y S, las etiquetamos alfa y beta. En forma alfa, el\(\mathrm{OH}\) carbono 1 está en el lado opuesto del anillo al\(\mathrm{CH}_{2}\mathrm{OH}\) (\(\mathrm{C-} 6\)de la cadena original), la forma beta tiene el\(\mathrm{OH}\) grupo en el mismo lado que el\(\mathrm{CH}_{2}\mathrm{OH}\). Estas dos formas son estereoisómeros porque tienen la configuración opuesta en\(\mathrm{C-} 1\), pero a diferencia de los estereoisómeros típicos, pueden interconvertirse mediante la apertura del anillo del hemiacetal y el cierre del anillo. Se les llama formas anoméricas y\(\mathrm{C-} 1\) se les conoce como el carbono anomérico. Dichos carbonos pueden identificarse por el hecho de que tienen dos oxígenos unidos a ellos. En una solución acuosa de glucosa en equilibrio, menos del 1% está presente en la forma de cadena abierta, pero como siempre hay una concentración de equilibrio presente, las formas alfa y beta pueden y se interconvertirán a través de esta forma de cadena abierta. Como cabría esperar, la forma beta es más estable (porque la\(\mathrm{OH}\) es ecuatorial) y en equilibrio hay alrededor de 64% beta. Para azúcares como la glucosa, también existe la posibilidad de que se pueda formar un anillo de cinco miembros por la reacción del alcohol en\(\mathrm{C-} 4\) con el carbonilo. Nuevamente, son posibles dos formas (alfa y beta), que se pueden interconvertir a través de la apertura del anillo. Esta forma de anillo de cinco miembros se llama la forma furanosa (el furano es un anillo de cinco miembros con un oxígeno).
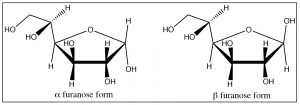
Fructosa:
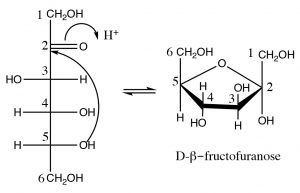
La fructosa es otro azúcar de seis carbonos. Se diferencia de la glucosa en que tiene una cetona en lugar de un aldehído en\(\mathrm{C-} 2\); por esta razón, se le llama cetosa (en lugar de aldosa). La fructosa suele existir en un anillo hemiacetal de cinco miembros formado por reacción del\(\mathrm{OH}\) at\(\mathrm{C-} 5\) con la cetona carbonilo at\(\mathrm{C-} 2\). El anillo resultante de cinco miembros se llama forma furanosa (furano es un anillo de cinco miembros con un oxígeno) y típicamente los anillos de furanosa se representan usando otra representación estructural: la proyección Haworth, que se muestra aquí. En esta estructura, el anillo se dibuja como un plano (aunque no lo es, por supuesto), y los sustituyentes están por encima o por debajo del plano del anillo. De la misma manera que la glucosa, la fructosa puede existir ya sea en las formas alfa o beta.