5.3: Sistema de Chiralidad y Nombramiento R/S
- Page ID
- 76454
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Aparte de los isómeros geométricos, existe otro tipo de estereoisómero que se relaciona con una propiedad especial llamada quiralidad. Comenzaremos con los conceptos básicos de la quiralidad, luego ampliaremos el tema más a partir de ahí.
5.3.1 Quiral y Chiralidad
Para hablar de quiralidad, primero echemos un vistazo más de cerca a nuestras manos, mano izquierda y mano derecha. La mano izquierda puede considerarse como la imagen especular de la mano derecha, y viceversa. Ahora intentemos superponer (superponer) la mano izquierda sobre la mano derecha, ¿puedes hacer eso?
¡No! No importa cuánto lo intentes, la mano izquierda no se puede superponer a la mano derecha. Esto se debe a la propiedad especial de la mano, que se llama quiralidad. Tanto la mano izquierda como la derecha son quirales (ky-ral), y muestran quiralidad. Quiral deriva de la palabra griega cheir, que significa “mano”, y quiralidad significa “mano”.

La definición de la quiralidad es la propiedad de cualquier objeto (molécula) de ser no superponible en su imagen especular. La mano izquierda y derecha son imagen especular entre sí, y no son superponibles, por lo que tanto la mano izquierda como la derecha son quirales. Aparte de eso, también puedes encontrar muchos otros objetos en la vida diaria que también muestran quiralidad.


Si un objeto es superponible sobre su imagen especular (para tal caso el objeto y su imagen especular son exactamente idénticos), entonces este objeto no es quiral, eso puede decirse como aquiral.


En química orgánica, nos interesan las moléculas orgánicas que son quirales. Veamos los siguientes modelos moleculares que representan una molécula y su imagen especular.

En los modelos aquí, las cuatro bolas con diferentes colores representan cuatro sustituyentes diferentes, y las dos estructuras son imagen especular entre sí. El esfuerzo de intentar superponer una estructura a la otra no funciona. Por lo tanto, de acuerdo con la definición de quiral/quiralidad, ambas moléculas son no superponibles sobre la imagen especular, por lo que tanto quirales como muestran quiralidad.
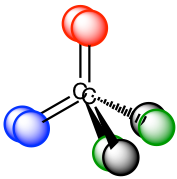
La quiralidad de la molécula resulta de la estructura del carbono central. Cuando el carbono central es carbono sp 3, y unido con cuatro grupos diferentes (representados por cuatro colores diferentes en el modelo), la molécula es quiral. El carbono central se llama centro de quiralidad (o centro asimétrico). La molécula con un centro de quiralidad debe ser quiral. El centro de quiralidad también se puede llamar centro asimétrico. Utilizaremos el término centro de quiralidad en este libro.
Es muy recomendable que el conjunto de modelos moleculares se utilice como herramienta de aprendizaje en este capítulo. Ensamblar el modelo como se muestra arriba para entender el concepto de quiral y quiralidad. El modelo también es muy útil para la asignación R/S más adelante en esta sección.Como resumen, un centro de quiralidad (asimétrico) debe cumplir dos requisitos:
- sp 3 carbono;
- unidos con cuatro grupos diferentes.
Ejemplos
Para los siguientes compuestos, etiquetar cada uno de los centros de quiralidad con una estrella.
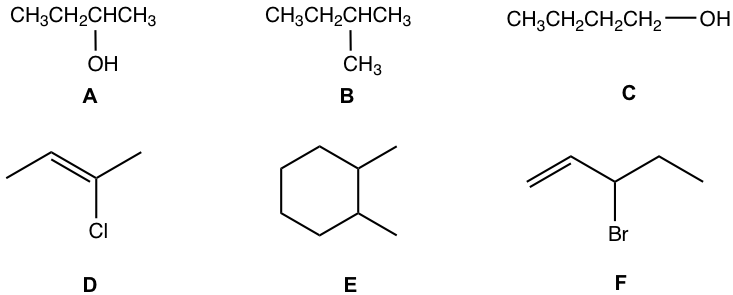
Enfoque:
- Los carbonos en CH 3 o CH 2 NUNCA son centros de quiralidad. El centro de quiralidad debe ser el carbono unido con una rama (o ramas).
- El carbono de doble enlace sp 2 NUNCA es un centro de quiralidad.
- El carbono en un anillo también puede ser centro de quiralidad siempre que cumpla con los dos requisitos.
- No todos los compuestos anteriores tienen un centro de quiralidad.
Solución:
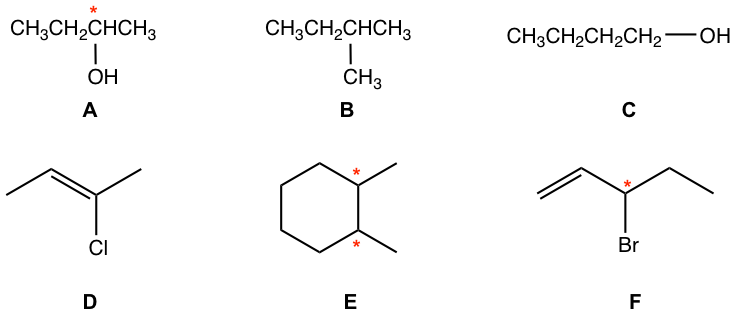
Ejercicios 5.2
- Dibujar la estructura de los siguientes compuestos, determinar cuál tiene un centro de quiralidad y etiquetarlo con una estrella.
a) 1-bromobutano,
b) 1-pentanol,
c) 2-pentanol,
d) 3-pentanol,
e) Ácido 2-bromopropanoico
f) 2-metilciclohexanona
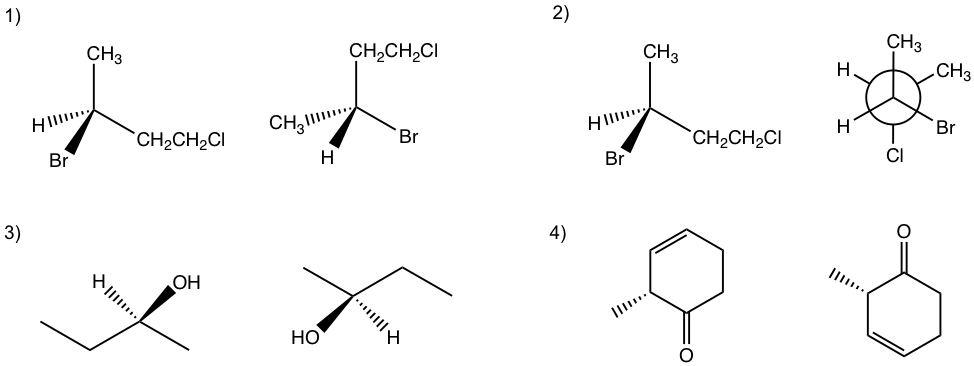
2. Marcar todos los centros de quiralidad en las siguientes moléculas.
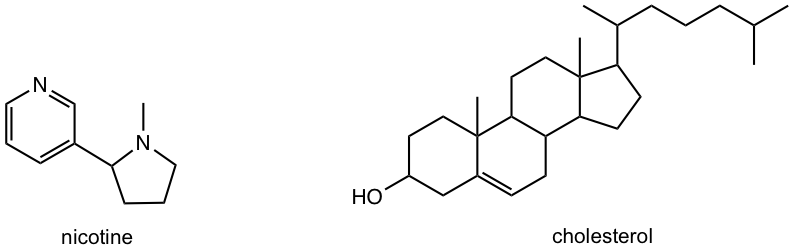
Respuestas a las preguntas de práctica Capítulo 5
5.3.2 Estereoisómero con un centro de quiralidad — Enantiómeros
Para el 2-butanol, somos capaces de reconocer que C2 es el centro de quiralidad.

La fórmula de perspectiva muestra la estructura 3D del 2-butanol de dos maneras diferentes, y son imágenes especulares no superponibles entre sí.
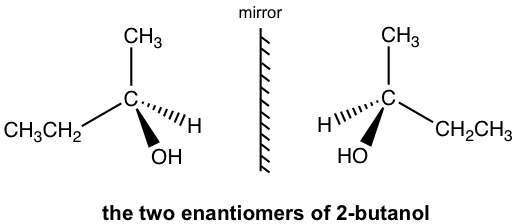
Las dos imágenes especulares son moléculas diferentes. Tienen la misma unión, pero difieren en la forma en que los átomos se disponen en el espacio. Entonces las dos moléculas son estereoisómeros. Este tipo específico de estereoisómero aquí se define como enantiómeros. Las moléculas que son un par de imágenes especulares no superponibles entre sí se denominan enantiómeros.
Propiedades importantes sobre los enantiómeros:
- Los enantiómeros son un par de imágenes especulares no superponibles.
- Los enantiómeros son un par de moléculas, ambos quirales y muestran quiralidad. (El enantiómero debe ser quiral).
- Para cualquier molécula quiral, debe tener su enantiómero, es decir, la imagen especular a la molécula.
- La molécula aquiral no tiene enantiómero. La imagen especular de una molécula aquiral es la molécula idéntica a sí misma.
Ejemplos: Dibujar el par de enantiómeros del ácido 2-bromopropanoico.
Enfoque:
Para dibujar la estructura 3D de cualquier enantiómero, necesitamos usar una fórmula en perspectiva con cuñas sólidas y discontinuas para mostrar las disposiciones tetraédricas de los grupos alrededor del carbono sp 3 (consulte la sección 2.11). De los cuatro enlaces en carbono tetraédrico, dos enlaces se encuentran dentro del plano del papel se muestran como líneas ordinarias, la cuña sólida representa un enlace que apunta hacia fuera del plano del papel, y la cuña discontinua representa un enlace que apunta detrás del plano del papel. Para el primer enantiómero, puedes dibujar los cuatro grupos con cualquier arreglo, luego dibujar el otro enantiómero dibujando la imagen especular del primero. Tenga en cuenta, aunque parece que hay diferentes formas de mostrar los enantiómeros, solo hay dos enantiómeros totales, aprenderemos en la siguiente sección cómo identificar y designar cada uno de ellos.
Varias formas posibles de mostrar las estructuras se incluyen en la respuesta aquí. Sin embargo, tu respuesta puede ser diferente a cualquiera de ellas, siempre y cuando se muestren un par de imágenes especulares.
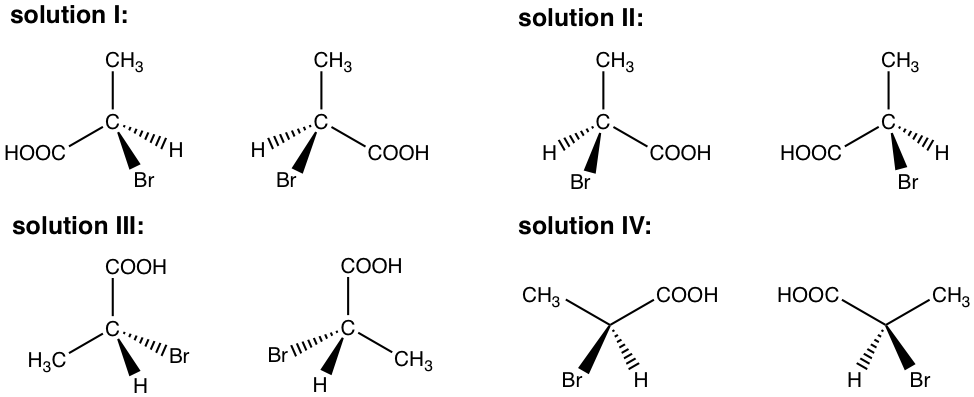
Ejercicios 5.3
Dibujar el par de enantiómeros de 2-cloro-1-propanol.
Respuestas a las preguntas de práctica Capítulo 5
5.3.3 Sistema de Nombramiento R/S de Centro de Chiralidad
Los dos enantiómeros son compuestos diferentes, aunque son muy similares. Por lo tanto necesitamos un sistema de nomenclatura para distinguir entre ellos, para darle a cada uno una designación diferente para que sepamos de cuál estamos hablando. Ese es el sistema de nomenclatura R/S definido en la IUPAC. La designación R/S se puede determinar siguiendo la regla Cahn-Ingold-Prelog, la regla ideada por R. S Cahn, C. Ingold y V. Prelog.
Para un par de enantiómeros con un centro de quiralidad, un enantiómero tiene la configuración R y el otro tiene la configuración S.Regla Cahn-Ingold-Prelog:
- Asignar prioridades de los grupos (o átomos) unidos al centro de quiralidad siguiendo las mismas reglas de prioridad que para el sistema E/Z (sección 5.2). El grupo de mayor prioridad está etiquetado como #1, y el grupo de menor prioridad etiquetado como #4 en este libro.
- Orienta la molécula de la manera en que el grupo de prioridad más baja (#4) apunte lejos de ti.
Para el sentido contrario a las agujas del reloj, la designación es S —, siniestra, significa “izquierda” en latín.
Tomemos como ejemplo la siguiente molécula para practicar la regla:
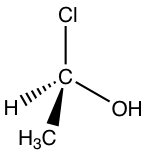
Paso 1: Se asignan las prioridades.
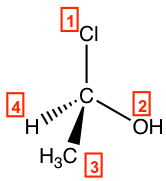
Paso 2: Reoriente la molécula, por lo que H (#4, prioridad más baja) está en la posición alejada de nosotros. Entonces los otros tres grupos se organizarán de esta manera:
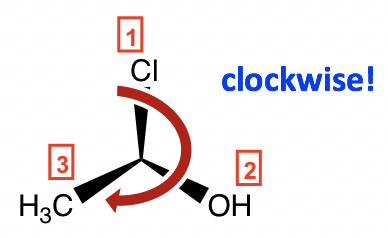
Paso 3: Ir en la dirección desde #1 → #2 → #3, es en el sentido de las agujas del reloj, por lo que a este enantiómero se le asigna la configuración R, y el nombre completo de la molécula es (R) -1-cloroetanol.
Ahora vamos a asignar la configuración del otro enantiómero:
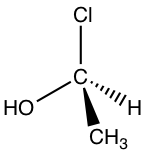
Siguiendo los mismos pasos, alejar a H de nosotros, y el arreglo de los otros tres grupos es:
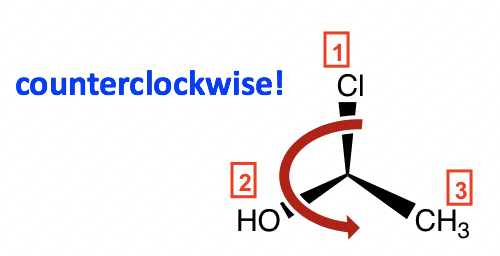
El sentido contrario a las agujas del reloj da la configuración S, y el nombre completo de la molécula es (S) -1-cloroetanol.
Ejemplos: Asignar configuración R/S del centro de quiralidad.
1.
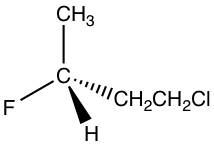
Solución:

2.
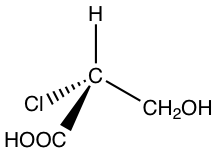
Solución:

Más consejos prácticos sobre la asignación R/S con la regla Cahn-Ingold-Prelog:
- Asignar prioridad es el primer reto posible para aplicar la regla C.I.P. Revisar y practicar los lineamientos en la sección 5.2.
- El segundo desafío es reorientar la molécula (para organizar el grupo #4 lejos de ti). El modelo de molécula será de gran ayuda para este propósito. Ensamble un modelo molecular con cuatro colores diferentes conectados sobre el carbono. Compara tu modelo con la estructura dada y haz coincidir la prioridad asignada a cada color, por ejemplo, el rojo es #1, el azul es #2, etc. luego gira el modelo para organizar el grupo más bajo (#4) lejos de ti y ver cómo se ubican los otros grupos para obtener la respuesta.
Para la fórmula de perspectiva de los enantiómeros, es importante conocer las siguientes propiedades:
- Un (número impar de) conmutador (intercambiable) para un par de grupos invertir la configuración del centro de quiralidad;
- Dos (número par de) conmutadores recuperan la configuración original.
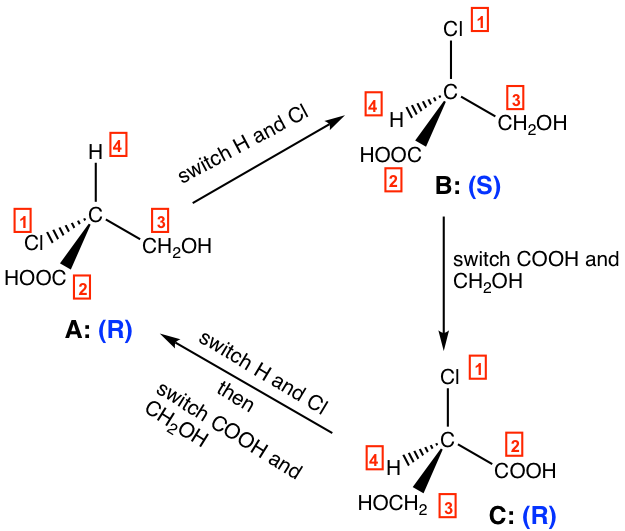
Para las estructuras anteriores:
- Un interruptor de A conduce a B, A es R y B es S, entonces A y B son enantiómeros ,
- Un interruptor de B conduce a C, B es S y C es R, así que B y C son enantiómeros ,
- Dos interruptores de C conduce a A, tanto C como A son R, por lo que C y A son idénticos.
Ejercicios 5.4
Determinar la configuración R/S del centro de quiralidad en los siguientes compuestos.
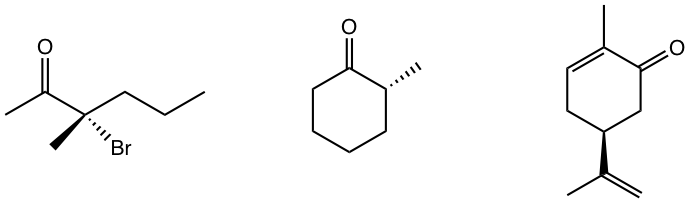
Respuestas a las preguntas de práctica Capítulo 5
Ejercicios 5.5
Determinar la relación para cada par de moléculas: enantiómeros, idénticos, isómeros constitucionales, no isómero: