6.8: Espectroscopia de RMN ¹³C
- Page ID
- 76344
Para el elemento carbono, el isótopo 12 C más abundante (con ~ 99% de abundancia natural) no tiene un momento magnético nuclear, y por lo tanto es NMR-inactivo. Por lo tanto, la RMN C se basa en el isótopo 13 C, que representa alrededor del 1% de los átomos de carbono en la naturaleza y tiene un momento dipolar magnético igual que un protón. Las teorías que hemos aprendido sobre la espectroscopia de RMN 1H también se aplican a la RMN de 13 C, sin embargo con varias diferencias importantes sobre el espectro.
El momento magnético de un núcleo de 13 C es mucho más débil que el de un protón, lo que significa que las señales de RMN de 13 C son inherentemente mucho más débiles que las señales de protones. Esto, combinado con la baja abundancia natural de 13 C, significa que es mucho más difícil observar las señales de carbono. Por lo general, se requieren muestras con alta concentración y gran número de escaneos (miles o más) para reducir la relación señal/ruido a niveles aceptables para 13 espectros de RMN C.
Equivalente Químico
Para los carbonos que son equivalentes químicos, solo muestran una señal en 13 C NMR como protones similares para 1 HNMR. Por lo que es muy importante poder identificar carbonos equivalentes en la estructura, a fin de interpretar correctamente el espectro de 13 C NMR. Tomando como ejemplo el tolueno, hay cinco conjuntos de diferentes átomos de carbono (mostrados en diferentes colores), por lo que hay cinco señales en el espectro de 13 C RMN del tolueno.
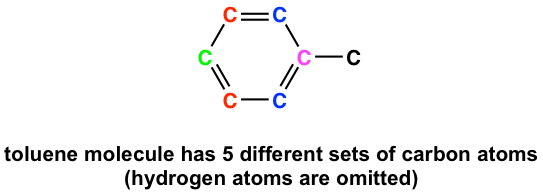
Desplazamiento Químico
Los núcleos de 13 C tienen diferente valor de g (la relación magnetogírica) en comparación con los núcleos de 1 H, por lo que las frecuencias de resonancia de 13 núcleos C son diferentes a las de los protones en el mismo campo aplicado (refiriéndose a la fórmula. 6.4, en la sección 6.5). En un instrumento con un imán de 7.05 Tesla, los protones resuenan a aproximadamente 300 MHz, mientras que los carbonos resuenan a aproximadamente 75 MHz. Esto nos permite observar las señales de 13 C utilizando una 'ventana' completamente separada de frecuencias de radio. Al igual que en 1H NMR, el tetrametilsilano (TMS) también se usa como compuesto estándar en 13 experimentos de RMN C para definir el 0 ppm, sin embargo es la señal de los cuatro átomos de carbono equivalentes en TMS la que sirve como estándar. Los desplazamientos químicos para núcleos de 13 C en moléculas orgánicas se extienden en un rango mucho más amplio de aproximadamente 220 ppm (ver Cuadro 6.3).
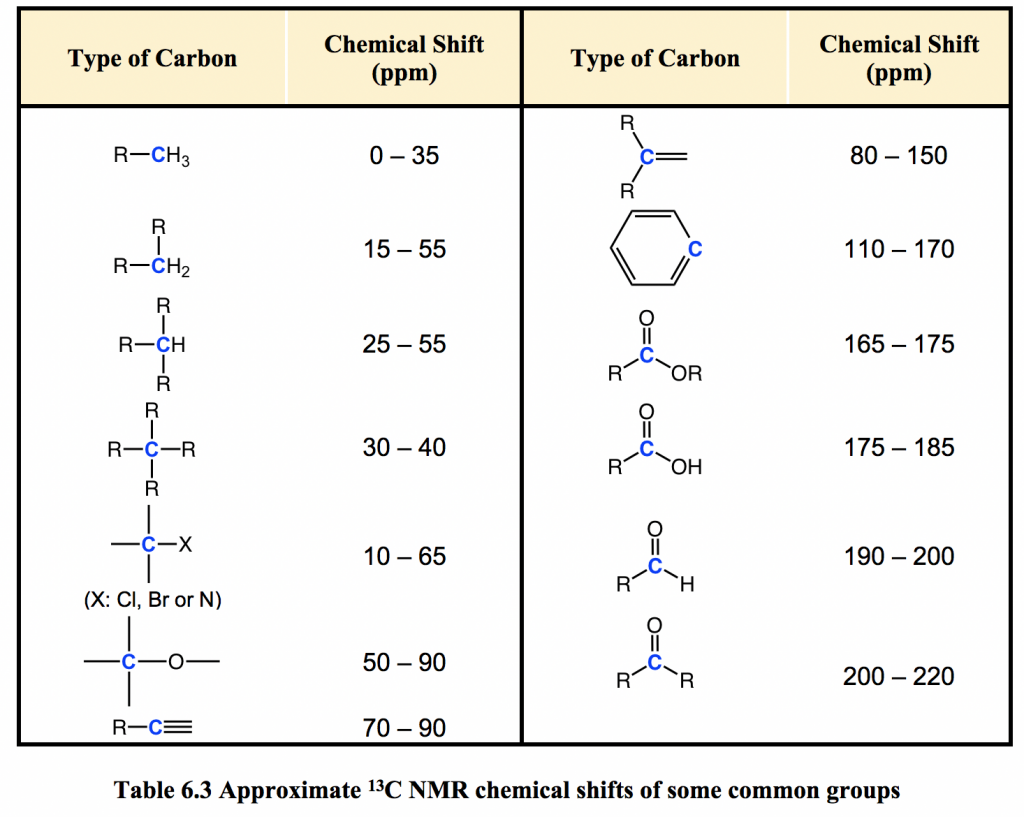
El desplazamiento químico de un núcleo de 13 C está influenciado esencialmente por los mismos factores que influyen en el desplazamiento químico de un protón: el efecto deshielding de los átomos electronegativos y los efectos de anisotropía tienden a desplazar las señales campo abajo (mayor frecuencia de resonancia, con mayores desplazamientos químicos). Además, la hibridación sp 2 da como resultado un gran cambio de campo abajo. Las señales de RMN de 13 C para los carbonos carbonílicos son generalmente las más alejadas (170-220 ppm), debido tanto a la hibridación sp 2 como al doble enlace con el oxígeno.
Integración y Acoplamiento en RMN de 13 C
A diferencia de 1H NMR, el área bajo una señal de RMN de 13 C no se puede utilizar fácilmente para determinar el número de carbonos a los que corresponde. Las señales para algunos tipos de carbonos son inherentemente más débiles que para otros tipos, por ejemplo, los picos correspondientes a los carbonos de carbonilo son mucho más pequeños que los de los picos de metilo o metileno (CH 2). Por esta razón, la integración de la señal generalmente no es útil en la espectroscopía de RMN 13 C.
Debido a la baja abundancia natural de 13 núcleos C, el acoplamiento espín-espín entre dos átomos de C no equivalentes es insignificante. Sin embargo, 13 núcleos C se acoplan a protones cercanos, lo que resulta en espectros complicados. Para mayor claridad, los químicos generalmente utilizan una técnica llamada desacoplamiento de banda ancha, que esencialmente 'desactiva 'el acoplamiento C-H, dando como resultado un espectro en el que todas las señales de carbono son singletes. A continuación se muestra el espectro de RMN 13C desacoplado de protones del acetato de etilo en CDCl 3 (Fig. 6.8a), mostrando las cuatro señales esperadas, una para cada uno de los carbonos.
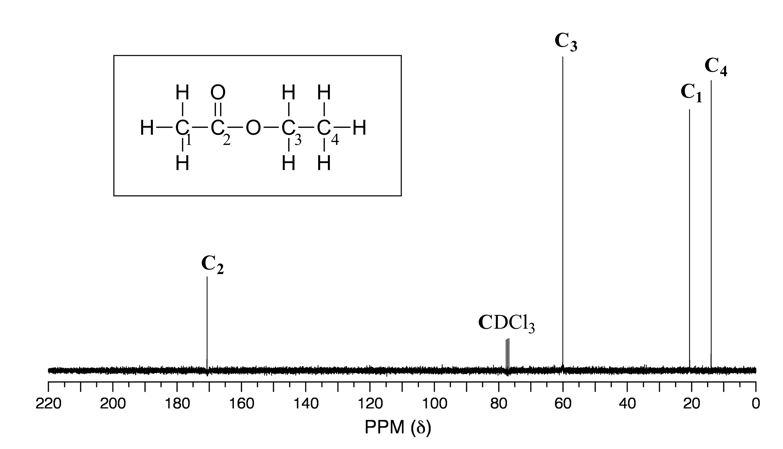
Para nuestro propósito de clase, los espectros de RMN de 13 C generalmente se utilizan como información de apoyo para confirmar la estructura de un compuesto.
Ejercicios 6.2
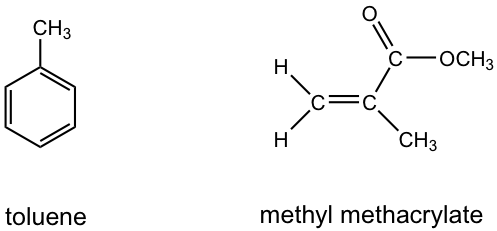
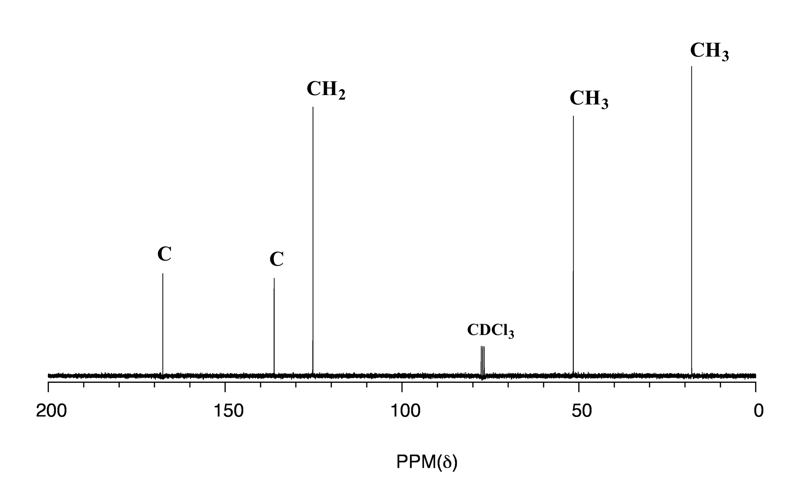
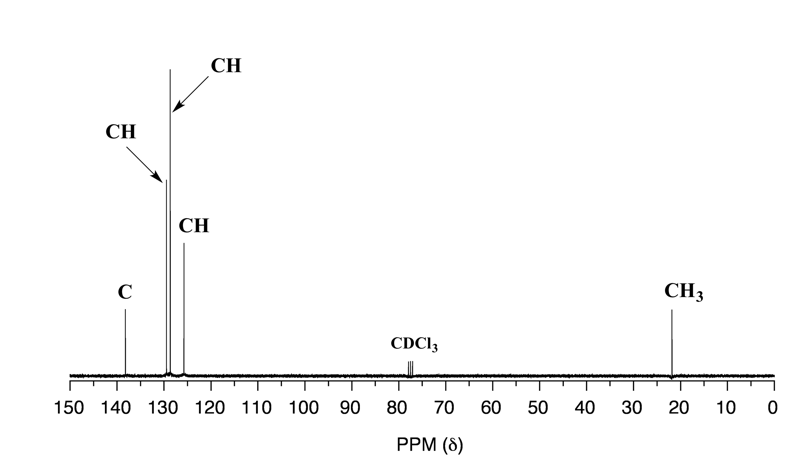 Respuestas a las preguntas de práctica Capítulo 6
Respuestas a las preguntas de práctica Capítulo 6

