6.7: Espectros de RMN 1H e Interpretación (Parte II)
- Page ID
- 76345
6.7.1 Integración de áreas de señal
La computadora en el instrumento de RMN puede ser instruida para integrar matemáticamente el área bajo una señal o grupo de señales. El proceso de integración de la señal es muy útil en el espectro de RMN 1H, ya que el área bajo una señal es proporcional al número de protones a los que corresponde la señal.
La Fig. 6.7a es el espectro de RMN 1H de 1,4-dimetilbenceno con línea de integración (líneas azules). La línea de integración generada por la computadora siempre está en forma de curva que se asemejan a pasos. Los números de integración también son generados por la computadora junto con la curva, que muestran el área relativa de cada señal (los números de integración en los espectros reales suelen ser con decimales, los números enteros se muestran aquí por simplicidad).
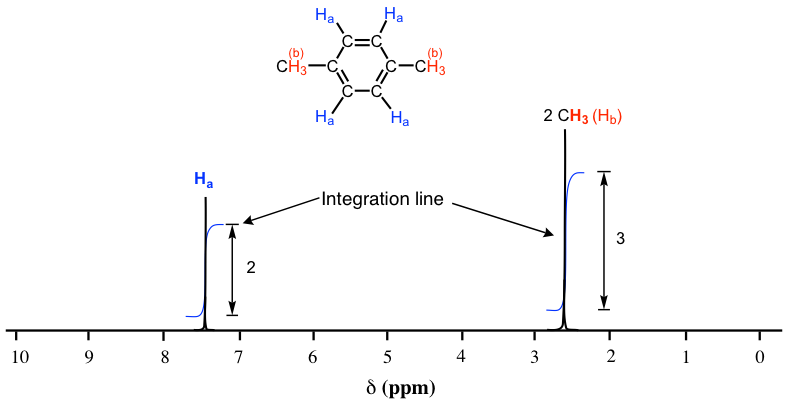
Como comentamos anteriormente, la molécula de 1,4-dimetilbenceno tiene dos conjuntos de protones equivalentes: los cuatro protones aromáticos (H a) y los seis protones metilo (H b). La integración del área bajo el pico a 2.6 ppm es 1.5 veces mayor que el área bajo el pico a 7.4 ppm. Tenga en cuenta que el número de integración muestra la relación relativa del número de protones, no el número real. La relación 3 a 2 aquí coincide con la relación del número real 6 a 4. Esta información de integración, junto con el conocimiento del cambio químico que hemos aprendido antes, nos permite asignar los picos: pico a 7.4 ppm corresponden a protones (H a) en el anillo bencénico, y el pico a 2.6 ppm corresponden a dos grupos metilo (H b).
6.7.2 División de señal (acoplamiento)
En los espectros de RMN 1H que hemos visto hasta ahora, cada conjunto de protones genera una única señal de RMN. Esto no es tan común para 1 HNMR en realidad. De hecho, los espectros de RMN 1H de la mayoría de las moléculas orgánicas contienen señales que se 'dividen' en dos o más picos que se llaman división (o acoplamiento). Los espectros con división de picos pueden parecer más complicados, sin embargo, este comportamiento de división proporciona información muy útil sobre la estructura de un compuesto.
Consideremos el espectro para 1,1,2-tricloroetano (Fig. 6.7b). En este y en otros espectros a seguir, se muestran las expansiones de señales individuales para que los patrones de división de señal sean reconocibles.
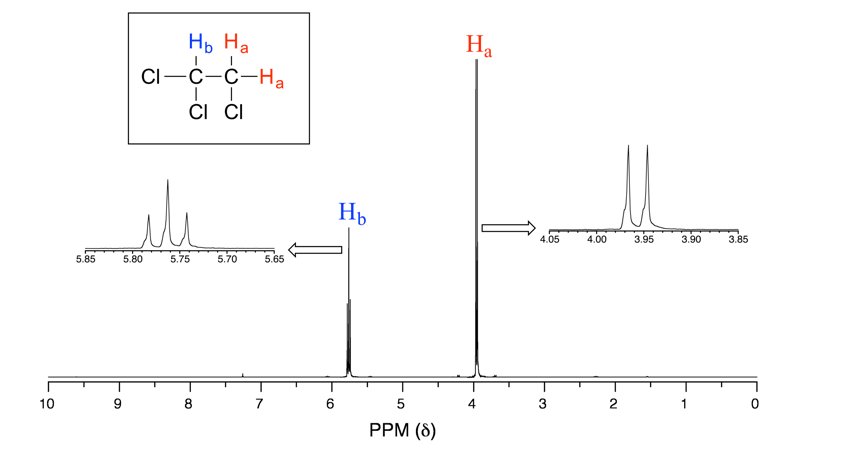
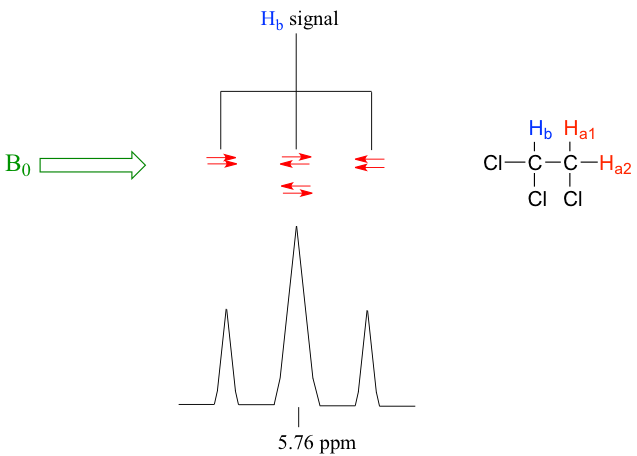
La señal a 3.96 ppm, correspondiente a los dos protones Ha, se divide en dos picos de igual altura (y área) —esto se conoce como doblete. La señal de Hb a 5.76 ppm, por otro lado, se divide en tres picos, con el pico medio más alto que los dos picos externos y la relación de integración entre los tres picos es 1:2:1, dicha señal de división se denomina triplete.
La división de la señal es causada por el acoplamiento espín-espín, término que describe las interacciones magnéticas entre átomos de hidrógeno no equivalentes que están con 2 o 3 enlaces de los hidrógenos que producen la señal. Los protones cercanos tienen un momento magnético que puede ser contra o con el campo magnético externo, por lo tanto, divide los niveles de energía de los protones cuya señal se está observando, y resulta en la división de la señal en múltiples picos (los términos 'división' y 'acoplamiento' se utilizan a menudo indistintamente cuando se discute RMN).
El acoplamiento más típico que observamos en este curso es de hidrógenos vecinales no equivalentes que están a 3 enlaces de distancia, es decir, los hidrógenos en los carbonos adyacentes. Esto también se llama acoplamiento vecinal o acoplamiento de tres enlaces.
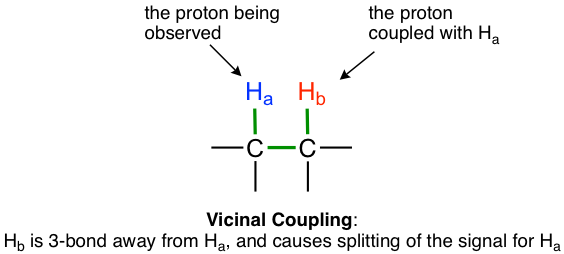
Una regla simple que se aplica para predecir el número de picos (o patrón de división) esperados del acoplamiento y la regla en 1 H NMRI:
número de picos = n + 1
(n es el número de hidrógenos vecinales no equivalentes)
Examinaremos el patrón de división con diferente número de n:
- Cuando n=0, la señal es un singlete, o tiene solo un pico, como las señales observadas en la Fig. 6.6d y Fig. 6.7a.
- Cuando n=1, la señal es un doblete con dos picos. La relación de área de los dos picos para un doblete es 1:1. El espacio entre los dos picos se denomina constante de acoplamiento, J ab, medida en Hz.
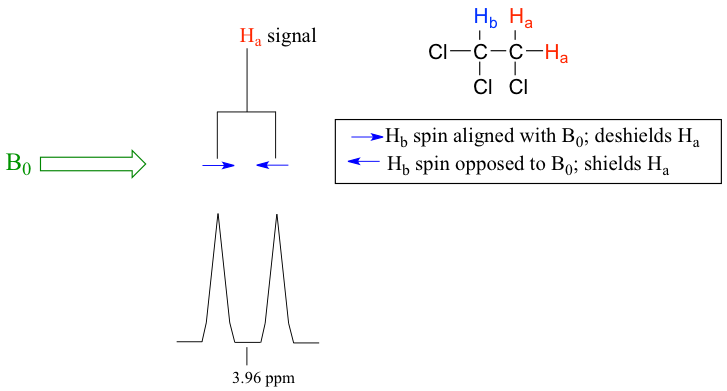
Para el ejemplo del compuesto 1,1,2-triclorometano, la señal de los protones H a encaja en esta situación. Con un solo protón vecinal, H b, sobre el carbono adyacente, la señal de H a se muestra como doblete.
- Cuando n=2, la señal es un triplete con tres picos. Los tres picos de triplete tienen la relación del área como 1:2:1.
En el mismo compuesto 1,1,2-triclorometano, la señal del protón H b encaja en esta situación. Con dos protones vecinales, 2 H a, sobre el carbono adyacente, la señal de H b se muestra como un triplete.
- Cuando n=3, la señal es un cuarteto, eso significa cuatro picos. Los cuatro picos del cuarteto tienen la relación de área de 1:3:3:1.
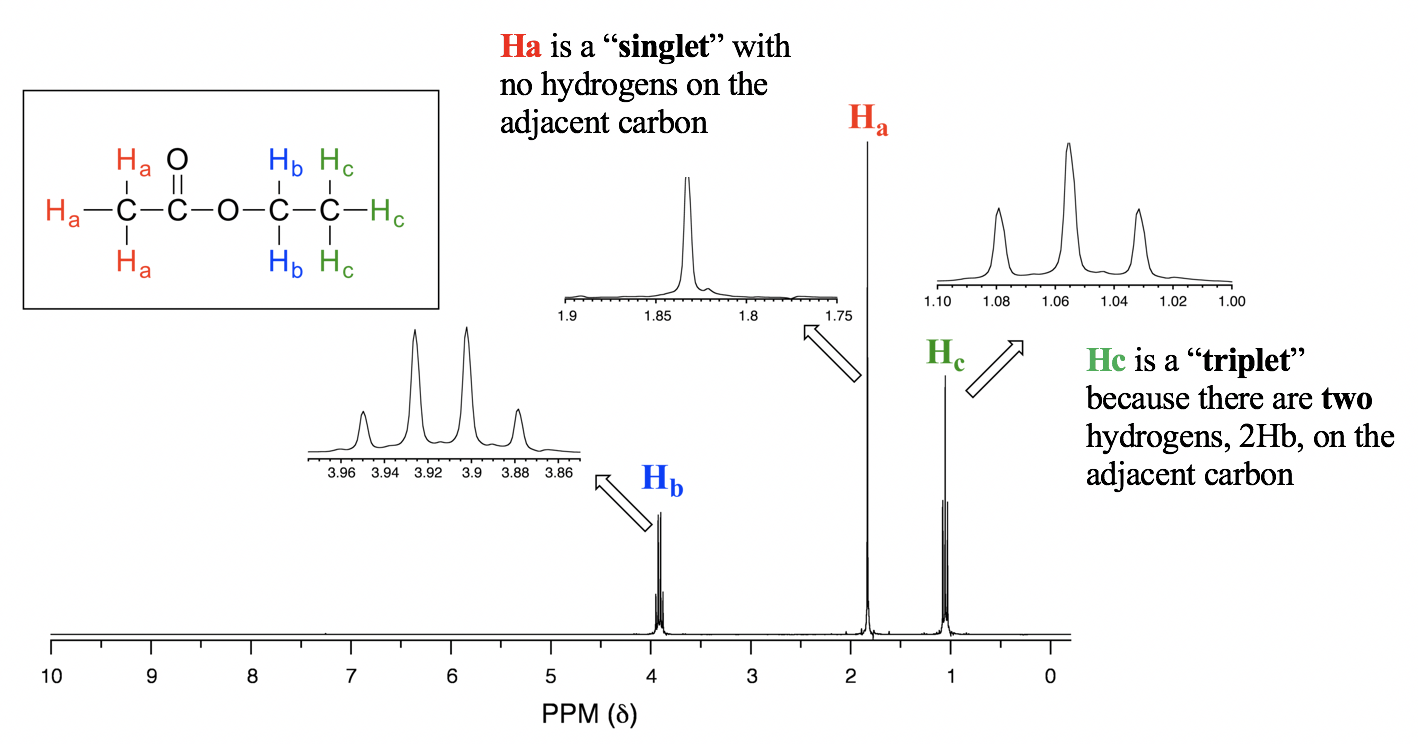
Para el espectro de acetato de etilo (Fig. 6.7e), la señal de H b es un cuarteto, debido a que hay tres protones vecinales 3 H c en el carbono adyacente. Tenga en cuenta que el carbono con H b conectado con oxígeno en el otro lado, y no hay átomos de hidrógeno en ese átomo de oxígeno, por lo que solo se aplica el acoplamiento con tres protones vecinales.
- Cuando n≥4, la señal se puede llamar multiplete. Teóricamente, con n aumentar la señal se divide en más picos y el número total de picos es “n+1”. Sin embargo, los pequeños picos en los lados pueden o no ser capaces de ser observados ya que podrían fusionarse en ruido. La señal con más de cuatro picos generalmente se llama como multiplete, y no es tan crítico decir exactamente cuántos picos participan en un multiplete.
Notas adicionales sobre la división de la señal:
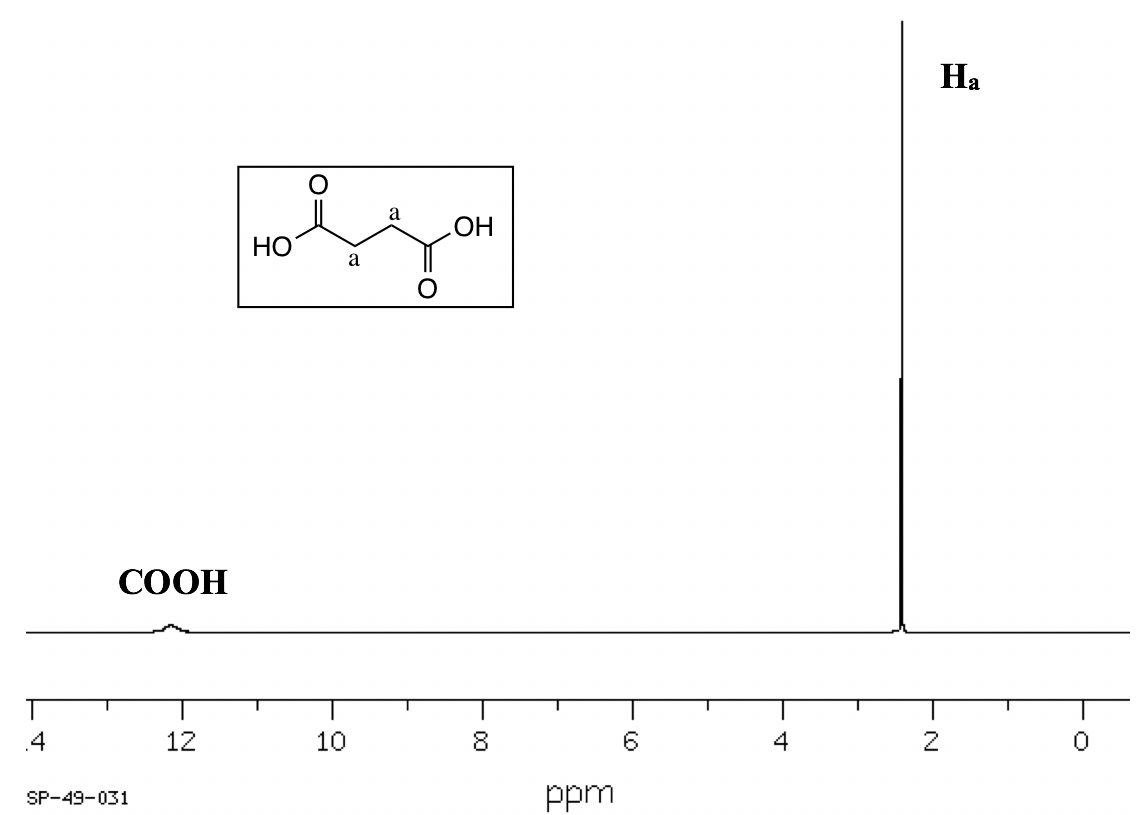
- La división (acoplamiento) solo ocurre entre protones no equivalentes. Para protones equivalentes, no hay acoplamiento. En el espectro del ácido succínico (Fig. 6.7f) por ejemplo, los protones en los dos carbonos medios son equivalentes (H a), por lo que no hay acoplamiento entre ellos y muestran un singlete.
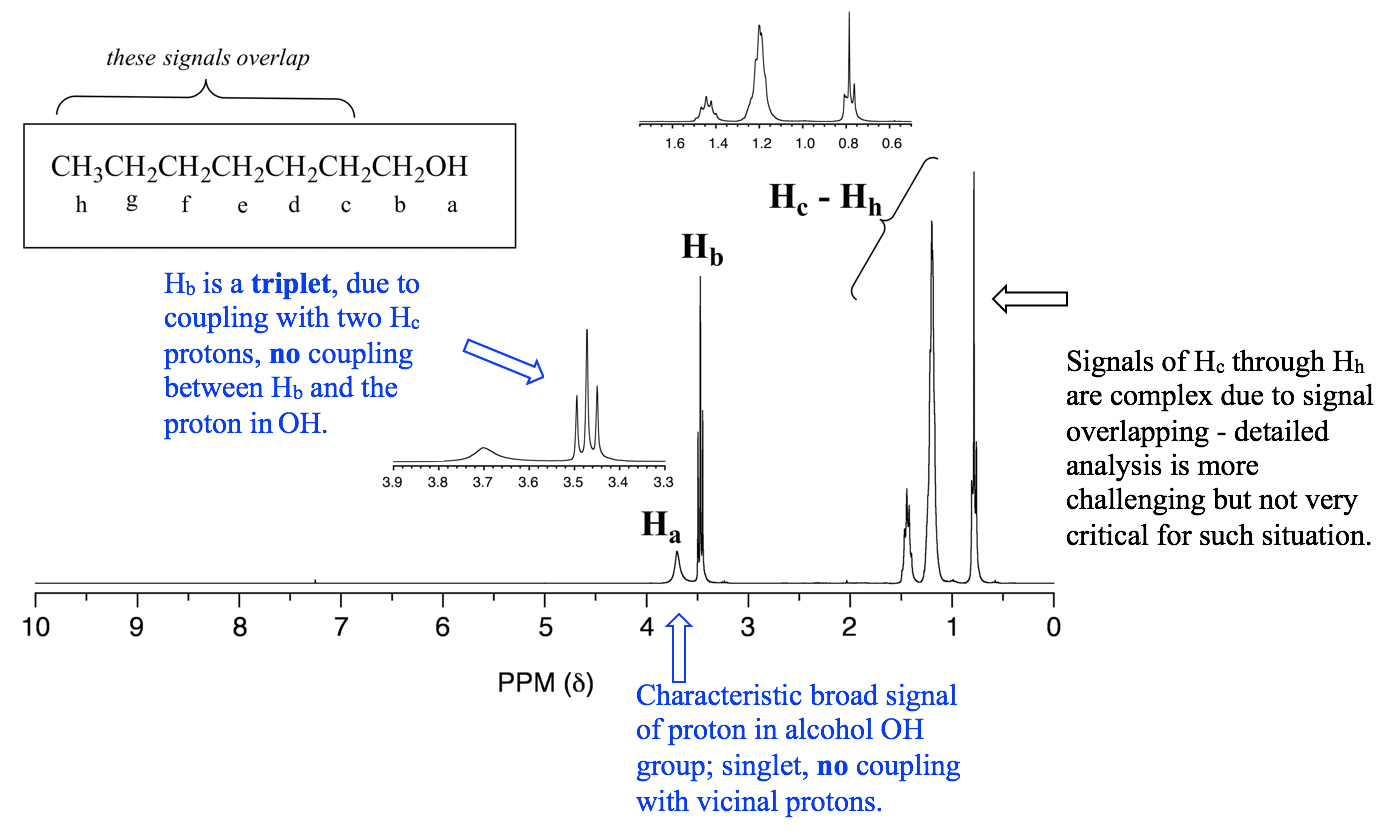
2. Los protones en OH o NH generalmente no se acoplan con hidrógenos vecinales. Los protones OH y NH son lo suficientemente ácidos como para intercambiar rápidamente entre diferentes moléculas, por lo que los protones vecinos nunca 'sienten' su influencia. Ver el ejemplo específico del espectro de 1-heptanol en la Fig. 6.7g.
6.7.3 Práctica de RMN de 1 H
Asignación de señal basada en la estructura dada
Con la estructura de un compuesto dada, podemos aplicar todo el conocimiento sobre 1H RMN para asignar las señales en el espectro, es decir, identificar una determinada señal proviene de la cual el hidrógeno (es).
Ejemplos
Coincidir el espectro de RMN 1H a continuación con su compuesto correspondiente, y asignar todas las señales.
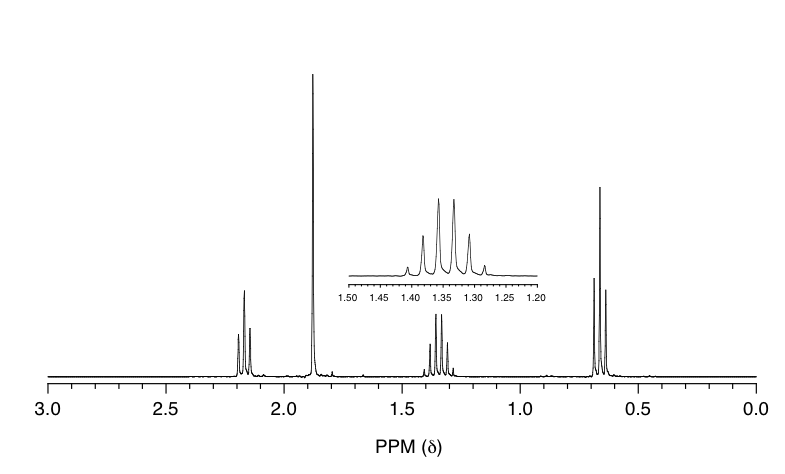
a) ciclopentanona b) 3-pentanona c) butaldehído d) 2-pentanona
e) 4-heptanona f) 1-buteno
Enfoque: Es buena idea dibujar la estructura de cada compuesto y tratar de ver cuáles coinciden con el espectro.
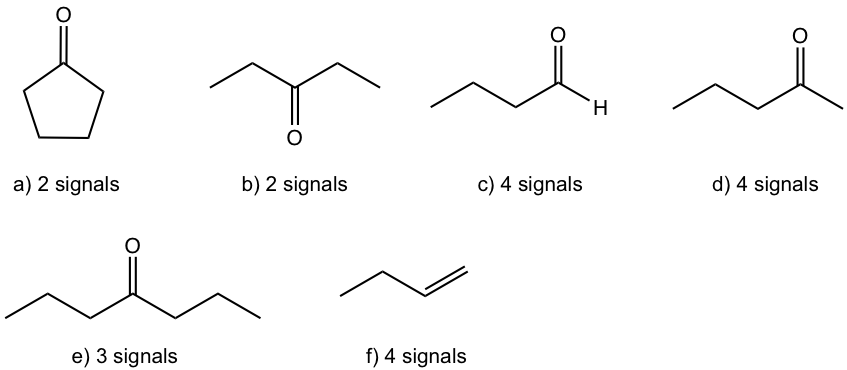
El espectro tiene cuatro señales: triplete (~0.7 ppm), multiplete (~1.4 ppm), singlete (~1.9 ppm) y triplete (~2.2 ppm). Con base en la estructura de cada compuesto, los compuestos c), d) y f) deben tener cuatro señales en el espectro de RMN 1H.
- No hay señales a aproximadamente 9 ppm para los hidrógenos de aldehído en los espectros, por lo que el espectro no es para c ompound c), butaldehído.
- No hay señales a aproximadamente 4~5 ppm para los hidrógenos de alqueno en los espectros, por lo que el espectro no es para c ompound f), 1-buteno.
- Las señales en el espectro coinciden con lo que se espera para el compuesto d), 2-pentanona.
Solución: El espectro es para 2-pentanona.

Determinación de la estructura basada en el espectro de RMN 1H
Para un nivel avanzado de práctica, se supone que debemos ser capaces de determinar la estructura exacta de un compuesto con espectro de RMN 1H dado (y otra información necesaria). Como hemos aprendido, hay mucha información valiosa sobre la estructura de un compuesto que se puede obtener a partir de un espectro de RMN de 1H. Para un resumen, analizar las cuatro características del espectro es crítico para dilucidar la estructura de un compuesto:
- El número de señales indica cuántos conjuntos diferentes de protones hay en la molécula;
- El desplazamiento químico de la señal nos habla del entorno electrónico de cada conjunto de protones;
- La integración bajo cada señal proporciona información sobre cuántos protones hay en el conjunto que se está midiendo (tenga en cuenta que los valores de integración son para la relación, no el número real de protones);
- El patrón de división de cada señal habla sobre el número de protones en los átomos adyacentes a aquel cuya señal se está midiendo.


