1.1: Electricidad estática
- Page ID
- 155381
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
Se descubrió hace siglos que ciertos tipos de materiales se atraerían misteriosamente unos a otros después de ser frotados juntos. Por ejemplo: después de frotar un trozo de seda contra un trozo de vidrio, la seda y el vidrio tenderían a pegarse. En efecto, había una fuerza atractiva que podía demostrarse incluso cuando los dos materiales estaban separados:

El vidrio y la seda no son los únicos materiales que se sabe que se comportan así. Cualquiera que alguna vez se haya rozado contra un globo de látex sólo para descubrir que trata de pegarse a ellos ha experimentado este mismo fenómeno. La cera de parafina y la tela de lana son otro par de materiales que los primeros experimentadores reconocidos por manifestar fuerzas atractivas después de ser frotados juntos:

Este fenómeno se volvió aún más interesante cuando se descubrió que materiales idénticos, después de haber sido frotados con sus respectivos paños, siempre se repelían entre sí:

También se señaló que cuando un trozo de vidrio frotado con seda se exponía a un trozo de cera frotado con lana, los dos materiales se atraerían entre sí:

Además, se encontró que cualquier material que demuestre propiedades de atracción o repulsión después de ser frotado podría ser clasificado en una de dos categorías distintas: atraído al vidrio y repelido por la cera, o repelido por el vidrio y atraído a la cera. Era uno o el otro: no se encontraron materiales que fueran atraídos o repelidos tanto por el vidrio como por la cera, o que reaccionaran a uno sin reaccionar al otro.
Se dirigió más la atención hacia los trozos de tela utilizados para hacer el frotamiento. Se descubrió que después de frotar dos piezas de vidrio con dos piezas de tela de seda, no sólo las piezas de vidrio se repelían entre sí, sino que también lo hicieron los paños. El mismo fenómeno se sostuvo para las piezas de lana utilizadas para frotar la cera:

Ahora bien, esto fue realmente extraño de presenciar. Después de todo, ninguno de estos objetos fue visiblemente alterado por el roce, sin embargo, definitivamente se comportaron de manera diferente que antes de ser frotados. Cualquier cambio que se haya producido para hacer que estos materiales se atraigan o repelan unos a otros era invisible.
Algunos experimentadores especularon que se estaban transfiriendo “fluidos” invisibles de un objeto a otro durante el proceso de frotamiento, y que estos “fluidos” eran capaces de efectuar una fuerza física a lo largo de una distancia. Charles Dufay fue uno de los primeros experimentadores que demostró que definitivamente hubo dos tipos diferentes de cambios forjados al frotar ciertos pares de objetos juntos. El hecho de que hubiera más de un tipo de cambio manifestado en estos materiales fue evidente por el hecho de que se produjeron dos tipos de fuerzas: la atracción y la repulsión. La hipotética transferencia de fluido se conoció como carga.
Un investigador pionero, Benjamin Franklin, llegó a la conclusión de que solo había un fluido intercambiado entre objetos frotados, y que las dos “cargas” diferentes no eran más que un exceso o una deficiencia de ese líquido. Después de experimentar con cera y lana, Franklin sugirió que la lana gruesa eliminara parte de este fluido invisible de la cera lisa, provocando un exceso de líquido en la lana y una deficiencia de líquido en la cera. La disparidad resultante en el contenido de fluido entre la lana y la cera provocaría entonces una fuerza atractiva, ya que el fluido intentaba recuperar su equilibrio anterior entre los dos materiales.
Postular la existencia de un solo “fluido” que se ganó o perdió a través del frotamiento representó mejor el comportamiento observado: que todos estos materiales caían pulcramente en una de dos categorías cuando se frotaban, y lo más importante, que los dos materiales activos frotados uno contra el otro siempre cayeron en categorías opuestas como lo demuestra su invariable atracción entre sí. Es decir, nunca hubo un momento en el que dos materiales frotados uno contra el otro se volvieran ambos positivos o negativos.
Tras la especulación de Franklin de que la lana se frotaba algo de la cera, el tipo de carga que se asociaba con la cera frotada se conoció como “negativa” (porque se suponía que tenía una deficiencia de líquido) mientras que el tipo de carga asociada con la lana de frotamiento se conoció como “positiva” (porque se suponía que tenía un exceso de líquido). ¡Poco sabía que su inocente conjetura causaría mucha confusión a los estudiantes de la electricidad en el futuro!
Las mediciones precisas de la carga eléctrica fueron realizadas por el físico francés Charles Coulomb en la década de 1780 utilizando un dispositivo llamado equilibrio torsional que mide la fuerza generada entre dos objetos cargados eléctricamente. Los resultados del trabajo de Coulomb llevaron al desarrollo de una unidad de carga eléctrica nombrada en su honor, el culomb. Si dos objetos “puntuales” (objetos hipotéticos que no tienen una superficie apreciable) se cargaran por igual a una medida de 1 culombo y se colocan a 1 metro (aproximadamente 1 yarda) de distancia, generarían una fuerza de alrededor de 9 mil millones de newtons (aproximadamente 2 mil millones de libras), ya sea atrayendo o repeliendo dependiendo del tipos de cargos involucrados. Se encontró que la definición operativa de culombo como unidad de carga eléctrica (en términos de fuerza generada entre cargas puntuales) era igual a un exceso o deficiencia de aproximadamente 6,250,000,000,000,000,000 electrones. O, dicho en términos inversos, un electrón tiene una carga de aproximadamente 0.00000000000000000016 culombios. Siendo que un electrón es el portador más pequeño conocido de carga eléctrica, esta última cifra de carga para el electrón se define como la carga elemental.
Se descubrió mucho más tarde que este “fluido” en realidad estaba compuesto por trozos extremadamente pequeños de materia llamados electrones, así llamado en honor a la antigua palabra griega para ámbar: otro material que exhibe propiedades cargadas cuando se frota con tela. Desde entonces, la experimentación ha revelado que todos los objetos están compuestos de “bloques de construcción” extremadamente pequeños conocidos como átomos, y que estos átomos a su vez están compuestos por componentes más pequeños conocidos como partículas. Las tres partículas fundamentales que comprenden la mayoría de los átomos se denominan protones, neutrones y electrones. Mientras que la mayoría de los átomos tienen una combinación de protones, neutrones y electrones, no todos los átomos tienen neutrones; un ejemplo es el isótopo de protio (1H 1) de hidrógeno (Hidrógeno-1) que es la forma más ligera y común de hidrógeno que solo tiene un protón y un electrón. Los átomos son demasiado pequeños para ser vistos, pero si pudiéramos mirar uno, podría parecer algo como esto:
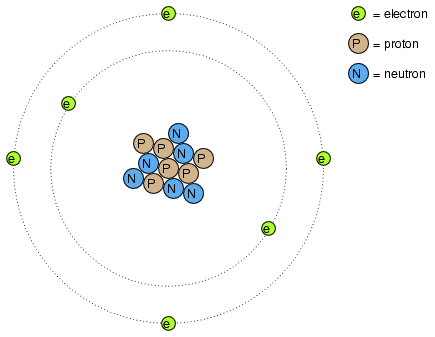
A pesar de que cada átomo en una pieza de material tiende a mantenerse unido como una unidad, en realidad hay mucho espacio vacío entre los electrones y el cúmulo de protones y neutrones que residen en el medio.
Este modelo crudo es el del elemento carbono, con seis protones, seis neutrones y seis electrones. En cualquier átomo, los protones y neutrones están muy unidos entre sí, lo que es una cualidad importante. El grupo fuertemente unido de protones y neutrones en el centro del átomo se llama núcleo, y el número de protones en el núcleo de un átomo determina su identidad elemental: cambiar el número de protones en el núcleo de un átomo, y cambias el tipo de átomo que es. De hecho, si pudieras quitar tres protones del núcleo de un átomo de plomo, ¡habrás logrado el sueño de los viejos alquimistas de producir un átomo de oro! La apretada unión de protones en el núcleo es responsable de la identidad estable de los elementos químicos, y del fracaso de los alquimistas para lograr su sueño.
Los neutrones son mucho menos influyentes en el carácter químico y la identidad de un átomo que los protones, aunque son igual de difíciles de agregar o eliminar del núcleo, estando tan fuertemente unidos. Si se agregan o ganan neutrones, el átomo seguirá conservando la misma identidad química, pero su masa cambiará ligeramente y puede adquirir extrañas propiedades nucleares como la radiactividad.
Sin embargo, los electrones tienen significativamente más libertad para moverse en un átomo que los protones o neutrones. De hecho, pueden ser noqueados de sus respectivas posiciones (¡incluso dejando el átomo por completo!) por mucha menos energía de la que se necesita para desalojar partículas en el núcleo. Si esto sucede, el átomo aún conserva su identidad química, pero se produce un desequilibrio importante. Los electrones y protones son únicos en el hecho de que se sienten atraídos entre sí a lo largo de una distancia. Es esta atracción sobre la distancia la que provoca la atracción entre objetos frotados, donde los electrones se alejan de sus átomos originales para residir alrededor de átomos de otro objeto.
Los electrones tienden a repeler a otros electrones a distancia, al igual que los protones con otros protones. La única razón por la que los protones se unen en el núcleo de un átomo es por una fuerza mucho más fuerte llamada fuerza nuclear fuerte que tiene efecto sólo a distancias muy cortas. Debido a este comportamiento de atracción/repulsión entre partículas individuales, se dice que los electrones y protones tienen cargas eléctricas opuestas. Es decir, cada electrón tiene una carga negativa, y cada protón una carga positiva. En números iguales dentro de un átomo, contrarrestan la presencia del otro para que la carga neta dentro del átomo sea cero. Es por ello que la imagen de un átomo de carbono tenía seis electrones: para equilibrar la carga eléctrica de los seis protones en el núcleo. Si los electrones se van o llegan electrones adicionales, la carga eléctrica neta del átomo se desequilibrará, dejando al átomo “cargado” como un todo, haciendo que interactúe con partículas cargadas y otros átomos cargados cercanos. Los neutrones no son atraídos ni repelidos por electrones, protones, o incluso otros neutrones, y en consecuencia se categorizan como sin carga alguna.
El proceso de los electrones que llegan o salen es exactamente lo que sucede cuando ciertas combinaciones de materiales se frotan entre sí: los electrones de los átomos de un material son forzados por el frotamiento a dejar sus respectivos átomos y transferirse a los átomos del otro material. En otras palabras, los electrones comprenden el “fluido” hipotetizado por Benjamin Franklin.
El resultado de un desequilibrio de este “fluido” (electrones) entre los objetos se llama electricidad estática. Se llama “estática” porque los electrones desplazados tienden a permanecer estacionarios después de ser movidos de un material aislante a otro. En el caso de la cera y la lana, se determinó a través de una mayor experimentación que los electrones en la lana realmente se transferían a los átomos de la cera, ¡lo cual es exactamente opuesto a la conjetura de Franklin! En honor a la designación de Franklin de que la carga de la cera es “negativa” y la carga de la lana es “positiva”, se dice que los electrones tienen una influencia de carga “negativa”. Así, se dice que un objeto cuyos átomos han recibido un excedente de electrones está cargado negativamente, mientras que un objeto cuyos átomos carecen de electrones se dice que está cargado positivamente, por confuso que puedan parecer estas designaciones. Para cuando se descubrió la verdadera naturaleza del “fluido” eléctrico, la nomenclatura de carga eléctrica de Franklin estaba demasiado bien establecida para cambiarla fácilmente, y así permanece hasta el día de hoy.
Michael Faraday demostró (1832) que la electricidad estática era la misma que la producida por una batería o un generador. La electricidad estática es, en su mayor parte, una molestia. El polvo negro y el polvo sin humo tienen grafito agregado para evitar la ignición debido a la electricidad estática. Causa daño a los circuitos semiconductores sensibles. Si bien es posible producir motores alimentados por alta tensión y baja corriente característica de la electricidad estática, esto no es económico. Las pocas aplicaciones prácticas de la electricidad estática incluyen la impresión xerográfica, el filtro de aire electrostático y el generador Van de Graaff de alto voltaje.
Revisar
- Todos los materiales están formados por pequeños “bloques de construcción” conocidos como átomos.
- Todos los átomos naturales contienen partículas llamadas electrones, protones y neutrones, con la excepción del isótopo de protio (1 H 1) de hidrógeno.
- Los electrones tienen una carga eléctrica negativa (-).
- Los protones tienen una carga eléctrica positiva (+).
- Los neutrones no tienen carga eléctrica.
- Los electrones pueden ser desalojados de los átomos mucho más fácilmente que los protones o neutrones.
- El número de protones en el núcleo de un átomo determina su identidad como elemento único.


