11.4: Baterías para fines especiales
- Page ID
- 155294
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
En los primeros días de la tecnología de medición eléctrica, un tipo especial de batería conocida como celda estándar de mercurio se utilizó popularmente como estándar de calibración de voltaje. La salida de una celda de mercurio fue de 1.0183 a 1.0194 voltios de CC (dependiendo del diseño específico de la celda), y fue extremadamente estable en el tiempo. La deriva anunciada fue de alrededor de 0.004 por ciento del voltaje nominal por año. Las células estándar de mercurio a veces se conocían como células Weston o células de cadmio.
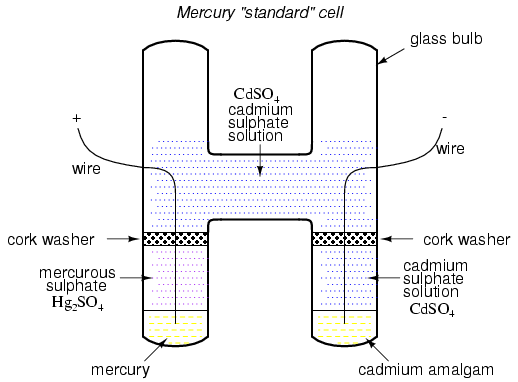
Desafortunadamente, las celdas de mercurio eran bastante intolerantes a cualquier drenaje de corriente y ni siquiera podían medirse con un voltímetro analógico sin comprometer la precisión. Los fabricantes normalmente pedían no más de 0.1 mA de corriente a través de la celda, ¡e incluso esa cifra se consideró momentánea, o máxima de sobretensión! En consecuencia, las celdas estándar solo se pudieron medir con un dispositivo potenciométrico (balance nulo) donde el drenaje de corriente es casi cero. Se prohibió el cortocircuito de una celda de mercurio, y una vez que se cortocircuitó, nunca más se pudo confiar en la celda como un dispositivo estándar.
Las celdas estándar de mercurio también fueron susceptibles a ligeros cambios en el voltaje si se alteraban física o térmicamente. Se desarrollaron dos tipos diferentes de celdas estándar de mercurio para diferentes propósitos de calibración: saturadas e insaturadas. Las celdas estándar saturadas proporcionaron la mayor estabilidad de voltaje a lo largo del tiempo, a expensas de la inestabilidad térmica. En otras palabras, su voltaje derivó muy poco con el paso del tiempo (¡solo unos microvoltios en el lapso de una década!) , pero tendían a variar con los cambios de temperatura (decenas de microvoltios por grado Celsius). Estas células funcionaron mejor en entornos de laboratorio con temperatura controlada donde la estabilidad a largo plazo es primordial. Las celdas insaturadas proporcionaron estabilidad térmica a expensas de la estabilidad a lo largo del tiempo, permaneciendo el voltaje prácticamente constante con cambios de temperatura pero disminuyendo constantemente en aproximadamente 100 µV cada año. Estas celdas funcionaron mejor como dispositivos de calibración de “campo” donde la temperatura ambiente no se controla con precisión. El voltaje nominal para una celda saturada fue de 1.0186 voltios y 1.019 voltios para una celda insaturada.
Las referencias modernas de voltaje semiconductor (regulador de diodo zener) han remplazado a las baterías de celda estándar como estándares de voltaje de laboratorio y de campo.
Un dispositivo fascinante estrechamente relacionado con las baterías de celda primaria es la pila de combustible, llamada porque aprovecha la reacción química de la combustión para generar una corriente eléctrica. El proceso de oxidación química (unión de oxígeno iónicamente con otros elementos) es capaz de producir un flujo de electrones entre dos electrodos así como cualquier combinación de metales y electrolitos. Una pila de combustible se puede considerar como una batería con una fuente de energía química suministrada externamente.
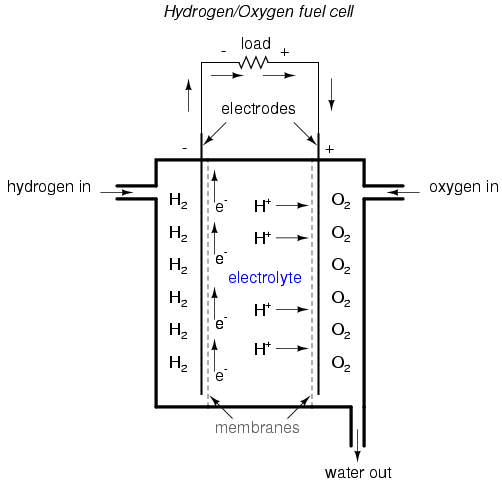
Hasta la fecha, las pilas de combustible construidas con mayor éxito son las que funcionan con hidrógeno y oxígeno, aunque se han realizado muchas investigaciones sobre celdas que utilizan combustibles hidrocarbonados. Si bien “quema” hidrógeno, los únicos subproductos de desecho de una pila de combustible son el agua y una pequeña cantidad de calor. Cuando se opera con combustibles que contienen carbono, el dióxido de carbono también se libera como subproducto. Debido a que la temperatura de funcionamiento de las pilas de combustible modernas está muy por debajo de la de la combustión normal, no se forman óxidos de nitrógeno (NO x), haciéndola mucho menos contaminante, siendo iguales todos los demás factores.
La eficiencia de la conversión de energía en una pila de combustible de química a eléctrica supera con creces el límite teórico de eficiencia Carnot de cualquier motor de combustión interna, lo que es una perspectiva emocionante para la generación de energía y los automóviles eléctricos híbridos.
Otro tipo de “batería” es la célula solar, un subproducto de la revolución de los semiconductores en la electrónica. El efecto fotoeléctrico, mediante el cual los electrones se desalojan de los átomos bajo la influencia de la luz, se conoce en la física desde hace muchas décadas, pero sólo ha sido con los recientes avances en la tecnología de semiconductores que existía un dispositivo capaz de aprovechar este efecto en cualquier grado práctico. Las eficiencias de conversión para las células solares de silicio siguen siendo bastante bajas, pero sus beneficios como fuentes de energía son legión: sin partes móviles, sin ruido, sin productos de desecho o contaminación (aparte de la fabricación de células solares, que sigue siendo una industria bastante “sucia”), y vida indefinida.

El costo específico de la tecnología de células solares (dólares por kilovatio) sigue siendo muy alto, con pocas perspectivas de disminución significativa salvo algún tipo de avance revolucionario en la tecnología. A diferencia de los componentes electrónicos hechos de material semiconductor, que se pueden hacer cada vez más pequeños con menos desechos como resultado de un mejor control de calidad, una sola célula solar todavía toma la misma cantidad de silicio ultra puro para fabricar que hace treinta años. El control de calidad superior no logra producir la misma ganancia de producción observada en la fabricación de chips y transistores (donde las motas aisladas de impurezas pueden arruinar muchos circuitos microscópicos en una oblea de silicio). El mismo número de inclusiones impuras hace poco para impactar la eficiencia general de una célula solar de 3 pulgadas.
Otro tipo de “batería” de propósito especial es la celda de detección química. En pocas palabras, estas celdas reaccionan químicamente con sustancias específicas en el aire para crear un voltaje directamente proporcional a la concentración de esa sustancia. Una aplicación común para una célula de detección química es en la detección y medición de la concentración de oxígeno. Muchos analizadores de oxígeno portátiles se han diseñado alrededor de estas pequeñas celdas. La química celular debe diseñarse para que coincida con la sustancia o sustancias específicas que se van a detectar, y las células tienden a “desgastarse”, ya que los materiales de sus electrodos se agotan o se contaminan con el uso.
Revisar
- Las celdas estándar de mercurio son tipos especiales de baterías que alguna vez se usaron como estándares de calibración de voltaje antes de la llegada de los dispositivos de referencia de semiconductores de precisión
- Una pila de combustible es un tipo de batería que utiliza un combustible y un oxidante como reactivos para generar electricidad. Son fuentes prometedoras de energía eléctrica en el futuro, “quemando” combustibles con muy bajas emisiones.
- Una célula solar utiliza energía de luz ambiental para motivar electrones de un electrodo a otro, produciendo voltaje (y corriente, proporcionando un circuito externo).
- Una celda de detección química es un tipo especial de celda voltaica que produce voltaje proporcional a la concentración de una sustancia aplicada (generalmente un gas específico en el aire ambiente).


