12.7: Leucemia Mieloide Crónica (LMC)
- Page ID
- 56630
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
La leucemia es una proliferación incontrolada de un tipo de glóbulos blancos (o leucocitos). Como todos los cánceres (probablemente), todas las células leucémicas descienden de una sola célula que perdió la capacidad de mantener un control normal sobre el ciclo celular. Hay una serie de tipos de leucemia, como cabría esperar de la cantidad de tipos de glóbulos blancos (5) y el número de estadios por los que pasan a medida que maduran. Una de las más comunes es la c hrónica m yelógena l euquemia o LMC.
La Leucemia Mieloide Crónica (LMC) surge en una célula madre de médula ósea que es la precursora de todos los tipos de células sanguíneas. Sin embargo, suele afectar al llamado linaje mieloide (de ahí el nombre) que produce granulocitos y macrófagos. Como su nombre indica, la enfermedad a menudo existe desde hace años con solo números moderadamente elevados de células leucémicas (descendientes de las células madre) y pocos síntomas. En algún momento, sin embargo, el paciente atraviesa una “crisis blástica” cuando los progenitores leucémicos de granulocitos-macrófagos comienzan a dividirse por sí mismos, incrementando su número enormemente al tiempo que no logran continuar su diferenciación.
El cromosoma Filadelfia (Ph 1)
En la mayoría de los casos de LMC, las células leucémicas comparten una anomalía cromosómica que no se encuentra en ningún glóbulo blanco no leucémico, ni en ninguna otra célula del cuerpo del paciente. Esta anomalía es una translocación recíproca entre un cromosoma 9 y un cromosoma 22. Esta translocación se designa t (9; 22). Da como resultado un cromosoma 9 más largo de lo normal y un cromosoma 22 más corto de lo normal. Este último se llama cromosoma Filadelfia y se designa\(Ph^1\).
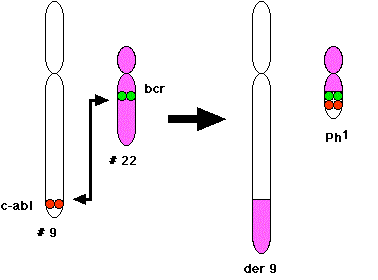
El ADN extraído del cromosoma 9 contiene la mayor parte del protooncogén denominado c-Abl. La ruptura en el cromosoma 22 ocurre en medio de un gen denominado BCR. El cromosoma Filadelfia resultante tiene la sección 5' de BCR fusionada con la mayoría de c-Abl.
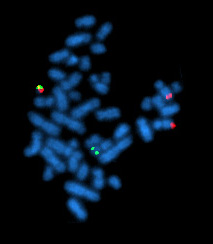
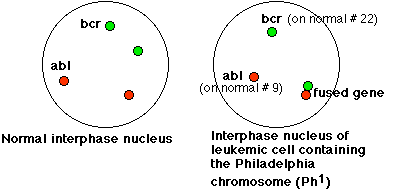
La micrografía de la Figura\(\PageIndex{2}\) utiliza f luorescencia i n s itu h ybridization (FISH) para revelar el ADN ABL (rojo) y el ADN BCR (verde) en los núcleos interfase de las células leucémicas de un paciente con LMC. El punto rojo en el centro izquierdo revela la ubicación de ABL en el cromosoma 9 normal; el punto verde (centro superior) muestra BCR en el cromosoma 22 normal. Los puntos combinados (rojo + verde = amarillo) en la parte inferior derecha revelan el gen BCR-ABL fusionado en el cromosoma Filadelfia. La Figura 12.7.3 es un esquema que puede ayudarle a interpretar la micrografía.
La transcripción y traducción del gen híbrido BCR-ABL produce una proteína anormal (“fusión”) que activa constitutivamente (todo el tiempo) una serie de actividades celulares que normalmente se activan solo cuando la célula es estimulada por un factor de crecimiento, como el factor de crecimiento derivado de plaquetas ( PDGF).
Esta activación desenfrenada aumenta la tasa de mitosis y protege a la célula de la apoptosis. El resultado es un incremento en el número de células que contienen Ph 1. Durante la fase crónica de la enfermedad, éstas aún pueden salir del ciclo celular y diferenciarse en células maduras que realizan sus funciones normales. En algún momento, sin embargo, otra mutación en un protooncogén (RAS, por ejemplo) o en un gen supresor de tumores (p53, por ejemplo), ocurrirá en una de estas células. La mutación adicional hace que la tasa de mitosis en esa célula y sus descendientes aumente bruscamente. Las células hijas no logran diferenciarse y el paciente entra en la fase de crisis de la enfermedad.
Hasta hace poco, el único tratamiento exitoso de la LMC era destruir la médula ósea del paciente y luego restaurar la producción de células sanguíneas infundiendo células madre de la médula ósea de un donante sano. Pero ahora el tratamiento con el medicamento mesilato de imatinib (Gleevec® también conocido STI571) parece ser capaz de curar la enfermedad. Esta molécula encaja en el sitio activo de la proteína ABL evitando que el ATP se una allí. Sin ATP como donante de fosfato, la proteína ABL no puede fosforilar su (s) sustrato (s). Un estudio de fase 2, encontró que casi el 90% de los pacientes con LMC tratados con el medicamento no mostraron mayor progresión de su enfermedad.
Gleevec también se muestra prometedor contra un tipo de cáncer de estómago (tumores estromales gastrointestinales = GIST), que es una producción excesiva de eosinófilos potencialmente mortal. En esta enfermedad, Gleevec inhibe una tirosina quinasa hiperactiva diferente. Este también es el resultado de la fusión de partes de dos genes diferentes (debido a la deleción del ADN entre ellos):
- los primeros 233 codones de un gen designado FIP1L1 fusionados a
- los 523 codones finales del gen (PDGFRα) que codifica el dominio tirosina quinasa de un receptor para el factor de crecimiento derivado de plaquetas. La proteína de fusión producida, como BCR-ABL, es hiperactiva.


