35.2: Cómo se comunican las neuronas
- Page ID
- 59629
Habilidades para Desarrollar
- Describir la base del potencial de membrana en reposo
- Explicar las etapas de un potencial de acción y cómo se propagan los potenciales de acción
- Explicar las similitudes y diferencias entre sinapsis químicas y eléctricas
- Describir la potenciación a largo plazo y la depresión
Todas las funciones que realiza el sistema nervioso, desde un simple reflejo motor hasta funciones más avanzadas como hacer una memoria o una decisión, requieren que las neuronas se comuniquen entre sí. Mientras que los humanos usan palabras y lenguaje corporal para comunicarse, las neuronas usan señales eléctricas y químicas. Al igual que una persona en un comité, una neurona suele recibir y sintetizar mensajes de otras múltiples neuronas antes de “tomar la decisión” de enviar el mensaje a otras neuronas.
Transmisión del impulso nervioso dentro de una neurona
Para que el sistema nervioso funcione, las neuronas deben poder enviar y recibir señales. Estas señales son posibles porque cada neurona tiene una membrana celular cargada (una diferencia de voltaje entre el interior y el exterior), y la carga de esta membrana puede cambiar en respuesta a moléculas neurotransmisoras liberadas de otras neuronas y estímulos ambientales. Para entender cómo se comunican las neuronas, primero hay que entender la base de la carga de membrana basal o 'en reposo'.
Membranas Neuronales
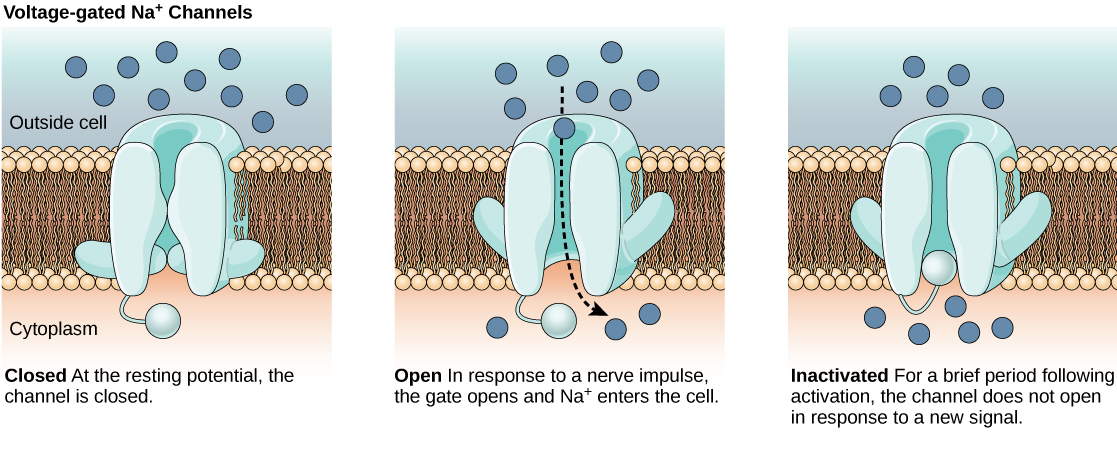
La membrana bicapa lipídica que rodea a una neurona es impermeable a moléculas o iones cargados. Para entrar o salir de la neurona, los iones deben pasar a través de proteínas especiales llamadas canales iónicos que abarcan la membrana. Los canales iónicos tienen diferentes configuraciones: abierto, cerrado e inactivo, como se ilustra en la Figura\(\PageIndex{1}\). Algunos canales iónicos necesitan ser activados para abrirse y permitir que los iones pasen dentro o fuera de la célula. Estos canales iónicos son sensibles al medio ambiente y pueden cambiar su forma en consecuencia. Los canales iónicos que cambian su estructura en respuesta a los cambios de voltaje se denominan canales iónicos regulados por voltaje. Los canales iónicos regulados por voltaje regulan las concentraciones relativas de diferentes iones dentro y fuera de la célula. La diferencia en la carga total entre el interior y el exterior de la célula se denomina potencial de membrana.
Enlace al aprendizaje
Este video analiza la base del potencial de la membrana en reposo.
Potencial de membrana en reposo
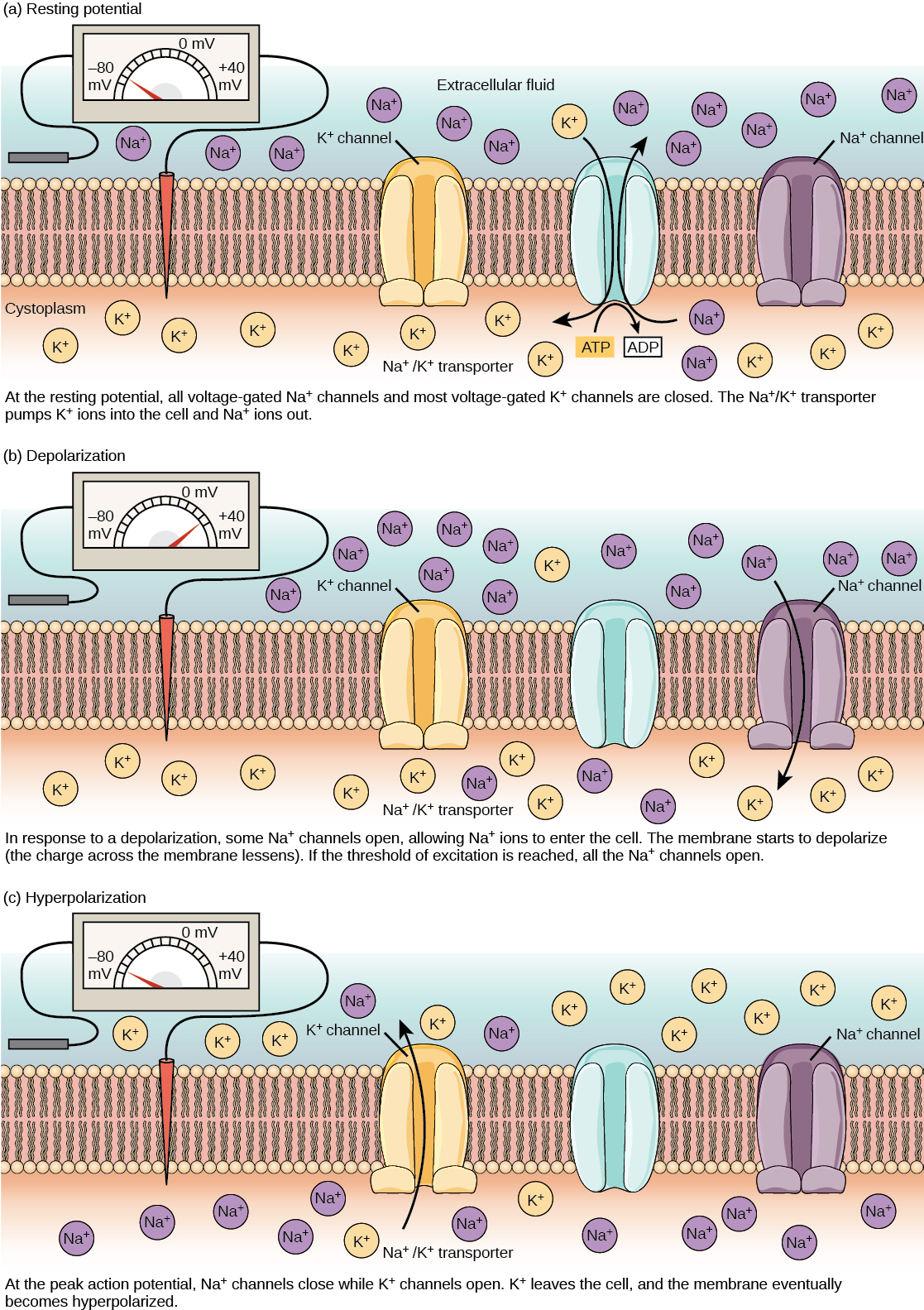
Una neurona en reposo está cargada negativamente: el interior de una célula es aproximadamente 70 milivoltios más negativo que el exterior (−70 mV, tenga en cuenta que este número varía según el tipo de neurona y por especie). Este voltaje se denomina potencial de membrana en reposo; es causado por diferencias en las concentraciones de iones dentro y fuera de la célula. Si la membrana fuera igualmente permeable a todos los iones, cada tipo de ion fluiría a través de la membrana y el sistema alcanzaría el equilibrio. Debido a que los iones no pueden simplemente cruzar la membrana a voluntad, existen diferentes concentraciones de varios iones dentro y fuera de la célula, como se muestra en la siguiente tabla. La diferencia en el número de iones de potasio cargados positivamente (K +) dentro y fuera de la célula domina el potencial de membrana en reposo (Figura\(\PageIndex{2}\)). Cuando la membrana está en reposo, los iones K + se acumulan dentro de la célula debido a un movimiento neto con el gradiente de concentración. El potencial negativo de la membrana en reposo se crea y mantiene aumentando la concentración de cationes fuera de la célula (en el fluido extracelular) en relación con el interior de la célula (en el citoplasma). La carga negativa dentro de la célula es creada por la membrana celular siendo más permeable al movimiento de iones potasio que al movimiento de iones sodio. En las neuronas, los iones potasio se mantienen a altas concentraciones dentro de la célula mientras que los iones de sodio se mantienen a altas concentraciones fuera de la célula. La célula posee canales de fuga de potasio y sodio que permiten que los dos cationes se difundan por su gradiente de concentración. Sin embargo, las neuronas tienen muchos más canales de fuga de potasio que los canales de fuga de sodio. Por lo tanto, el potasio se difunde fuera de la celda a un ritmo mucho más rápido que el sodio se filtra. Debido a que más cationes están saliendo de la celda de los que están entrando, esto hace que el interior de la celda se cargue negativamente en relación con el exterior de la celda. Las acciones de la bomba de sodio y potasio ayudan a mantener el potencial de reposo, una vez establecido. Recordemos que las bombas de sodio y potasio traen dos iones K + a la célula mientras eliminan tres iones Na + por ATP consumido. A medida que se expulsan más cationes de la célula que los absorbidos, el interior de la célula permanece cargado negativamente en relación con el líquido extracelular. Cabe señalar que los iones calcio (Cl —) tienden a acumularse fuera de la célula porque son repelidos por proteínas cargadas negativamente dentro del citoplasma.
| Ion | Concentración extracelular (mM) | Concentración intracelular (mM) | Relación exterior/interior |
|---|---|---|---|
| Na + | 145 | 12 | 12 |
| K + | 4 | 155 | 0.026 |
| Cl − | 120 | 4 | 30 |
| Aniones orgánicos (A−) | — | 100 |
Potencial de acción
Una neurona puede recibir entrada de otras neuronas y, si esta entrada es lo suficientemente fuerte, enviar la señal a las neuronas aguas abajo. La transmisión de una señal entre neuronas generalmente es transportada por una sustancia química llamada neurotransmisor. La transmisión de una señal dentro de una neurona (de dendrita a axón terminal) es transportada por una breve inversión del potencial de membrana en reposo llamado potencial de acción. Cuando las moléculas de neurotransmisores se unen a receptores localizados en las dendritas de una neurona, los canales iónicos se abren. En las sinapsis excitatorias, esta apertura permite que los iones positivos ingresen a la neurona y da como resultado la despolarización de la membrana, una disminución en la diferencia de voltaje entre el interior y el exterior de la neurona. Un estímulo de una célula sensorial u otra neurona despolariza la neurona diana a su potencial umbral (-55 mV). Los canales de Na + en el montículo del axón se abren, permitiendo que los iones positivos ingresen a la célula (Figura\(\PageIndex{3}\) y Figura\(\PageIndex{4}\)). Una vez que los canales de sodio se abren, la neurona se despolariza completamente a un potencial de membrana de aproximadamente +40 mV. Los potenciales de acción se consideran un evento de “todo o nada”, en el sentido de que, una vez que se alcanza el potencial umbral, la neurona siempre se despolariza por completo. Una vez que se completa la despolarización, la célula ahora debe “restablecer” su voltaje de membrana de nuevo al potencial de reposo. Para lograrlo, los canales Na + cierran y no se pueden abrir. Esto inicia el periodo refractario de la neurona, en el que no puede producir otro potencial de acción porque sus canales de sodio no se abrirán. Al mismo tiempo, los canales K + regulados por voltaje se abren, permitiendo que K + salga de la celda. A medida que los iones K + salen de la célula, el potencial de membrana vuelve a ser negativo. La difusión de K + fuera de la célula en realidad hiperpolariza la célula, ya que el potencial de membrana se vuelve más negativo que el potencial de reposo normal de la célula. En este punto, los canales de sodio volverán a su estado de reposo, lo que significa que están listos para abrirse nuevamente si el potencial de membrana vuelve a superar el potencial umbral. Finalmente, los iones K + adicionales se difunden fuera de la célula a través de los canales de fuga de potasio, llevando a la célula de su estado hiperpolarizado, de nuevo a su potencial de membrana en reposo.
Conexión de arte
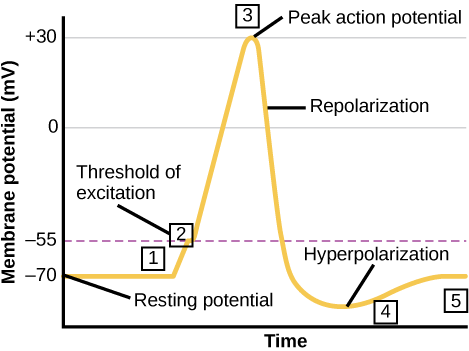
Los bloqueadores de los canales de potasio, como la amiodarona y la procainamida, que se utilizan para tratar la actividad eléctrica anormal en el corazón, llamada disritmia cardíaca, impiden el movimiento de K + a través de canales K + regulados por voltaje. ¿Qué parte del potencial de acción esperarías que afectaran los canales de potasio?
Enlace al aprendizaje
Este video presenta una visión general del potencial de acción.
La mielina y la propagación del potencial de acción
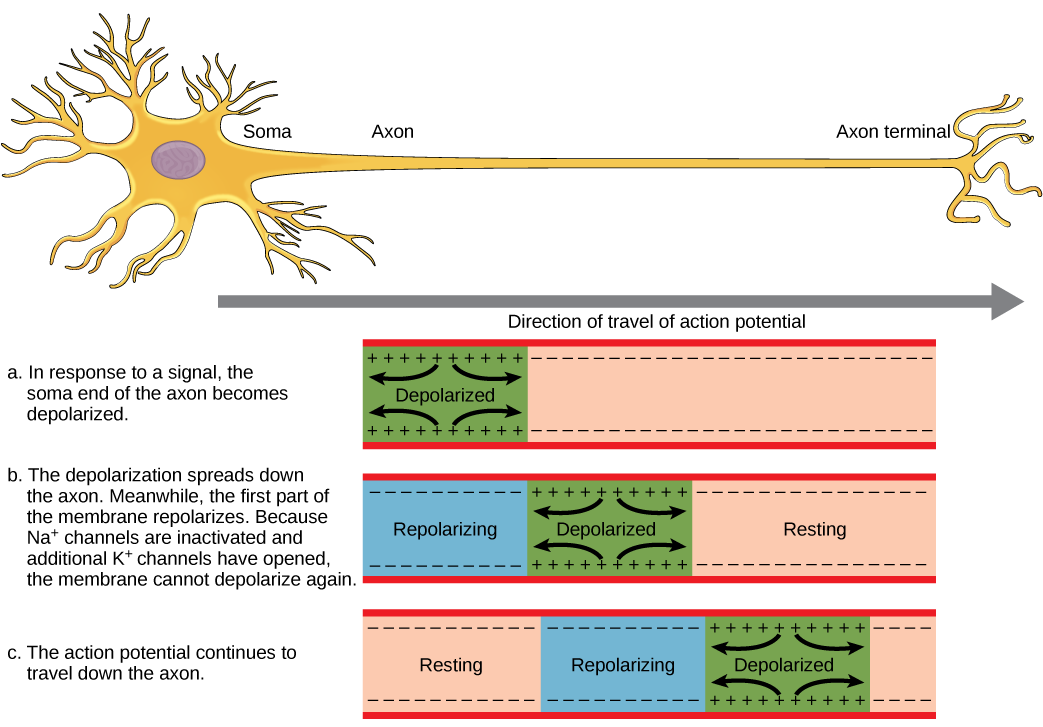
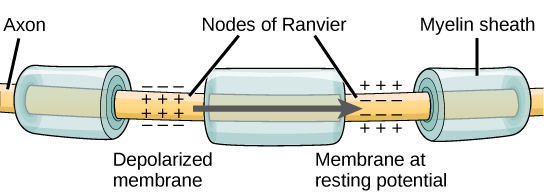
Para que un potencial de acción comunique información a otra neurona, debe viajar a lo largo del axón y llegar a las terminales del axón donde puede iniciar la liberación de neurotransmisores. La velocidad de conducción de un potencial de acción a lo largo de un axón está influenciada tanto por el diámetro del axón como por la resistencia del axón a la fuga de corriente. La mielina actúa como aislante que impide que la corriente salga del axón; esto aumenta la velocidad de conducción del potencial de acción. En enfermedades desmielinizantes como la esclerosis múltiple, la conducción del potencial de acción se ralentiza debido a que la corriente se filtra desde áreas axónicas previamente aisladas. Los nodos de Ranvier, ilustrados en la Figura,\(\PageIndex{5}\) son huecos en la vaina de mielina a lo largo del axón. Estos espacios no mielinizados tienen aproximadamente un micrómetro de largo y contienen canales Na + y K + con voltaje cerrado. El flujo de iones a través de estos canales, particularmente los canales de Na +, regenera el potencial de acción una y otra vez a lo largo del axón. Este 'salto' del potencial de acción de un nodo al siguiente se llama conducción saltatoria. Si los nodos de Ranvier no estuvieran presentes a lo largo de un axón, el potencial de acción se propagaría muy lentamente ya que los canales Na + y K + tendrían que regenerar continuamente los potenciales de acción en cada punto a lo largo del axón en lugar de en puntos específicos. Los nodos de Ranvier también ahorran energía para la neurona ya que los canales solo necesitan estar presentes en los nodos y no a lo largo de todo el axón.
Transmisión sináptica
La sinapsis o “gap” es el lugar donde la información se transmite de una neurona a otra. Las sinapsis suelen formarse entre los terminales axones y las espinas dendríticas, pero esto no es universalmente cierto. También hay sinapsis de axón a axón, dendríta a dendrita y axón a célula. La neurona que transmite la señal se llama neurona presináptica, y la neurona que recibe la señal se llama neurona postsináptica. Tenga en cuenta que estas designaciones son relativas a una sinapsa particular, la mayoría de las neuronas son tanto presinápticas como postsinápticas. Hay dos tipos de sinapsis: química y eléctrica.
Sinapsis Química
Cuando un potencial de acción alcanza el terminal del axón, despolariza la membrana y abre canales Na + regulados por voltaje. Los iones Na + ingresan a la célula, despolarizando aún más la membrana presináptica. Esta despolarización hace que se abran canales de Ca 2+ regulados por voltaje. Los iones de calcio que ingresan a la célula inician una cascada de señalización que hace que pequeñas vesículas unidas a la membrana, llamadas vesículas sinápticas, que contienen moléculas neurotransmisoras se fusionen con la membrana presináptica. Las vesículas sinápticas se muestran en la Figura\(\PageIndex{6}\), la cual es una imagen de un microscopio electrónico de barrido.
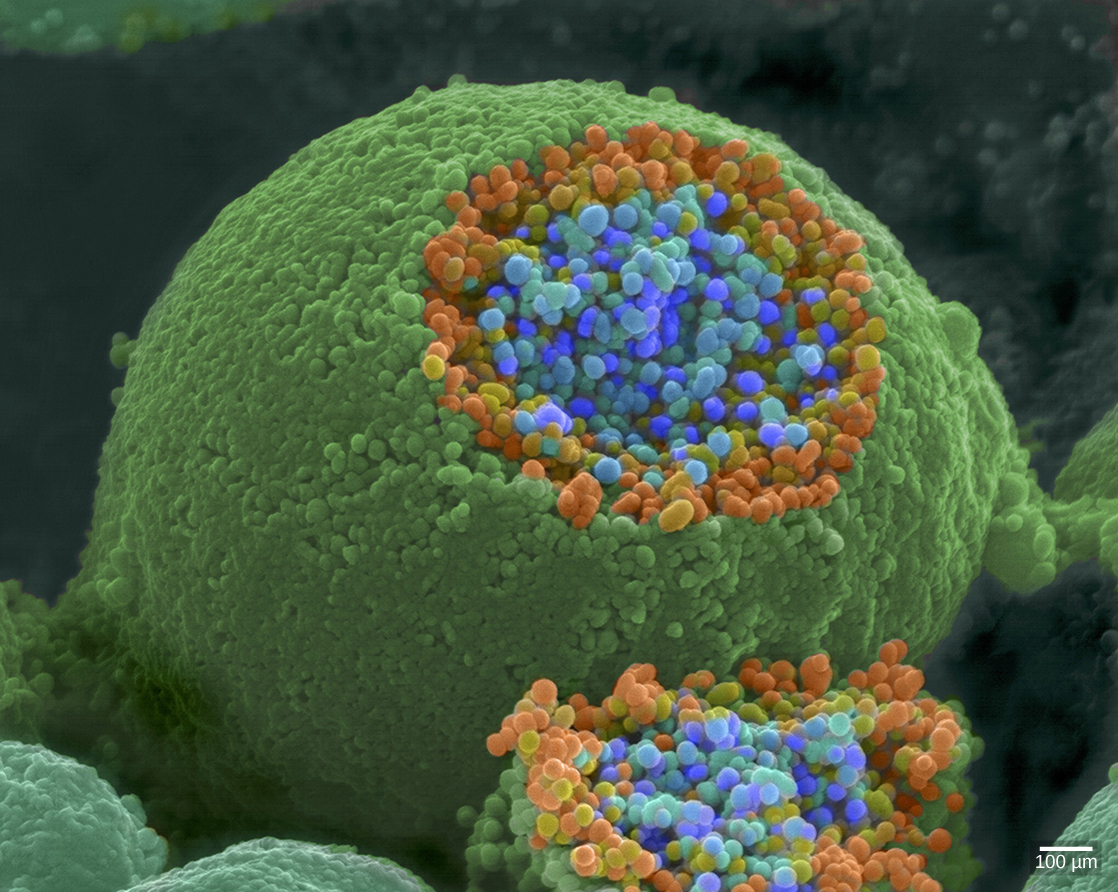
La fusión de una vesícula con la membrana presináptica provoca la liberación del neurotransmisor en la hendidura sináptica, el espacio extracelular entre las membranas presináptica y postsináptica, como se ilustra en la Figura\(\PageIndex{7}\). El neurotransmisor se difunde a través de la hendidura sináptica y se une a las proteínas receptoras en la membrana postsináptica.
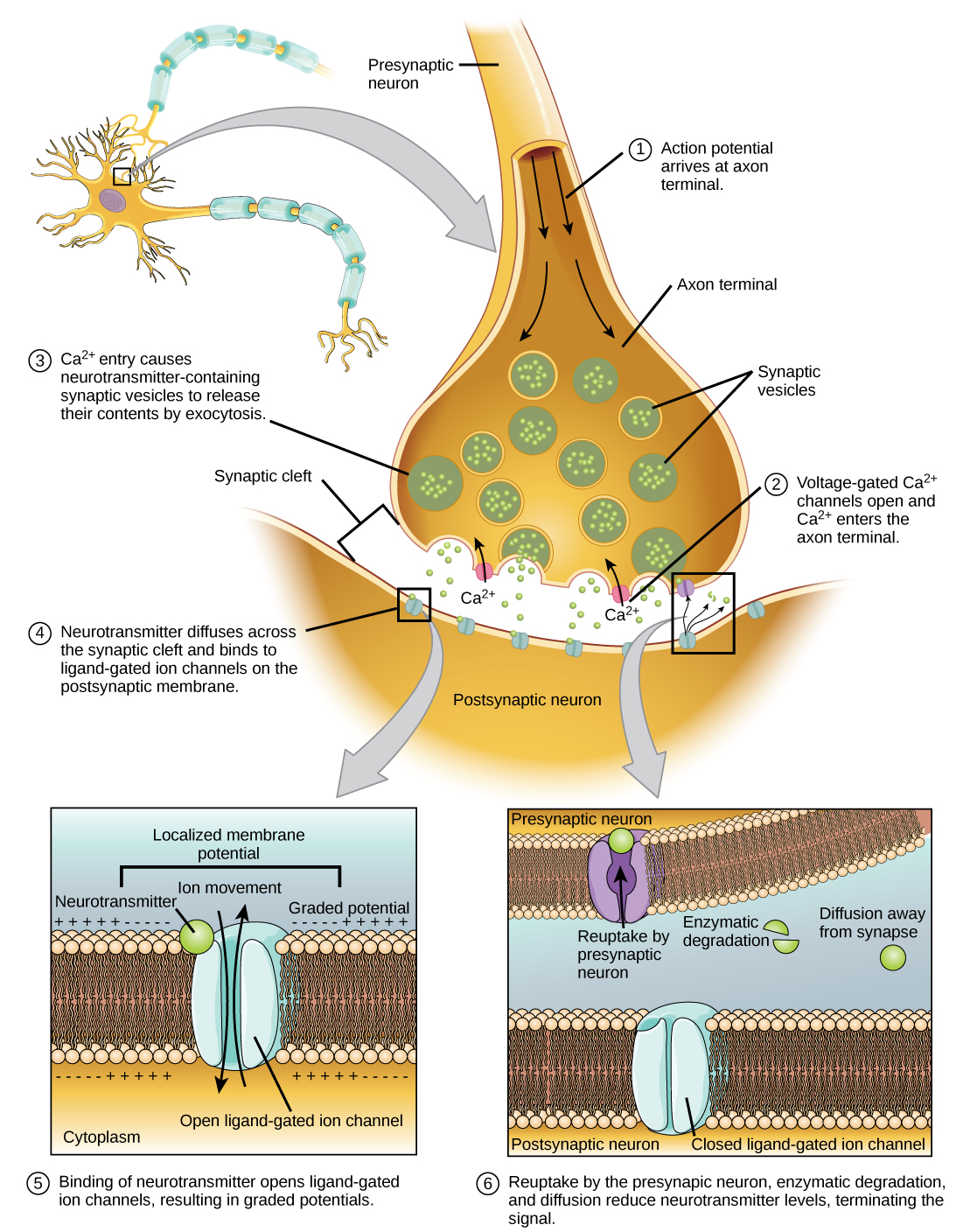
La unión de un neurotransmisor específico hace que se abran canales iónicos particulares, en este caso canales regulados por ligando, en la membrana postsináptica. Los neurotransmisores pueden tener efectos excitadores o inhibitorios sobre la membrana postsináptica, como se detalla en la siguiente tabla. Por ejemplo, cuando la acetilcolina es liberada en la sinapsis entre un nervio y un músculo (llamada unión neuromuscular) por una neurona presináptica, provoca que se abran canales Na + postsinápticos. Na + ingresa a la célula postsináptica y hace que la membrana postsináptica se despolarice. Esta despolarización se denomina potencial postsináptico excitatorio (EPSP) y hace que la neurona postsináptica sea más propensa a disparar un potencial de acción. La liberación de neurotransmisores en las sinapsis inhibitorias provoca potenciales postsinápticos inhibitorios (IPSP), una hiperpolarización de la membrana presináptica. Por ejemplo, cuando el neurotransmisor GABA (ácido gamma-aminobutírico) se libera de una neurona presináptica, se une y abre los canales Cl -. Cl - los iones ingresan a la célula e hiperpolarizan la membrana, lo que hace que la neurona sea menos propensa a disparar un potencial de acción.
Una vez que se ha producido la neurotransmisión, el neurotransmisor debe ser retirado de la hendidura sináptica para que la membrana postsináptica pueda “reiniciarse” y estar lista para recibir otra señal. Esto se puede lograr de tres maneras: el neurotransmisor puede difundirse lejos de la hendidura sináptica, puede ser degradado por enzimas en la hendidura sináptica, o puede ser reciclado (a veces llamado recaptación) por la neurona presináptica. Varios fármacos actúan en este paso de la neurotransmisión. Por ejemplo, algunos medicamentos que se administran a los pacientes de Alzheimer funcionan inhibiendo la acetilcolinesterasa, la enzima que degrada la acetilcolina. Esta inhibición de la enzima aumenta esencialmente la neurotransmisión en las sinapsis que liberan acetilcolina. Una vez liberada, la acetilcolina permanece en la hendidura y puede unirse y desunirse continuamente a los receptores postsinápticos.
| Neurotransmisor | Ejemplo | Ubicación |
|---|---|---|
| Acetilcolina | — | SNC y/o PNS |
| Amina biogénica | Dopamina, serotonina, norepinefrina | SNC y/o PNS |
| Aminoácido | Glicina, glutamato, aspartato, ácido gamma aminobutírico | CNS |
| Neuropéptido | Sustancia P, endorfinas | SNC y/o PNS |
Sinapsis eléctrica
Si bien las sinapsis eléctricas son menos en número que las sinapsis químicas, se encuentran en todos los sistemas nerviosos y desempeñan papeles importantes y únicos. El modo de neurotransmisión en las sinapsis eléctricas es bastante diferente al de las sinapsis químicas. En una sinapsis eléctrica, las membranas presináptica y postsináptica están muy juntas y en realidad están conectadas físicamente por proteínas de canal que forman uniones gap. Los cruces huecos permiten que la corriente pase directamente de una celda a la siguiente. Además de los iones que transportan esta corriente, otras moléculas, como el ATP, pueden difundirse a través de los poros de unión de grandes huecos.
Existen diferencias clave entre sinapsis químicas y eléctricas. Debido a que las sinapsis químicas dependen de la liberación de moléculas neurotransmisoras de las vesículas sinápticas para transmitir su señal, hay un retraso de aproximadamente un milisegundo entre cuando el potencial axónico alcanza el terminal presináptico y cuando el neurotransmisor conduce a la apertura de canales iónicos postsinápticos . Adicionalmente, esta señalización es unidireccional. La señalización en las sinapsis eléctricas, por el contrario, es prácticamente instantánea (lo cual es importante para las sinapsis involucradas en reflejos clave), y algunas sinapsis eléctricas son bidireccionales. Las sinapsis eléctricas también son más confiables ya que tienen menos probabilidades de ser bloqueadas, y son importantes para sincronizar la actividad eléctrica de un grupo de neuronas. Por ejemplo, se cree que las sinapsis eléctricas en el tálamo regulan el sueño de onda lenta, y la interrupción de estas sinapsis puede causar convulsiones.
Suma de señal
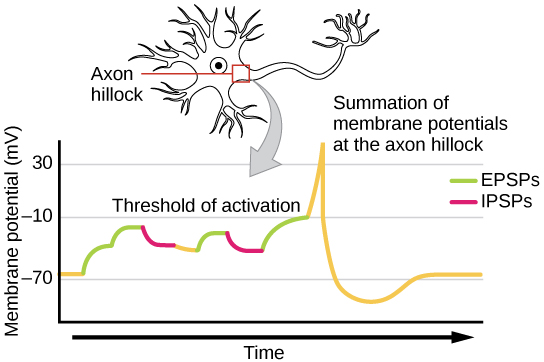
A veces, una sola EPSP es lo suficientemente fuerte como para inducir un potencial de acción en la neurona postsináptica, pero a menudo múltiples entradas presinápticas deben crear EPSP aproximadamente al mismo tiempo para que la neurona postsináptica sea suficientemente despolarizada para disparar un potencial de acción. Este proceso se denomina suma y ocurre en el montículo del axón, como se ilustra en la Figura\(\PageIndex{8}\). Además, una neurona a menudo tiene entradas de muchas neuronas presinápticas, algunas excitadoras y otras inhibidoras, por lo que los IPSP pueden cancelar los EPSP y viceversa. Es el cambio neto en el voltaje de la membrana postsináptica lo que determina si la célula postsináptica ha alcanzado su umbral de excitación necesario para disparar un potencial de acción. En conjunto, la suma sináptica y el umbral de excitación actúan como un filtro para que el “ruido” aleatorio en el sistema no se transmita como información importante.
Conexión diaria: interfaz cerebro-computadora
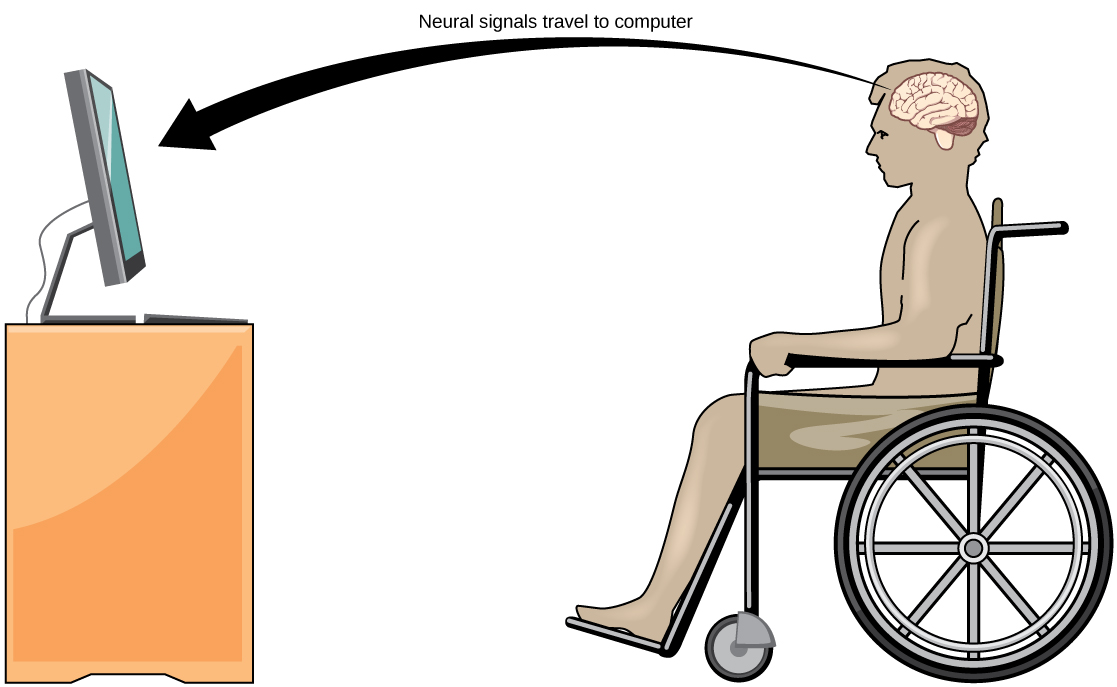
La esclerosis lateral amiotrófica (ELA, también llamada Enfermedad de Lou Gehrig) es una enfermedad neurológica caracterizada por la degeneración de las neuronas motoras que controlan los movimientos voluntarios. La enfermedad comienza con el debilitamiento muscular y la falta de coordinación y finalmente destruye las neuronas que controlan el habla, la respiración y la deglución; al final, la enfermedad puede llevar a la parálisis. En ese punto, los pacientes requieren asistencia de las máquinas para poder respirar y comunicarse. Se han desarrollado varias tecnologías especiales para permitir que los pacientes “encerrados” se comuniquen con el resto del mundo. Una tecnología, por ejemplo, permite a los pacientes escribir oraciones al sacudir la mejilla. Estas frases pueden entonces ser leídas en voz alta por una computadora.
Una línea de investigación relativamente nueva para ayudar a los pacientes paralizados, incluyendo aquellos con ELA, a comunicarse y retener un grado de autosuficiencia se llama tecnología de interfaz cerebro-computadora (BCI) y se ilustra en la Figura\(\PageIndex{9}\). Esta tecnología suena como algo sacado de la ciencia ficción: permite a los pacientes paralizados controlar una computadora usando solo sus pensamientos. Existen varias formas de BCI. Algunas formas utilizan grabaciones EEG de electrodos pegados en el cráneo. Estas grabaciones contienen información de grandes poblaciones de neuronas que pueden ser decodificadas por una computadora. Otras formas de BCI requieren la implantación de una matriz de electrodos más pequeños que un sello postal en el área del brazo y la mano de la corteza motora. Esta forma de BCI, aunque más invasiva, es muy poderosa ya que cada electrodo puede registrar potenciales de acción reales de una o más neuronas. Estas señales se envían luego a una computadora, la cual ha sido entrenada para decodificar la señal y alimentarla a una herramienta, como un cursor en la pantalla de una computadora. Esto significa que un paciente con ELA puede usar el correo electrónico, leer Internet y comunicarse con otros pensando en mover su mano o brazo (aunque el paciente paralizado no pueda realizar ese movimiento corporal). Los avances recientes han permitido a una paciente paralizada encerrada que sufrió un derrame cerebral hace 15 años controlar un brazo robótico e incluso alimentarse de café usando tecnología BCI.
A pesar de los increíbles avances en la tecnología BCI, también tiene limitaciones. La tecnología puede requerir muchas horas de entrenamiento y largos periodos de intensa concentración para el paciente; también puede requerir cirugía cerebral para implantar los dispositivos.
Enlace al aprendizaje
Mira este video en el que una mujer paralizada usa un brazo robótico controlado por el cerebro para llevar una bebida a la boca, entre otras imágenes de la tecnología de interfaz cerebro-computadora en acción.
Plasticidad sináptica
Las sinapsis no son estructuras estáticas. Pueden ser debilitados o fortalecidos. Se pueden romper, y se pueden hacer nuevas sinapsis. La plasticidad sináptica permite estos cambios, que son todos necesarios para un funcionamiento del sistema nervioso. De hecho, la plasticidad sináptica es la base del aprendizaje y la memoria. Dos procesos en particular, la potenciación a largo plazo (LTP) y la depresión a largo plazo (LTD) son formas importantes de plasticidad sináptica que ocurren en las sinapsis en el hipocampo, una región cerebral que participa en el almacenamiento de recuerdos.
Potenciación a largo plazo (LTP)
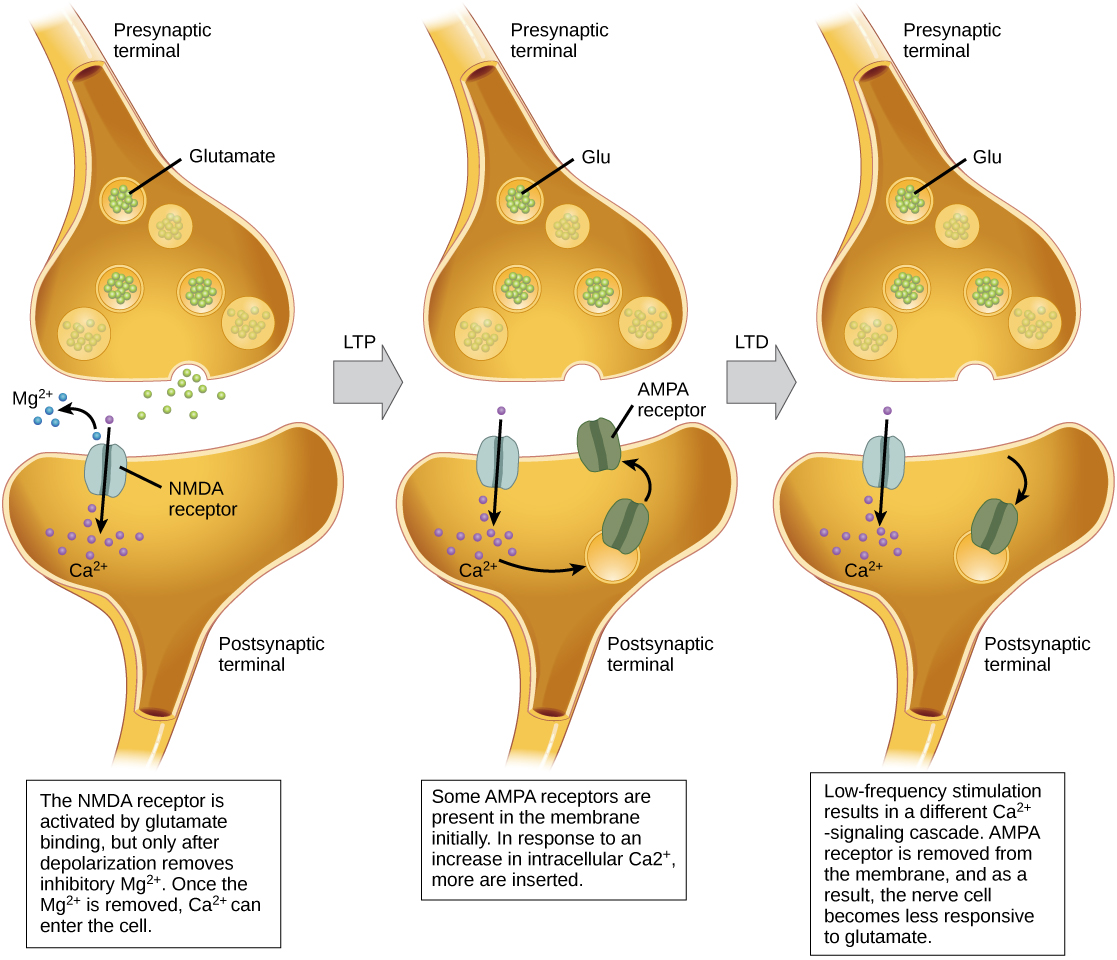
La potenciación a largo plazo (LTP) es un fortalecimiento persistente de una conexión sináptica. LTP se basa en el principio de Hebbian: celdas que disparan juntos cables juntos. Existen diversos mecanismos, ninguno completamente entendido, detrás del fortalecimiento sináptico visto con LTP. Un mecanismo conocido involucra un tipo de receptor postsináptico de glutamato, llamados receptores NMDA (N-metil-D-aspartato), mostrados en la Figura\(\PageIndex{10}\). Estos receptores normalmente están bloqueados por iones magnesio; sin embargo, cuando la neurona postsináptica es despolarizada por múltiples entradas presinápticas en rápida sucesión (ya sea de una neurona o múltiples neuronas), los iones de magnesio son forzados a salir permitiendo que los iones Ca pasen a la célula postsináptica. A continuación, los iones Ca 2+ que ingresan a la célula inician una cascada de señalización que provoca que un tipo diferente de receptor de glutamato, llamado receptores AMPA (ácido α-amino-3-hidroxi-5-metil-4-isoxazolpropiónico), se inserte en la membrana postsináptica, ya que los receptores AMPA activados permiten la entrada de iones positivos la celda. Entonces, la próxima vez que se libere glutamato de la membrana presináptica, tendrá un mayor efecto excitatorio (EPSP) sobre la célula postsináptica debido a que la unión del glutamato a estos receptores AMPA permitirá que entren más iones positivos en la célula. La inserción de receptores AMPA adicionales fortalece la sinapsis y significa que la neurona postsináptica es más probable que se active en respuesta a la liberación de neurotransmisores presinápticos. Algunas drogas de abuso cooptan por la vía LTP, y este fortalecimiento sináptico puede llevar a la adicción.
Depresión a largo plazo (LTD)
La depresión a largo plazo (LTD) es esencialmente la inversa de LTP: es un debilitamiento a largo plazo de una conexión sináptica. Un mecanismo que se sabe que causa el LTD también involucra a los receptores AMPA. En esta situación, el calcio que ingresa a través de los receptores NMDA inicia una cascada de señalización diferente, lo que da como resultado la eliminación de los receptores AMPA de la membrana postsináptica, como se ilustra en la Figura\(\PageIndex{10}\). La disminución de los receptores AMPA en la membrana hace que la neurona postsináptica sea menos sensible al glutamato liberado de la neurona presináptica. Si bien puede parecer contradictorio, LTD puede ser tan importante para el aprendizaje y la memoria como LTP. El debilitamiento y poda de sinapsis no utilizadas permite que se pierdan conexiones sin importancia y hace que las sinapsis que han sufrido LTP sean mucho más fuertes en comparación.
Resumen
Las neuronas tienen membranas cargadas porque hay diferentes concentraciones de iones dentro y fuera de la célula. Los canales iónicos controlados por voltaje controlan el movimiento de iones dentro y fuera de una neurona. Cuando una membrana neuronal se despolariza hasta al menos el umbral de excitación, se dispara un potencial de acción. Luego, el potencial de acción se propaga a lo largo de un axón mielinado hasta las terminales del axón. En una sinapsis química, el potencial de acción provoca la liberación de moléculas neurotransmisoras en la hendidura sináptica. Mediante la unión a receptores postsinápticos, el neurotransmisor puede causar potenciales postsinápticos excitadores o inhibitorios al despolarizar o hiperpolarizar, respectivamente, la membrana postsináptica. En las sinapsis eléctricas, el potencial de acción se comunica directamente a la célula postsináptica a través de uniones gap, proteínas de canal grande que conectan las membranas pre y postsinápticas. Las sinapsis no son estructuras estáticas y pueden fortalecerse y debilitarse. Dos mecanismos de plasticidad sináptica son la potenciación a largo plazo y la depresión a largo plazo.
Conexiones de arte
Figura\(\PageIndex{3}\): Los bloqueadores de los canales de potasio, como la amiodarona y la procainamida, que se utilizan para tratar la actividad eléctrica anormal en el corazón, llamada disritmia cardíaca, impiden el movimiento de K + a través de canales K + regulados por voltaje. ¿Qué parte del potencial de acción esperarías que afectaran los canales de potasio?
- Contestar
-
Los bloqueadores de los canales de potasio ralentizan la fase de repolarización, pero no tienen efecto sobre la despolarización.
Glosario
- potencial de acción
- cambio momentáneo autopropagante en el potencial eléctrico de una membrana neurona (o muscular)
- despolarización
- cambio en el potencial de membrana a un valor menos negativo
- Potencial postsináptico excitatorio (EPSP)
- despolarización de una membrana postsináptica causada por moléculas neurotransmisoras liberadas de una célula presináptica
- hiperpolarización
- cambio en el potencial de membrana a un valor más negativo
- Potencial postsináptico inhibitorio (IPSP)
- hiperpolarización de una membrana postsináptica causada por moléculas neurotransmisoras liberadas de una célula presináptica
- depresión a largo plazo (LTD)
- disminución prolongada del acoplamiento sináptico entre una célula pre y postsináptica
- Potenciación a largo plazo (LTP)
- aumento prolongado del acoplamiento sináptico entre una célula pre y postsináptica
- potencial de membrana
- diferencia en el potencial eléctrico entre el interior y el exterior de una celda
- periodo refractario
- período después de un potencial de acción cuando es más difícil o imposible que un potencial de acción sea disparado; causado por la inactivación de los canales de sodio y la activación de canales de potasio adicionales de la membrana
- conducción saltatoria
- “salto” de un potencial de acción a lo largo de un axón de un nodo de Ranvier al siguiente
- sumatoria
- proceso de múltiples entradas presinápticas creando EPSP aproximadamente al mismo tiempo para que la neurona postsináptica sea suficientemente despolarizada para disparar un potencial de acción
- hendidura sináptica
- espacio entre las membranas presinápticas y postsinápticas
- vesícula sináptica
- estructura esférica que contiene un neurotransmisor
- umbral de excitación
- nivel de despolarización necesario para un potencial de acción para disparar


