28.1: Historia y Cantidades Mecánicas Cuánticas
- Page ID
- 128197
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)objetivos de aprendizaje
- Explicar cómo la paradoja del efecto fotoeléctrico fue resuelta por Albert Einstein.
Los electrones se emiten de la materia cuando la luz brilla sobre una superficie. Esto se llama el efecto fotoeléctrico, y los electrones emitidos de esta manera se denominan fotoelectrones.

El Efecto Fotoeléctrico: Los electrones son emitidos por la materia por la luz absorbida.
El efecto fotoeléctrico normalmente requiere fotones con energías de unos pocos electronvoltios a 1 MeV para elementos más pesados, aproximadamente en el rango ultravioleta y de rayos X. El estudio del efecto fotoeléctrico condujo a pasos importantes en la comprensión de la naturaleza cuántica de la luz y los electrones e influyó en la formación del concepto de dualidad onda-partícula. El efecto fotoeléctrico también es ampliamente utilizado para investigar los niveles de energía electrónica en la materia.
Efecto Fotoeléctrico: Una breve introducción al Efecto Fotoeléctrico y la fotoemisión electrónica.
Heinrich Hertz descubrió el efecto fotoeléctrico en 1887. Aunque todavía no se habían descubierto electrones, Hertz observó que las corrientes eléctricas se producían cuando la luz ultravioleta brillaba sobre un metal. A principios del siglo XX, los físicos confirmaron que:
- La energía de los fotoelectrones individuales aumentó con la frecuencia (o color) de la luz, pero fue independiente de la intensidad (o brillo) de la radiación.
- La corriente fotoeléctrica fue determinada por la intensidad de la luz; duplicando la intensidad de la luz duplicó el número de electrones emitidos.
Esta observación fue muy desconcertante para muchos físicos. En su momento, la luz fue aceptada como un fenómeno de onda. Dado que la energía transportada por una onda solo debería depender de su amplitud (y no de la frecuencia de la onda), la dependencia de frecuencia de las energías de los electrones emitidos no tenía sentido.
En 1905, Albert Einstein resolvió esta aparente paradoja al describir la luz como compuesta de cuantos discretos (ahora llamados fotones), en lugar de ondas continuas. Basándose en la teoría de Max Planck sobre la radiación del cuerpo negro, Einstein teorizó que la energía en cada cuántica de luz era igual a la frecuencia multiplicada por una constante h, más tarde llamada constante de Planck. Un fotón por encima de una frecuencia umbral tiene la energía requerida para expulsar un solo electrón, creando el efecto observado. A medida que aumenta la frecuencia de la luz entrante, cada fotón transporta más energía, aumentando así la energía de cada fotoelectrón saliente. Al duplicar el número de fotones a medida que se duplica la intensidad, el número de photelectrones debería duplicarse en consecuencia.
Según Einstein, la energía cinética máxima de un electrón expulsado viene dada por\(\mathrm{K_{max}=hf−ϕ}\), donde\(\mathrm{h}\) está la constante de Planck y f es la frecuencia del fotón incidente. El término\(ϕ\) se conoce como la función de trabajo, la energía mínima requerida para eliminar un electrón de la superficie del metal. La función de trabajo satisface\(\mathrm{ϕ=hf_0}\), donde\(\mathrm{f_0}\) está la frecuencia umbral para el metal para el inicio del efecto fotoeléctrico. El valor de la función de trabajo es una propiedad intrínseca de la materia.
¿La luz se compone entonces de partículas u ondas? El experimento de Young sugirió que se trataba de una onda, pero el efecto fotoeléctrico indicó que debía estar hecha de partículas. Esta pregunta la resolvería de Broglie: la luz, y toda la materia, tienen propiedades tanto onduladas como partículas.
Energías Fotónicas del Espectro EM
El espectro electromagnético (EM) es el rango de todas las frecuencias posibles de radiación electromagnética.
objetivos de aprendizaje
- Comparar la energía fotónica con la frecuencia de la radiación
El espectro electromagnético
El espectro electromagnético (EM) es el rango de todas las frecuencias posibles de radiación electromagnética. El espectro electromagnético se extiende desde debajo de las bajas frecuencias utilizadas para la comunicación de radio moderna hasta la radiación gamma en el extremo de longitud de onda corta (alta frecuencia), cubriendo así longitudes de onda de miles de kiilómetros hasta las de una fracción del tamaño de un átomo (aproximadamente un angstrom). El límite para longitudes de onda largas es el tamaño del universo mismo.

Espectro electromagnético: Muestra el espectro electromagnético, incluyendo la región visible, en función tanto de la frecuencia (izquierda) como de la longitud de onda (derecha).
Las ecuaciones de Maxwell predijeron un número infinito de frecuencias de ondas electromagnéticas, todas viajando a la velocidad de la luz. Esta fue la primera indicación de la existencia de todo el espectro electromagnético. Las ondas predichas de Maxwell incluyeron ondas a frecuencias muy bajas en comparación con las infrarrojas, que en teoría podrían ser creadas por cargas oscilantes en un circuito eléctrico ordinario de cierto tipo. En 1886, el físico Hertz construyó un aparato para generar y detectar lo que ahora se llaman ondas de radio, en un intento de probar las ecuaciones de Maxwell y detectar dicha radiación electromagnética de baja frecuencia. Hertz encontró las ondas y pudo inferir (midiendo su longitud de onda y multiplicándola por su frecuencia) que viajaban a la velocidad de la luz. Hertz también demostró que la nueva radiación podría ser reflejada y refractada por diversos medios dieléctricos, de la misma manera que la luz.
Rellenar el espectro electromagnético
En 1895, Wilhelm Röntgen notó un nuevo tipo de radiación emitida durante un experimento con un tubo evacuado sometido a un alto voltaje. Llamó a estas radiaciones 'rayos X' y encontró que eran capaces de viajar a través de partes del cuerpo humano pero fueron reflejadas o detenidas por materia más densa como los huesos. En poco tiempo, hubo muchos usos nuevos para ellos en el campo de la medicina.
La última porción del espectro electromagnético se llenó con el descubrimiento de rayos gamma. En 1900, Paul Villard estaba estudiando las emisiones radiactivas de radio cuando identificó un nuevo tipo de radiación que primero pensó consistía en partículas similares a las partículas alfa y beta conocidas, pero mucho más penetrantes que cualquiera de ellas. Sin embargo, en 1910, el físico británico William Henry Bragg demostró que los rayos gamma son radiación electromagnética, no partículas. En 1914, Ernest Rutherford (quien los había nombrado rayos gamma en 1903 cuando se dio cuenta de que eran fundamentalmente diferentes de los rayos alfa y beta cargados) y Edward Andrade midieron sus longitudes de onda, y encontraron que los rayos gamma eran similares a los rayos X, pero con longitudes de onda más cortas y frecuencias más altas.
La relación entre la energía fotónica y la frecuencia y longitud de onda de la radiación se ilustra como la siguiente ecuación equilavente:\(\nu = \frac { c } { \lambda }\),\(\nu = \mathrm{\frac { E } { h }}\) o\(\mathrm { E } = \frac { \mathrm { hc } } { \lambda }\) donde νν es la frecuencia,\(\mathrm{λ}\) es la longitud de onda,\(\mathrm{E}\) es la energía fotónica,\(\mathrm{c}\) es la velocidad de la luz, y hh es la constante de Planck. Generalmente, la radiación electromagnética se clasifica por longitud de onda en ondas de radio, microondas, radiación de terahercios (o submilimétricos), infrarrojos, la región visible que los humanos perciben como luz, ultravioleta, rayos X y rayos gamma. El comportamiento de la radiación EM depende de su longitud de onda. Cuando la radiación EM interactúa con átomos y moléculas individuales, su comportamiento también depende de la cantidad de energía por cuántico (fotón) que transporta.
La mayoría de las partes del espectro electromagnético se utilizan en la ciencia para interacciones espectroscópicas y otras interacciones de sondeo como formas de estudiar y caracterizar la materia. Además, la radiación de diversas partes del espectro tiene muchos otros usos en las comunicaciones y la fabricación.
Energía, masa e impulso del fotón
Un fotón es una partícula elemental, el cuántico de la luz, que lleva impulso y energía.
objetivos de aprendizaje
- Estado de las propiedades físicas de un fotón
Un fotón es una partícula elemental, el cuántico de la luz. No tiene masa de descanso y no tiene carga eléctrica. El concepto moderno de fotones fue desarrollado gradualmente por Albert Einstein para explicar observaciones experimentales del efecto fotoeléctrico, que no se ajustaba al modelo clásico de onda de luz. En particular, el modelo de fotones explicó la dependencia de la frecuencia de la energía de la luz. Max Planck explicó la radiación del cuerpo negro utilizando modelos semiclásicos, en los que la luz aún es descrita por las ecuaciones de Maxwell, pero los objetos materiales que emiten y absorben la luz, lo hacen en cantidades de energía que se cuantifican.
Los fotones se emiten en muchos procesos naturales. Se emiten desde fuentes de luz como lámparas de pie o láseres. Por ejemplo, cuando se acelera una carga emite fotones, fenómeno conocido como radiación sincrotrón. Durante una transición molecular, atómica o nuclear a un nivel de energía inferior o superior, se emitirán o absorberán fotones de diversas energías respectivamente. También se puede emitir un fotón cuando una partícula y su correspondiente antipartícula son aniquiladas. Durante todos estos procesos, los fotones llevarán energía e impulso.

láser: Fotones emitidos en un haz coherente desde un láser.
Energía del fotón: A partir de los estudios de los efectos fotoeléctricos, la energía de un fotón es directamente proporcional a su frecuencia siendo la constante de Planck el factor de proporcionalidad. Por lo tanto, ya lo sabemos\(\mathrm { E } = \mathrm { h } \nu\) (Ec. 1), dónde\(\mathrm{E}\) está la energía y νν es la frecuencia.
Momentum de fotón: Según la teoría de la Relatividad Especial, la energía y el impulso (p) de una partícula con masa de reposo m tiene la siguiente relación:\(\mathrm { E } ^ { 2 } = \left( \mathrm { mc } ^ { 2 } \right) ^ { 2 } + \mathrm { p } ^ { 2 } \mathrm { c } ^ { 2 }\), dónde\(\mathrm{c}\) está la velocidad de la luz. En el caso de un fotón con masa de reposo cero, obtenemos\(\mathrm { E } = \mathrm { p c}\). Combinando esto con la Ecuación 1, obtenemos\(\mathrm { p } = \frac { \mathrm { h } \nu } { \mathrm { c } } = \frac { \mathrm { h } } { \lambda }\). Aquí,\(\mathrm{λ}\) está la longitud de onda de la luz. Dado que el momentum es una cantidad de vector y p apunta en la dirección de la propagación del fotón, podemos escribir\(\mathrm { p } = \mathrm { h } \mathrm { k }\), donde\(\mathrm { h } = \frac { \mathrm { h } } { 2 \pi }\) y es\(\mathrm{k}\) un vector de onda.
Quizás te preguntes cómo un objeto con masa de reposo cero puede tener un impulso distinto de cero. Esta confusión a menudo surge debido a la forma de momentum comúnmente utilizada (mvmv en mecánica no relativista y γmvγmv en mecánica relativista, donde vv es velocidad y\(\gamma = \frac { 1 } { \sqrt { 1 - \frac { v ^ { 2 } } { c ^ { 2 } } } }\).) Esta fórmula, obviamente, no debería usarse en el caso\(\mathrm{v=c}\).
Implicaciones de la Mecánica
La mecánica cuántica ha tenido un enorme éxito al explicar los sistemas microscópicos y se ha convertido en una base de la ciencia y la tecnología modernas.
objetivos de aprendizaje
- Explicar la importancia de la mecánica cuántica para la tecnología y otras ramas de la ciencia
El campo de la mecánica cuántica ha tenido un enorme éxito al explicar muchas de las características de nuestro mundo. El comportamiento de las partículas subatómicas (electrones, protones, neutrones, fotones y otros) que componen todas las formas de materia a menudo puede describirse satisfactoriamente solo usando la mecánica cuántica. La mecánica cuántica también ha influenciado fuertemente la teoría de cuerdas.
La mecánica cuántica también es de vital importancia para comprender cómo los átomos individuales se combinan covalentemente para formar moléculas. La aplicación de la mecánica cuántica a la química se conoce como química cuántica. La mecánica cuántica relativista puede, en principio, describir matemáticamente la mayor parte de la química. La mecánica cuántica también puede proporcionar información cuantitativa sobre los procesos de enlace iónico y covalente al mostrar explícitamente qué moléculas son energéticamente favorables a qué otras moléculas y las magnitudes de las energías involucradas. Además, la mayoría de los cálculos realizados en la química computacional moderna se basan en la mecánica cuántica.
Un gran número de invenciones tecnológicas modernas operan en una escala donde los efectos cuánticos son significativos. Los ejemplos incluyen el láser, el transistor (y por lo tanto el microchip), el microscopio electrónico y la resonancia magnética (MRI). El estudio de los semiconductores llevó a la invención del diodo y el transistor, que son partes indispensables de los sistemas y dispositivos electrónicos modernos.

Láser: Láseres rojo (635-nm), verde (532-nm) y azul-violeta (445-nm)
Actualmente, los investigadores están buscando métodos sólidos para manipular directamente los estados cuánticos. Se están haciendo esfuerzos para desarrollar más plenamente la criptografía cuántica, que teóricamente permitirá una transmisión segura garantizada de la información. Un objetivo más distante es el desarrollo de computadoras cuánticas, que se espera realicen ciertas tareas computacionales exponencialmente más rápido que las computadoras clásicas. Otro tema de investigación activa es la teletransportación cuántica, que trata de técnicas para transmitir información cuántica a distancias arbitrarias.
Dualidad de onda de partículas
Onda: la dualidad de partículas postula que todas las entidades físicas exhiben propiedades de onda y partículas.
objetivos de aprendizaje
- Describir experimentos que demostraron la dualidad onda-partícula de entidades físicas
Onda: la dualidad de partículas postula que todas las entidades físicas exhiben propiedades de onda y partículas. Como concepto central de la mecánica cuántica, esta dualidad aborda la incapacidad de conceptos clásicos como “partícula” y “onda” para describir completamente el comportamiento de (generalmente) objetos microscópicos.
Desde el punto de vista de la física clásica, las partículas y las ondas son conceptos distintos. Son mutuamente excluyentes, en el sentido de que una partícula no exhibe propiedades onduladas y viceversa. Intuitivamente, una pelota de béisbol no desaparece a través de interferencias destructivas, y nuestra voz no puede ser localizada en el espacio. ¿Por qué entonces es que los físicos creen en la dualidad onda-partícula? Porque así es como opera la madre Naturaleza, como han aprendido de varios experimentos innovadores. Aquí hay una breve lista cronológica de esos experimentos:
- Experimento de doble hendidura de Young: A principios del siglo XIX, los experimentos de doble rendija de Young y Fresnel proporcionaron evidencia de que la luz es una onda. En 1861, James Clerk Maxwell explicó la luz como la propagación de ondas electromagnéticas según las ecuaciones de Maxwell.
- Radiación de cuerpo negro: En 1901, para explicar el espectro observado de luz emitida por un objeto resplandeciente, Max Planck asumió que la energía de la radiación en la cavidad estaba cuantificada, contradiciendo la creencia establecida de que la radiación electromagnética es una onda.
- Efecto fotoeléctrico: La teoría clásica de ondas de la luz tampoco explica el efecto fotoeléctrico. En 1905, Albert Einstein explicó los efectos fotoeléctricos postulando la existencia de fotones, cuantos de energía lumínica con cualidades particuladas.
- Onda de De Broglie (onda de materia): En 1924, Louis-Victor de Broglie formuló la hipótesis de Broglie, alegando que toda la materia, no solo la luz, tiene una naturaleza ondulada. Su hipótesis se confirmó pronto con la observación de que los electrones (materia) también muestran patrones de difracción, que es intuitivamente una propiedad de onda.
A partir de estos logros históricos, los físicos aceptan ahora que todas las entidades de la naturaleza se comportan tanto como una partícula como una onda, dependiendo de los detalles de los fenómenos en consideración. Por su aspecto contrario a la intuición, el significado de la dualidad partícula-onda sigue siendo un punto de debate en la física cuántica. La interpretación estándar es que el acto de medición provoca que el conjunto de probabilidades, gobernado por una función de distribución de probabilidad adquirida a partir de una “onda”, asuma inmediata y aleatoriamente uno de los valores posibles, dando lugar a un resultado similar a una “partícula”.
Entonces, ¿por qué no notamos que un beisbol actúa como una ola? La longitud de onda de la onda de la materia asociada a una pelota de béisbol, digamos que se mueve a 95 millas por hora, es extremadamente pequeña en comparación con el tamaño de la pelota por lo que el comportamiento ondulatorio nunca se nota.
Difracción revisitada
La hipótesis de De Broglie fue que las partículas deben mostrar propiedades onduladas como difracción o interferencia.
objetivos de aprendizaje
- Comparar la aplicación de la difracción de rayos X, electrones y neutrones para la investigación de materiales
La hipótesis de Broglie, formulada en 1924, predice que las partículas también deben comportarse como ondas. La longitud de onda de un electrón viene dada por la ecuación de Broglie\(\mathrm{\lambda = \frac { h } { p }}\). Aquí\(\mathrm{h}\) está la constante de Planck y pp el impulso relativista del electrón. \(\mathrm{λ}\)se llama la longitud de onda de Broglie.
De la obra de Planck (radiación de cuerpo negro) y Einstein (efecto fotoeléctrico), los físicos entendieron que las ondas electromagnéticas a veces se comportaban como partículas. La hipótesis de De Broglie es complementaria a esta idea: las partículas también deben mostrar propiedades onduladas como la difracción o la interferencia. La fórmula de De Broglie se confirmó tres años después para los electrones (que tienen una masa de reposo) con la observación de difracción de electrones en dos experimentos independientes. George Paget Thomson pasó un haz de electrones a través de una delgada película metálica y observó los patrones de interferencia predichos. Clinton Joseph Davisson y Lester Halbert Germerguiaron su haz a través de una rejilla cristalina para observar patrones de difracción.
La difracción de rayos X es una herramienta comúnmente utilizada en la investigación de materiales. Gracias a la dualidad onda-partícula, la difracción de onda de materia también se puede utilizar para este propósito. El electrón, que es fácil de producir y manipular, es una opción común. Un neutrón es otra partícula de elección. Debido a los diferentes tipos de interacciones involucradas en los procesos de difracción, los tres tipos de radiación (rayos X, electrones, neutrones) son adecuados para diferentes tipos de estudios.
La difracción de electrones se utiliza con mayor frecuencia en la física y química del estado sólido para estudiar la estructura cristalina de los sólidos. Los experimentos generalmente se realizan usando un microscopio electrónico de transmisión o un microscopio electrónico de barrido. En estos instrumentos, los electrones son acelerados por un potencial electrostático con el fin de obtener la energía deseada y, así, la longitud de onda antes de que interactúen con la muestra a estudiar. La estructura periódica de un sólido cristalino actúa como una rejilla de difracción, dispersando los electrones de manera predecible. Trabajando a partir del patrón de difracción observado, entonces es posible deducir la estructura del cristal produciendo el patrón de difracción. A diferencia de otros tipos de radiación utilizados en estudios de difracción de materiales, como los rayos X y los neutrones, los electrones son partículas cargadas e interactúan con la materia a través de las fuerzas de Coulomb. Esto significa que los electrones incidentes sienten la influencia tanto de los núcleos atómicos cargados positivamente como de los electrones circundantes. En comparación, los rayos X interactúan con la distribución espacial de los electrones de valencia, mientras que los neutrones son dispersados por los núcleos atómicos a través de la fuerte fuerza nuclear.

Patrón de difracción de electrones: Patrón de difracción de electrones típico obtenido en un microscopio electrónico de transmisión con un haz de electrones paralelo.
Los neutrones también se han utilizado para estudiar estructuras cristalinas. Están dispersos por los núcleos de los átomos, a diferencia de los rayos X, que son dispersos por los electrones de los átomos. Así, la difracción de neutrones tiene algunas diferencias clave en comparación con los métodos más comunes que utilizan rayos X o electrones. Por ejemplo, la dispersión de los rayos X depende en gran medida del número atómico de los átomos (es decir, el número de electrones), mientras que la dispersión de neutrones depende de las propiedades de los núcleos. Además, el momento magnético del neutrón es distinto de cero, y así también puede ser dispersado por campos magnéticos. Esto significa que la dispersión de neutrones es más útil para determinar las propiedades de los núcleos atómicos, a pesar de que los neutrones son significativamente más difíciles de crear, manipular y detectar en comparación con los rayos X y los electrones.
La función de onda
Una función de onda es una amplitud de probabilidad en la mecánica cuántica que describe el estado cuántico de una partícula y cómo se comporta.
objetivos de aprendizaje
- Relacionar la función de onda con la densidad de probabilidad de encontrar una partícula, comentando las restricciones que la función de onda debe satisfacer para que esto tenga sentido
En mecánica cuántica, una función de onda es una amplitud de probabilidad que describe el estado cuántico de una partícula y cómo se comporta. Por lo general, sus valores son números complejos. Para una sola partícula, es una función del espacio y el tiempo. Los símbolos más comunes para una función de onda son\(\psi ( x )\) o\(\Psi ( x )\) (psi en minúscula o mayúscula, respectivamente), cuando la función de onda se da en función de la posición\(\mathrm{x}\). Si bien\(\psi\) es un número complejo,\(| \psi | 2\) es un número real y corresponde a la densidad de probabilidad de encontrar una partícula en un lugar dado en un momento dado, si se mide la posición de la partícula.
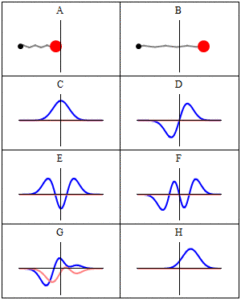
Trayectorias de un oscilador armónico: Esta figura muestra algunas trayectorias de un oscilador armónico (una bola unida a un resorte) en mecánica clásica (A-B) y mecánica cuántica (C-H). En mecánica cuántica (C-H), la pelota tiene una función de onda, la cual se muestra con su parte real en azul y su parte imaginaria en rojo. Las trayectorias C-F son ejemplos de ondas estacionarias, o “estados estacionarios”. Cada frecuencia de onda estacionaria es proporcional a un posible nivel de energía del oscilador. Esta “cuantificación de energía” no ocurre en la física clásica, donde el oscilador puede tener cualquier energía.
Las leyes de la mecánica cuántica (la ecuación de Schrödinger) describen cómo evoluciona la función de onda a lo largo del tiempo. La función de onda se comporta cualitativamente como otras olas, como olas de agua u ondas en una cuerda, porque la ecuación de Schrödinger es matemáticamente un tipo de ecuación de onda. Esto explica el nombre de “función de onda” y da lugar a la dualidad onda-partícula.
La función de onda debe satisfacer las siguientes restricciones para que los cálculos y la interpretación física tengan sentido:
- Debe ser finito en todas partes.
- Debe ser en todas partes una función continua y continuamente diferenciable.
- Debe en todas partes satisfacer la condición de normalización relevante para que la partícula (o sistema de partículas) exista en algún lugar con certeza del 100 por ciento.
Si no se cumplen estos requisitos, no es posible interpretar la función de onda como una amplitud de probabilidad. Esto se debe a que los valores de la función de onda y sus derivadas de primer orden pueden no ser finitos y definidos (teniendo exactamente un valor), lo que significa que las probabilidades pueden ser infinitas y tener múltiples valores en cualquier posición y tiempo, lo cual es una tontería. Además, cuando usamos la función de onda para calcular una observación del sistema cuántico sin cumplir con estos requisitos, no habrá valores finitos o definidos para usar (en este caso la observación puede tomar una serie de valores y puede ser infinita). Esto no es posible que ocurra en un experimento del mundo real. Por lo tanto, una función de onda es significativa solo si se cumplen estas condiciones.
de Broglie y la naturaleza ondulada de la materia
El concepto de “ondas de materia” o “ondas de Broglie” refleja la dualidad onda-partícula de la materia.
objetivos de aprendizaje
- Formular la relación de Broglie como una ecuación
En la mecánica cuántica, el concepto de ondas de materia (o ondas de Broglie) refleja la dualidad onda-partícula de la materia. La teoría fue propuesta por Louis de Broglie en 1924 en su tesis doctoral. Las relaciones de Broglie muestran que la longitud de onda es inversamente proporcional al impulso de una partícula, y también se llama longitud de onda de Broglie.
Einstein derivó en su teoría de la relatividad especial que la energía y el impulso de un fotón tiene la siguiente relación:
\(\mathrm { E } = \mathrm { p } \mathrm { c }\)(\(\mathrm{E}\): energía,\(\mathrm{p}\): impulso,\(\mathrm{c}\): velocidad de la luz).
También demostró, en su estudio de los efectos fotoeléctricos, que la energía de un fotón es directamente proporcional a su frecuencia, dándonos esta ecuación:
\(\mathrm { E } = \mathrm { h} \nu \)(\(\mathrm{h}\): Constante de Planck,\(\nu\): frecuencia).
Combinando las dos ecuaciones, podemos derivar una relación entre el momento y la longitud de onda de la luz:
\(\mathrm { p } = \frac { \mathrm { E } } { \mathrm { c } } = \frac { \mathrm { h } \nu } { \mathrm { c } } = \frac { \mathrm { h } } { \lambda }\). Por lo tanto, llegamos a\(\mathrm{\lambda = \frac { h } { p }}\).
La hipótesis de De Broglie es que esta relación\(\mathrm{λ=hp}\), derivada de ondas electromagnéticas, puede adoptarse para describir también la materia (por ejemplo, electrón, neutrón, etc.).
De Broglie no tenía ninguna prueba experimental al momento de su propuesta. Clinton Davisson y Lester Germer tardaron tres años en observar patrones de difracción de electrones que pasan por un objetivo metálico cristalino (ver). Antes de la aceptación de la hipótesis de Broglie, la difracción era una propiedad pensada para ser exhibida solo por las ondas. Por lo tanto, la presencia de cualquier efecto de difracción por materia demostró la naturaleza ondulada de la materia. Este fue un resultado fundamental en el desarrollo de la mecánica cuántica. Así como el efecto fotoeléctrico demostró la naturaleza de partículas de la luz, el experimento Davisson—Germer mostró la naturaleza onda-naturaleza de la materia, completando así la teoría de la dualidad onda-partícula.

Configuración experimental de Davisson-Germer: El experimento incluyó un cañón de electrones consistente en un filamento calentado que liberaba electrones térmicamente excitados, los cuales luego se aceleraron a través de una diferencia de potencial (dándoles una cierta cantidad de energía cinética hacia el cristal de níquel). Para evitar colisiones de los electrones con otras moléculas en su camino hacia la superficie, el experimento se realizó en una cámara de vacío. Para medir el número de electrones que se dispersaron en diferentes ángulos, se utilizó un detector de electrones que se podía mover en una trayectoria de arco alrededor del cristal. El detector fue diseñado para aceptar solo electrones dispersos elásticamente.
Los experimentos con difracción de Fresnel y reflexión especular de átomos neutros confirman la aplicación a los átomos de la hipótesis de Broglie. Además, experimentos recientes confirman las relaciones para moléculas e incluso macromoléculas, normalmente consideradas demasiado grandes para sufrir efectos mecánicos cuánticos. En 1999, un equipo de investigación en Viena demostró difracción para moléculas tan grandes como los fullerenos. Los investigadores calcularon una longitud de onda De Broglie de la\(\mathrm{C_{60}}\) velocidad más probable como 2.5 pm.
El principio de incertidumbre de Heisenberg
El principio de incertidumbre afirma un límite básico a la precisión con la que se pueden conocer simultáneamente algunas propiedades físicas de una partícula.
objetivos de aprendizaje
- Relacionar el principio de incertidumbre de Heisenberg con la naturaleza de onda de materia de todos los objetos cuánticos
El principio de incertidumbre es cualquiera de una variedad de desigualdades matemáticas, afirmando un límite fundamental a la precisión con la que ciertos pares de propiedades físicas de una partícula, como la posición\(\mathrm{x}\) y el impulso pp o la energía\(\mathrm{E}\) y el tiempo\(\mathrm{t}\), pueden conocerse simultáneamente. Cuanto más precisamente se determine la posición de alguna partícula, menos precisamente se puede conocer su impulso, y viceversa. Esto puede formularse como la siguiente desigualdad:\(\sigma _ { \mathrm { x } } \sigma _ { \mathrm { y } } \geq \frac { \mathrm { \overline{h} } } { 2 }\), donde\(\mathrm{σ_x}\) está la desviación estándar de posición, σp es la desviación estándar del momento, y\(\overline { \mathrm { h } } = \frac { \mathrm { h } } { 2 \pi }\). El principio de incertidumbre es inherente a las propiedades de todos los sistemas ondulados, y surge en la mecánica cuántica simplemente debido a la naturaleza de onda de materia de todos los objetos cuánticos. Así, el principio de incertidumbre en realidad establece una propiedad fundamental de los sistemas cuánticos, y no es una declaración sobre el éxito observacional de la tecnología actual.
El principio es bastante contradictorio, por lo que los primeros estudiantes de la teoría cuántica tuvieron que estar seguros de que las medidas ingenuas para violarlo estaban obligadas a ser siempre inviables. Una forma en la que Heisenberg ilustró originalmente la imposibilidad intrínseca de violar el principio de incertidumbre es utilizando un microscopio imaginario como dispositivo de medición.

Microscopio Heisenberg: Microscopio de Heisenberg, con cono de rayos de luz enfocándose en una partícula con ángulo\(ϵ\) Se imagina a un experimentador tratando de medir la posición y el impulso de un electrón disparándole un fotón.
Ejemplo\(\PageIndex{1}\):
Ejemplo Uno
Si el fotón tiene una longitud de onda corta y por lo tanto un impulso grande, la posición se puede medir con precisión. Pero el fotón se dispersa en una dirección aleatoria, transfiriendo una cantidad grande e incierta de impulso al electrón. Si el fotón tiene una longitud de onda larga y un impulso bajo, la colisión no perturbe mucho el impulso del electrón, sino que la dispersión revelará su posición solo vagamente.
Ejemplo Dos
Si se utiliza una gran apertura para el microscopio, la ubicación del electrón puede resolverse bien (ver criterio de Rayleigh); pero por el principio de conservación del impulso, el impulso transversal del fotón entrante y de ahí el nuevo impulso del electrón se resuelve mal. Si se usa una abertura pequeña, la precisión de ambas resoluciones es al revés.
Argumento de Heisenberg
El argumento de Heisenberg se resume de la siguiente manera. Comienza suponiendo que un electrón es como una partícula clásica, moviéndose en la dirección xx a lo largo de una línea debajo del microscopio, como en la ilustración de la derecha. Dejar que el cono de rayos de luz que sale de la lente del microscopio y enfocarse en el electrón haga un ángulo εε con el electrón. Dejar\(\lambda\) ser la longitud de onda de los rayos de luz. Entonces, según las leyes de la óptica clásica, el microscopio sólo puede resolver la posición del electrón hasta una precisión de\(\delta \mathrm { x } = \frac { \lambda } { \sin ( \varepsilon / 2 ) }\) Cuando un observador percibe una imagen de la partícula, es porque los rayos de luz golpean la partícula y rebotan a través del microscopio a su ojo. Sin embargo, sabemos por evidencia experimental que cuando un fotón golpea un electrón, este último tiene un retroceso con impulso proporcional a\(\mathrm{h/λ}\), donde\(\mathrm{h}\) está la constante de Planck.
Es en este punto que Heisenberg introduce la indeterminación objetiva en el experimento del pensamiento. Escribe que “no se puede conocer exactamente el retroceso, ya que la dirección del fotón dispersado es indeterminada dentro del haz de rayos que entran al microscopio”. En particular, el impulso del electrón en la dirección xx solo se determina hasta δpx≈hλsin (ε/2) δpx≈hλsin (ε/2). Combinando las relaciones para\(\mathrm{δx}\) y\(\mathrm{δp_x}\), así tenemos eso\(\delta \mathbf { x } \cdot \delta \mathrm { p } _ { \mathbf { x } } \approx \left( \frac { \lambda } { \sin ( \varepsilon / 2 ) } \right) \left( \frac { \mathrm { h } } { \lambda } \sin ( \varepsilon / 2 ) \right) = \mathrm { h }\), que es una expresión aproximada del principio de incertidumbre de Heisenberg.
Principio de incertidumbre de Heisenberg derivado y explicado
Uno de los resultados más citados de la física cuántica, este doozie nos obliga a reconsiderar lo que podemos saber sobre el universo. Algunas cosas no se pueden conocer simultáneamente. De hecho, si algo de un sistema se conoce perfectamente, es probable que haya otra característica que esté completamente envuelta en la incertidumbre. ¡Así que las cifras significativas SON importantes después de todo!
Implicaciones filosóficas
Desde sus inicios, muchos aspectos contra-intuitivos de la mecánica cuántica han provocado fuertes debates filosóficos.
objetivos de aprendizaje
- Formular la interpretación de Copenhague de la naturaleza probabilística de la mecánica cuántica
Desde sus inicios, muchos aspectos contra-intuitivos y resultados de la mecánica cuántica han provocado fuertes debates filosóficos y muchas interpretaciones. Incluso cuestiones fundamentales, como las reglas básicas de Max Born interpretando\(ψ∗ψ\) como una función de densidad de probabilidad tardaron décadas en ser apreciadas por la sociedad y muchos científicos líderes. En efecto, el reconocido físico Richard Feynman dijo una vez: “Creo que puedo decir con seguridad que nadie entiende la mecánica cuántica”.
La Interpretación de Copenhague
La interpretación de Copenhague —debida en gran parte al físico teórico danés Niels Bohr, mostrado en— sigue siendo un formalismo mecánico cuántico que es ampliamente aceptado entre los físicos, unos 75 años después de su enunciación. Según esta interpretación, la naturaleza probabilística de la mecánica cuántica no es una característica temporal que eventualmente será reemplazada por una teoría determinista, sino que debe considerarse una renuncia final a la idea clásica de causalidad.

Niels Bohr y Albert Einstein: Niels Bohr (izquierda) y Albert Einstein (derecha). A pesar de sus contribuciones pioneras al inicio de la mecánica cuántica, no estuvieron de acuerdo en su interpretación.
La interpretación de Copenhague tiene implicaciones filosóficas para el concepto de determinismo. Según la teoría del determinismo, para todo lo que sucede hay condiciones tales que, dadas esas condiciones, nada más podría pasar. El determinismo y el libre voluntad parecen ser mutuamente excluyentes. Si el universo, y cualquier persona en él se rigen por leyes estrictas y universales, entonces eso significa que el comportamiento de una persona podría predecirse con base en el conocimiento suficiente de las circunstancias obtenidas antes del comportamiento de esa persona. Sin embargo, la interpretación de Copenhague sugiere un universo en el que los resultados no están completamente determinados por circunstancias previas sino también por la probabilidad. Esto dio a los pensadores alternativas a posibilidades estrictamente vinculadas, proponiendo un modelo para un universo que sigue reglas generales pero que nunca tuvo un futuro predeterminado.
Implicaciones filosóficas
También se cree en ello que cualquier aplicación bien definida del formalismo mecánico cuántico siempre debe hacer referencia al arreglo experimental. Esto se debe al principio mecánico cuántico del colapso de la función de onda. Es decir, una función de onda que inicialmente se encuentra en una superposición de varios estados posibles diferentes parece reducirse a uno solo de esos estados después de la interacción con un observador. En términos simplificados, es la reducción de las posibilidades físicas en una sola posibilidad vista por un observador. Esto plantea interrogantes filosóficos sobre si realmente existe algo que nunca se observa.
Paradoja de Einstein-Podolsky-Rosen (EPR)
Albert Einstein (mostrado en, él mismo uno de los fundadores de la teoría cuántica) no le gustó esta pérdida de determinismo en la medición en la interpretación de Copenhague. Einstein sostuvo que debería haber una teoría local de variables ocultas subyacente a la mecánica cuántica y, en consecuencia, que la teoría actual era incompleta. Produjo una serie de objeciones a la teoría, la más famosa de las cuales se ha dado a conocer como la paradoja de Einstein-Podolsky-Rosen (EPR). John Bell demostró por el teorema de Bell que esta paradoja del “EPR” condujo a diferencias experimentalmente comprobables entre la mecánica cuántica y las teorías realistas locales. Se han realizado experimentos confirmando la precisión de la mecánica cuántica, demostrando así que el mundo físico no puede ser descrito por ninguna teoría realista local. Los debates de Bohr-Einstein proporcionan una crítica vibrante a la Interpretación de Copenhague desde un punto de vista epistemológico.
Enredo cuántico
Uno de los aspectos más extraños de la mecánica cuántica se conoce como enredo cuántico. El enredo cuántico ocurre cuando las partículas interactúan físicamente y luego se separan, mientras se isloan del resto del universo para evitar cualquier deterioro del estado cuántico. Según la interpretación de Copenhague de la mecánica cuántica, su estado compartido es indefinido hasta que se mide. Una vez que se mide una partícula en estado enredado y se determina su estado, la interpretación de Copenhague exige que el estado de las otras partículas también se determine instantáneamente. Esta extraña naturaleza de acción a distancia (que aparentemente viola el límite de velocidad en la transmisión de información implícita en la teoría de la relatividad) es lo que más molestó a Einstein. (Según la teoría de la relatividad, nada puede viajar más rápido que la velocidad de la luz en el vacío. Esto aparentemente pone un límite a la velocidad a la que se puede transmitir la información.) El enredo cuántico es el elemento clave en las propuestas de computadoras cuánticas y teletransportación cuántica.
Puntos Clave
- La energía de los electrones emitidos depende únicamente de la frecuencia de la luz incidente, y no de la intensidad de la luz.
- Einstein explicó el efecto fotoeléctrico al describir la luz como compuesta por partículas discretas.
- El estudio del efecto fotoeléctrico condujo a pasos importantes en la comprensión de la naturaleza cuántica de la luz y los electrones, lo que eventualmente conduciría al concepto de dualidad onda-partícula.
- La radiación electromagnética se clasifica según la longitud de onda, dividida en ondas de radio, microondas, radiación de terahercios (o submilimétricos), infrarrojos, la región visible que los humanos perciben como luz, ultravioleta, rayos X y rayos gamma.
- La energía fotónica es proporcional a la frecuencia de la radiación.
- La mayoría de las partes del espectro electromagnético se utilizan en la ciencia para interacciones espectroscópicas y otras interacciones de sondeo como formas de estudiar y caracterizar la materia.
- \(\mathrm { E } = \mathrm { hv }\)La energía del fotón es proporcional a su frecuencia.
- \(\mathrm{p=hk}\)El momento del fotón es proporcional al vector de onda.
- La masa de descanso del fotón es 0.
- Un gran número de invenciones tecnológicas modernas se basan en la mecánica cuántica, incluyendo el láser, el transistor, el microscopio electrónico y la resonancia magnética.
- La mecánica cuántica también es de vital importancia para comprender cómo los átomos individuales se combinan covalentemente para formar moléculas. La aplicación de la mecánica cuántica a la química se conoce como química cuántica.
- Actualmente, los investigadores buscan métodos sólidos para manipular directamente los estados cuánticos para aplicaciones en informática y ciencias de la información.
- Todas las entidades en la Naturaleza se comportan tanto como una partícula como una onda, dependiendo de las especificidades de los fenómenos en consideración.
- La dualidad partícula-onda suele estar oculta en fenómenos macroscópicos, conforme a nuestra intuición.
- En el experimento de doble rendija de electrones, el evento individual muestra una propiedad de localización similar a partículas (o un “punto”). Después de muchas repeticiones, sin embargo, la imagen muestra un patrón de interferencia, lo que indica que cada evento de hecho está gobernado por una distribución de probabilidad.
- La longitud de onda de un electrón viene dada por la ecuación de Broglie\(\mathrm{\lambda = \frac { h } { p }}\).
- Debido a las diferentes formas de interacción involucradas, los rayos X, los electrones y los neutrones son adecuados para diferentes estudios de las propiedades del material.
- La idea de De Broglie completó la dualidad onda-partícula.
- \(| \psi | 2 ( \mathrm { x } )\)corresponde a la densidad de probabilidad de encontrar una partícula en una ubicación dada x en un momento dado.
- Las leyes de la mecánica cuántica (la ecuación de Schrödinger) describen cómo evoluciona la función de onda a lo largo del tiempo. La ecuación de Schrödinger es un tipo de ecuación de onda, que explica el nombre de “función de onda”.
- Una función de onda debe satisfacer un conjunto de restricciones matemáticas para que los cálculos y la interpretación física tengan sentido.
- Las relaciones de Broglie muestran que la longitud de onda es inversamente proporcional al momento de una partícula.
- El experimento de Davisson-Germer demostró la naturaleza ondulada de la materia y completó la teoría de la dualidad onda-partícula.
- Los experimentos demostraron que la hipótesis de Broglie es aplicable a átomos y macromoléculas.
- El principio de incertidumbre es inherente a las propiedades de todos los sistemas ondulados, y que surge en la mecánica cuántica se debe simplemente a la naturaleza de onda de la materia de todos los objetos cuánticos.
- El principio de incertidumbre no es una declaración sobre el éxito observacional de la tecnología actual.
- Cuanto más precisamente se determine la posición de alguna partícula, menos precisamente se puede conocer su impulso, y viceversa. Esto puede formularse como la siguiente desigualdad:\(\sigma _ { \mathrm { X } } \sigma _ { \mathrm { y } } \geq \frac { \mathrm { \overline{h} } } { 2 }\).
- Según la interpretación de Copenhague, la naturaleza probabilística de la mecánica cuántica es intrínseca en nuestro universo físico.
- Cuando se produce el colapso de la función de onda cuántica, las posibilidades físicas se reducen en una sola posibilidad como lo ve un observador.
- Una vez que se mide una partícula en estado enredado y se determina su estado, la interpretación de Copenhague exige que el estado de la otra partícula enredada también se determine instantáneamente.
Términos Clave
- radiación de cuerpo negro: El tipo de radiación electromagnética dentro o alrededor de un cuerpo en equilibrio termodinámico con su entorno, o emitida por un cuerpo negro (un cuerpo opaco y no reflectante) mantenido a temperatura constante y uniforme.
- fotoelectrón: Electrones emitidos por la materia absorbiendo energía de la radiación electromagnética.
- dualidad onda-partícula: Una postulación en la que todas las partículas presentan propiedades tanto de onda como de partícula. Es un concepto central de la mecánica cuántica.
- Constante de Planck: una constante física que es la cuántica de acción en la mecánica cuántica. Tiene una unidad de momento angular. La constante de Planck se describió por primera vez como la constante de proporcionalidad entre la energía de un fotón (unidad de radiación electromagnética) y la frecuencia de su onda electromagnética asociada en su derivación de la ley de Planck
- Ecuaciones de Maxwell: Un conjunto de ecuaciones que describen cómo los campos eléctricos y magnéticos son generados y alterados entre sí y por cargas y corrientes.
- partícula elemental: una partícula que no se sabe que tiene ninguna subestructura
- Efecto fotoeléctrico: La ocurrencia de electrones que son emitidos por la materia (metales y sólidos no metálicos, líquidos o gases) como consecuencia de su absorción de energía de la radiación electromagnética.
- criptografía: la práctica y estudio de técnicas de comunicación segura en presencia de terceros
- Mecánica cuántica relativista: un marco teórico para la construcción de modelos mecánicos cuánticos de campos y sistemas de muchos cuerpos
- teoría de cuerdas: un marco de investigación activo en física de partículas que intenta conciliar la mecánica cuántica y la relatividad general
- cuerpo negro: Un cuerpo físico idealizado que absorbe toda la radiación electromagnética incidente, independientemente de la frecuencia o ángulo de incidencia. Si bien el cuerpo negro es un concepto teórico, se pueden encontrar realizaciones aproximadas del cuerpo negro en la naturaleza.
- rejilla: Cualquier colección regularmente espaciada de elementos esencialmente idénticos, paralelos y alargados.
- Ecuación de Schrödinger: Un diferencial parcial que describe cómo el estado cuántico de algunos sistemas físicos cambia con el tiempo. Fue formulado a finales de 1925 y publicado en 1926 por el físico austriaco Erwin Schrödinger
- oscilador armónico: un sistema que, al desplazarse de su posición de equilibrio, experimenta una fuerza restauradora\(\mathbf{F}\) proporcional al desplazamiento x
- difracción: La flexión de una onda alrededor de los bordes de una abertura o un obstáculo.
- relatividad especial: Una teoría que (descuidando los efectos de la gravedad) reconcilia el principio de relatividad con la observación de que la velocidad de la luz es constante en todos los marcos de referencia.
- dualidad onda-partícula: Una postulación en la que todas las partículas presentan propiedades tanto de onda como de partícula. Es un concepto central de la mecánica cuántica.
- onda de materia: Un concepto refleja la dualidad onda-partícula de la materia. La teoría fue propuesta por Louis de Broglie.
- Criterio de Rayleigh: La resolución angular de un sistema óptico puede estimarse a partir del diámetro de la abertura y la longitud de onda de la luz, la cual fue propuesta por primera vez por Lord Rayleigh.
- función de densidad de probabilidad: Cualquier función cuya integral sobre un conjunto da la probabilidad de que una variable aleatoria tenga un valor en ese conjunto.
- Teorema de Bell: Teorema no-go famoso por trazar una línea importante en la arena entre la mecánica cuántica (QM) y el mundo tal como lo conocemos clásicamente. En su forma más simple, el teorema de Bell afirma: Ninguna teoría física de las variables locales ocultas jamás podrá reproducir todas las predicciones de la mecánica cuántica.
- epistemológico: De o perteneciente a la epistemología o teoría del conocimiento, como campo de estudio.
LICENCIAS Y ATRIBUCIONES
CONTENIDO CON LICENCIA CC, COMPARTIDO PREVIAMENTE
- Curación y Revisión. Proporcionado por: Boundless.com. Licencia: CC BY-SA: Atribución-CompartirIgual
CC CONTENIDO LICENCIADO, ATRIBUCIÓN ESPECÍFICA
- fotoelectrón. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Photoelectron. Licencia: CC BY-SA: Atribución-CompartirIgual
- radiación de cuerpo negro. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Black%20Cuerpo%20Radiación. Licencia: CC BY-SA: Atribución-CompartirIgual
- efecto fotoeléctrico. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/photoelectric_effect. Licencia: CC BY-SA: Atribución-CompartirIgual
- Fotoeléctrico effect.svg. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/w/index. php*title=file:photoelectric_effect.svg&page=1. Licencia: CC BY-SA: Atribución-CompartirIgual
- Espectro electromagnético. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Electromagnetic_Spectrum. Licencia: CC BY-SA: Atribución-CompartirIgual
- Ecuaciones de Maxwell. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Maxwellu2019s%20Ecuaciones. Licencia: CC BY-SA: Atribución-CompartirIgual
- Constante de Planck. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Planck%20Constant. Licencia: CC BY-SA: Atribución-CompartirIgual
- partícula elemental. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Elementary%20Particle. Licencia: CC BY-SA: Atribución-CompartirIgual
- Fotón. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Photon. Licencia: CC BY-SA: Atribución-CompartirIgual
- radiación de cuerpo negro. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Black%20Cuerpo%20Radiación. Licencia: CC BY-SA: Atribución-CompartirIgual
- Láser militar experiment.jpg. Proporcionado por: Wikimedia. Ubicado en: http://upload.wikimedia.org/Wikipedia/commons/a/a0/Military_laser_experiment.jpg. Licencia: CC BY: Atribución
- teoría de cuerdas. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/String%20Theory. Licencia: CC BY-SA: Atribución-CompartirIgual
- criptografía. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Criptografía. Licencia: CC BY-SA: Atribución-CompartirIgual
- Mecánica cuántica. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Quantum_Mechanics%23Applications. Licencia: CC BY-SA: Atribución-CompartirIgual
- mecánica cuántica relativista. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Relativistica%20Quantum%20Mecánica. Licencia: CC BY-SA: Atribución-CompartirIgual
- Láser. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Laser. Licencia: CC BY: Atribución
- Onda de partículas. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Particle_wave. Licencia: CC BY-SA: Atribución-CompartirIgual
- Interpretación de Copenhague. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Copenhagen_interpretation. Licencia: CC BY-SA: Atribución-CompartirIgual
- efectos fotoeléctricos. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/PhotoElectric%20Effects. Licencia: CC BY-SA: Atribución-CompartirIgual
- Difracción eléctrica. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Difracción_electrónica. Licencia: CC BY-SA: Atribución-CompartirIgual
- reja. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Grating. Licencia: CC BY-SA: Atribución-CompartirIgual
- Difracción eléctrica. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Difracción_electrónica. Licencia: CC BY-SA: Atribución-CompartirIgual
- Gabriela Escalera, Andrew Barron, Difracción de Neutrones. 17 de septiembre de 2013. Proporcionado por: OpenStax CNX. Ubicado en: http://cnx.org/content/m43582/latest/. Licencia: CC BY: Atribución
- Ecuación de Schrodinger. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Schrodinger%20Ecuación. Licencia: CC BY-SA: Atribución-CompartirIgual
- oscilador armónico. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Harmonic%20oscilador. Licencia: CC BY-SA: Atribución-CompartirIgual
- Función de onda. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Wave_Function%23Requirements. Licencia: CC BY-SA: Atribución-CompartirIgual
- dualidad onda-partícula. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Wave-Particle%20Dualidad. Licencia: CC BY-SA: Atribución-CompartirIgual
- De Broglie longitud de onda. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/de_Broglie_Wavelength. Licencia: CC BY-SA: Atribución-CompartirIgual
- especial relativamente. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/special_relativity. Licencia: CC BY-SA: Atribución-CompartirIgual
- difracción. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/diffraction. Licencia: CC BY-SA: Atribución-CompartirIgual
- Principio de incertidumbre. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wikiUncertainty _principle. Licencia: CC BY-SA: Atribución-CompartirIgual
- Criterio de Rayleigh. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Rayleigh%20Criterio. Licencia: CC BY-SA: Atribución-CompartirIgual
- Microscopio de Heisenberg. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Heisenbergu2019s_Microscope. Licencia: CC BY-SA: Atribución-CompartirIgual
- onda de materia. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Matter%20Wave. Licencia: CC BY-SA: Atribución-CompartirIgual
- Microscopio de Heisenberg. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Heisenbergu2019s_Microscope. Licencia: CC BY: Atribución
- Teorema de Bell. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Bellu2019s%20Teorema. Licencia: CC BY-SA: Atribución-CompartirIgual
- función de densidad de probabilidad. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/probability_density_function. Licencia: CC BY-SA: Atribución-CompartirIgual
- epistemológico. Proporcionado por: Wikcionario. Ubicado en: es.wiktionary.org/wiki/epistemológico. Licencia: CC BY-SA: Atribución-CompartirIgual
- Debates de Bohr—Einstein. Proporcionado por: Wikipedia. Ubicado en: es.wikipedia.org/wiki/Bohr%e 2% 80% 93Einstein_debates. Licencia: CC BY: Atribución

