6.2: Semiconductores y Diagramas de Nivel de Energía
- Page ID
- 81916
Definiciones de semiconductores
Algunos semiconductores están formados por átomos de un solo tipo como Si puro o Ge puro. Otros contienen una combinación de elementos en la columna 13 y la columna 15 de la tabla periódica. Los semiconductores de este tipo incluyen AlAs, AlSb, GaAs e InP. Otros semiconductores contienen una combinación de elementos en las columnas 12 y 16 de la tabla periódica. Ejemplos de este tipo incluyen ZnTe, CdSe y ZnS [9]. La mayoría de los semiconductores involucran elementos ubicados en algún lugar cerca del silicio en la tabla periódica, pero también son posibles composiciones y estructuras más complicadas. Los materiales hechos de tres elementos diferentes de la tabla periódica se denominan compuestos ternarios, y los materiales hechos de cuatro elementos se denominan compuestos cuaternarios.
Para entender el funcionamiento de dispositivos como células solares, fotodetectores y ledes, necesitamos estudiar el flujo de cargas en semiconductores. Las propiedades eléctricas en los semiconductores están determinadas por el flujo tanto de electrones de valencia como de agujeros. Los electrones de valencia, a diferencia de los electrones de la capa interna, son los electrones más fácilmente arrancados de un átomo. Un agujero es la ausencia de un electrón. Los electrones y agujeros de valencia se conocen como portadores de carga porque están cargados y se mueven a través del semiconductor cuando se aplica una tensión externa. A una temperatura finita, los electrones están continuamente en movimiento, y algunos pares electrón-agujero pueden formar un excitón. Estos pares electrón-agujero se combinan naturalmente, también llamados decaimiento, en poco tiempo. Sin embargo, en cualquier momento, algunos portadores de carga están presentes en semiconductores a temperaturas superiores al cero absoluto debido al movimiento de las cargas.
Los semiconductores cristalinos pueden clasificarse como intrínsecos o extrínsecos [9, p. 65]. Un cristal semiconductor intrínseco es un cristal sin defectos de celosía o impurezas. A cero absoluto,\(T = 0\) K, un semiconductor intrínseco no tiene electrones libres ni agujeros. Todos los electrones de valencia están involucrados en enlaces químicos, y no hay agujeros. A temperatura finita, algunos portadores de carga están presentes debido al movimiento de electrones a temperatura finita. La concentración de estos portadores de carga se mide en unidades\(\frac{electrons}{m^3}\),\(\frac{holes}{m^3}\),\(\frac{electrons}{cm^3}\) o\(\frac{holes}{cm^3}\). La concentración intrínseca del portador es la densidad de electrones en un semiconductor puro, y es una función de la temperatura\(T\). A temperaturas más altas, estarán presentes más portadores de carga incluso si no hay impurezas o defectos en el semiconductor cristalino debido al mayor movimiento de las cargas. Si aplicamos un voltaje a través de un semiconductor intrínseco a\(T = 0\) K, no fluyen cargas. Cuando la concentración de equilibrio de electrones\(n\) o agujeros\(p\) es diferente de la concentración intrínseca del portador\(n_i\) entonces decimos que el semiconductor es extrínseco. Si están presentes impurezas o defectos cristalinos, el material será extrínseco. Si se aplica un voltaje a través de un semiconductor extrínseco a\(T = 0\) K, las cargas fluirán. Si se aplica un voltaje a través de un semiconductor extrínseco o intrínseco a temperaturas superiores a cero absoluto, los portadores de carga estarán presentes y fluirán.
El proceso de introducir más electrones o agujeros en un semiconductor se llama dopaje. Un semiconductor con un exceso de electrones en comparación con un semiconductor intrínseco se llama tipo n. Un semiconductor con exceso de agujeros se llama tipo p. El silicio típicamente tiene cuatro electrones de valencia que están involucrados en la unión. El fósforo tiene cinco electrones de valencia, y el aluminio tiene tres. Cuando un átomo de fósforo reemplaza a un átomo de silicio en un cristal de silicio, se le llama donante porque dona un electrón. Cuando un átomo de aluminio reemplaza a un átomo de silicio, se le llama aceptor. Los elementos de la columna 15 son donantes al silicio y los elementos de la columna 13 son aceptores. Si el silicio es una impureza en AlP, puede actuar como donador o aceptor. Si reemplaza un átomo de aluminio, actúa como donante. Si reemplaza a un átomo de fósforo, actúa como aceptor.
¿Cómo podemos dopar un trozo de silicio? Más específicamente, ¿cómo podemos dopar un semiconductor con boro? El boro se vende en algunas ferreterías. A veces se usa como ingrediente en el jabón. Comience con una oblea de silicio y elimine cualquier óxido que se haya formado en la superficie. Cada átomo de silicio forma enlaces con cuatro vecinos más cercanos. Sin embargo, en la superficie no hay un cuarto vecino, por lo que los átomos de silicio se unen con el oxígeno del aire. Unte algo de boro sobre la oblea o coloque un pedazo de boro encima de la oblea. Colóquelo en un horno a un poco menos de la temperatura de fusión del silicio, alrededor\(1000 ^{\circ}C\). Algo de boro se difundirá y reemplazará a los átomos de silicio. Eliminar el exceso de boro. El mismo procedimiento se puede utilizar para dopar con otros donantes o aceptores. ¿Cuál es la parte más peligrosa del proceso? Grabar el óxido del silicio porque se usa ácido fluorhídrico HF, un ácido peligroso [69].
A veces es posible hacer crecer una capa de un material semiconductor encima de una capa de un tipo diferente de material. Una pila de diferentes semiconductores uno encima del otro se llama heteroestructura. No todos los materiales se pueden convertir en heteroestructuras. Los GaAs y los ALAs tienen casi los mismos espaciamientos atómicos, por lo que se pueden formar heteroestructuras de estos materiales. El espaciamiento entre átomos, también llamado constante de retícula, en ALA es de 0.546 nm, y el espaciamiento entre átomos en GaAs es de 0.545 nm [9]. Si el espaciamiento atómico en los dos materiales es demasiado diferente, la tensión mecánica en el material resultante lo separará. Incluso la tensión mecánica moderada puede afectar negativamente las propiedades ópticas de un dispositivo porque se pueden introducir defectos en la interfaz entre los materiales. Estos defectos pueden introducir niveles de energía adicionales que pueden atrapar a los portadores de carga.
Niveles de Energía en Átomos Aislados y en Semiconductores
En una célula solar, la luz que brilla sobre un semiconductor hace que los electrones fluyan, lo que permite que el dispositivo convierta la luz en electricidad. ¿Cuánta energía se necesita para hacer que fluya un electrón en un semiconductor? Para responder a esta pregunta, veremos los niveles de energía de:
- Un átomo de Al aislado en\(T = 0\) K
- Un átomo de P aislado en\(T = 0\) K
- Átomo de Al aislado y átomos de P en\(T > 0\)
- Un cristal de AlP a\(T = 0\) K
- Un cristal de AlP a\(T > 0\) K
El aluminio tiene una configuración electrónica de\(1s^22s^22p^63s^23p^1\). Tiene 13 electrones totales, y tiene 3 electrones de valencia. Más específicamente, tiene dos electrones de valencia en la\(3s\) subcapa y uno en la\(3p\) subcapa. El fósforo tiene una configuración electrónica de\(1s^22s^22p^63s^23p^3\), por lo que tiene 5 electrones de valencia. Las ideas de esta sección se aplican a los materiales independientemente de que sean cristalinos, amorfos o policristalinos.
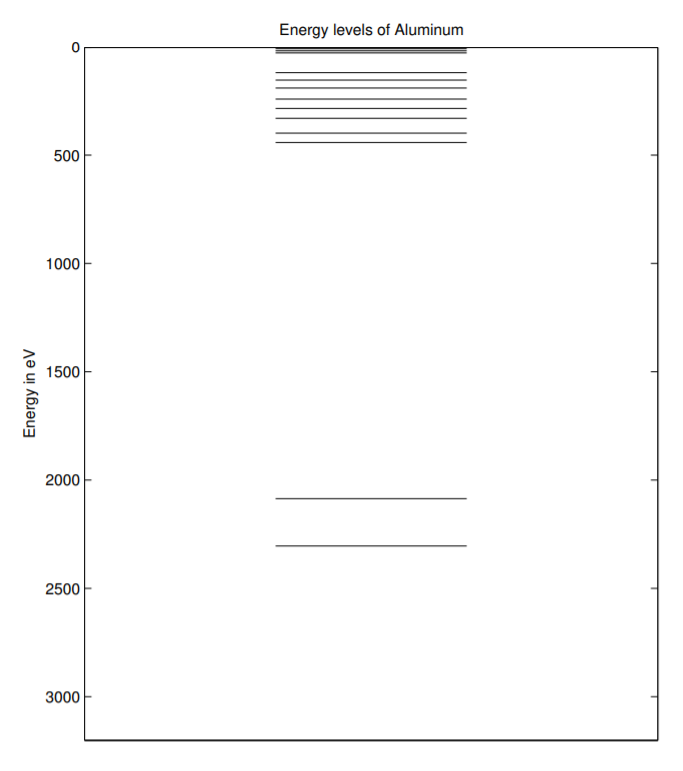
Niveles de energía de electrones de átomos de Al aislados y P aislados a\(T = 0\) K
Para entender la interacción de la luz y un semiconductor, comience por considerar un átomo de Al aislado y un átomo de P aislado en cero absoluto,\(T = 0\) K. ¿Cuánta energía se necesita para estafar electrones de Al? Se necesita significativamente menos energía para arrancar un electrón de valencia que un electrón de una capa interna. De hecho, cuando decimos que un electrón es un electrón de valencia, o un electrón está en una concha de valencia, queremos decir que el electrón está en la concha para la cual toma la menor energía para arrancar un electrón. No queremos decir que el electrón esté más lejos del núcleo, aunque muchas veces lo es. Cuando decimos que un electrón está en una capa interna, queremos decir que el electrón está en una concha para la cual se necesita más energía para arrancar un electrón. Este texto se centra en los dispositivos de conversión de energía que operan a energías moderadas, por lo que todos los dispositivos discutidos involucran interacciones de solo electrones de valencia. Los electrones de la capa interna no estarán involucrados. También es posible excitar, pero no estafar, a un electrón. Cuando un electrón es excitado, su impulso interno cambia y sus números cuánticos cambian. Los términos electrón de valencia y número cuántico se definieron en la Sec. 1.5.2. Se requiere menos energía para excitar que arrancar un electrón. La energía requerida para excitar o arrancar electrones puede ser suministrada por energía térmica, un voltaje externo, un campo óptico externo u otras fuentes externas.
La figura\(\PageIndex{1}\) es una gráfica de la energía requerida para excitar o eliminar electrones de un átomo de Al neutro aislado en\(T = 0\) K. La figura se trazó usando datos de [70]. Si bien los niveles de energía se dibujan usando datos reales, el grosor de las líneas no se dibuja a escala. La energía está en el eje vertical. Los niveles de energía permitidos se muestran mediante líneas horizontales. Cada electrón solo puede tener energía correspondiente a uno de estos niveles discretos de energía posibles. A\(T = 0\) K, los electrones ocupan los niveles de energía más bajos posibles. Un electrón puede ocupar cada línea, por lo que los 13 niveles de energía más bajos están ocupados por electrones. Si bien no se muestra debido a la resolución de la figura, la densidad de los niveles de energía permitidos aumenta a medida que la energía se acerca a cero en la parte superior de la figura. Dado que estamos considerando el caso de la temperatura cero absoluta, estos niveles superiores de energía no están ocupados por electrones.
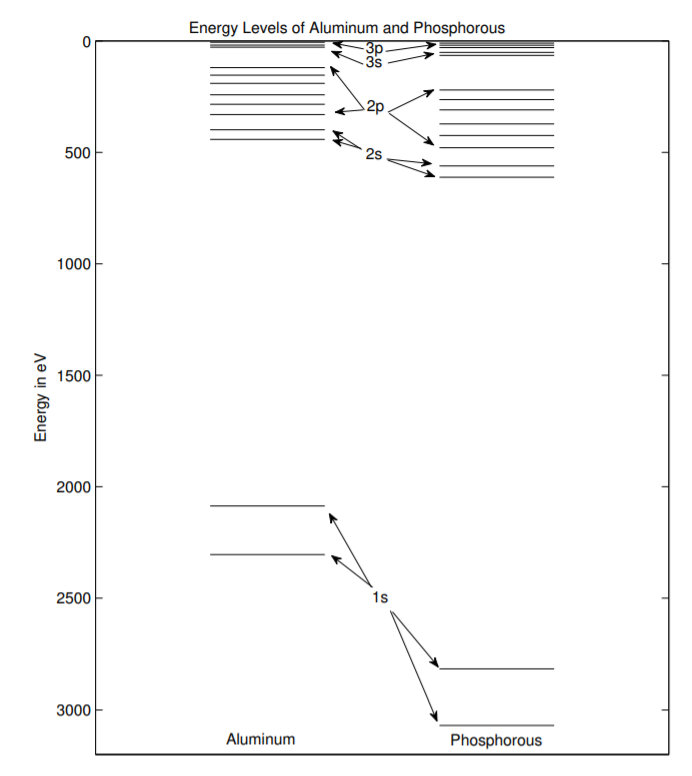
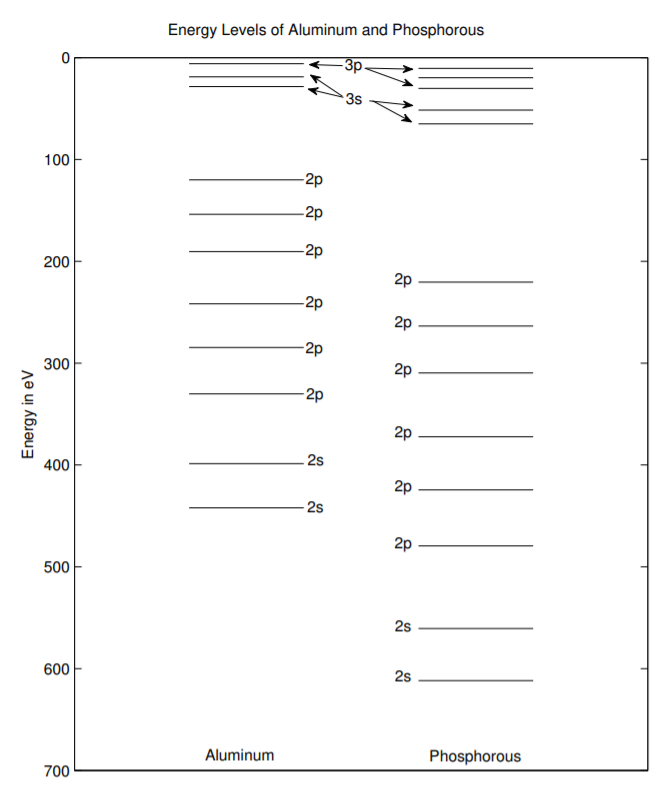
El lado izquierdo de la Fig. \(\PageIndex{2}\)retraza los niveles de energía permitidos de los electrones en un átomo de Al aislado en\(T = 0\) K. Los niveles de energía también están etiquetados. El lado derecho de la figura traza los niveles de energía permitidos de electrones en un átomo de P aislado también en\(T = 0\) K. Los datos sobre los niveles de energía de fósforo también provienen de [70]. Al igual que con el átomo de Al, los electrones del átomo P sólo pueden ocupar ciertos niveles específicos de energía discreta. Dado que los átomos están en cero absoluto, los electrones ocupan los niveles de energía más bajos posibles. La figura\(\PageIndex{3}\) contiene la misma información, pero se amplía verticalmente para mostrar más claramente los niveles de electrones de valencia.
El átomo P tiene dos electrones más que el átomo de Al. Los átomos de fósforo tienen más protones, por lo que los electrones están un poco más unidos al núcleo. Por esta razón, se necesita un poco más de energía para arrancar los electrones, y los niveles de energía permitidos son un poco diferentes a los de Al.
La cantidad de energía requerida para arrancar un\(3p\) electrón del átomo es la distancia vertical desde el\(3p\) nivel hasta la línea de tierra en la parte superior de la figura. La cantidad de energía requerida para arrancar un\(2p\) electrón es la distancia vertical desde el\(2p\) nivel hasta la línea de tierra. Como era de esperar, estas cifras muestran que se requiere más energía para arrancar el electrón de concha interna que el\(2p\) electrón de concha\(3p\) de valencia. Si se suministra suficiente energía, se arrancará un electrón y el electrón fluirá libremente a través del material. Si se suministra algo de energía pero no es suficiente para arrancar el electrón, el electrón puede excitarse a un nivel de energía más alto. La energía requerida para excitar un electrón viene dada por la distancia vertical en la figura de un nivel de energía ocupado a uno desocupado. En cualquier caso, decimos que se forma un par electrón-agujero. Si la cantidad de energía suministrada es demasiado pequeña para excitar un electrón de un estado lleno a no lleno, la energía externa no será absorbida.
Niveles de energía de electrones de átomos de Al aislados y P aislados a\(T > 0\) K
¿Cómo cambian los niveles de energía cuando los átomos de Al y P están a temperaturas superiores al cero absoluto, donde los electrones vibran y se mueven continuamente? Primero, los niveles de energía se amplían. Los electrones todavía solo pueden tomar ciertos niveles de energía, pero hay un rango más amplio para los niveles de energía permitidos. En segundo lugar, ocasionalmente, los electrones se excitan espontáneamente a estados superiores. Por ejemplo, un\(3p\) electrón puede excitarse al\(4s\) estado temporalmente. Si lo hace, volverá rápidamente al estado base.
Niveles de energía de AlP a\(T = 0\) K
¿Cuánta energía se necesita para extraer un electrón de un cristal de AlP a\(T = 0\) K? Los tres electrones de valencia de cada átomo de Al y los cinco electrones de valencia de cada átomo de P forman enlaces químicos. La energía requerida para arrancar estos electrones es ligeramente diferente a la energía requerida para arrancar los electrones equivalentes de los átomos de Al aislados y P aislados. La figura\(\PageIndex{4}\) ilustra los niveles de energía de los electrones de valencia de AlP. A diferencia de las cifras anteriores, estos niveles de energía no provienen de datos reales. En cambio, se entiende como una ilustración aproximada del efecto. La cantidad de energía requerida para arrancar un electrón se representa en el diagrama de nivel de energía por la distancia vertical desde ese nivel hasta el nivel del suelo en la parte superior del diagrama. Las energías necesarias para eliminar los electrones de la capa interna no cambian significativamente de los niveles de energía de los átomos aislados.
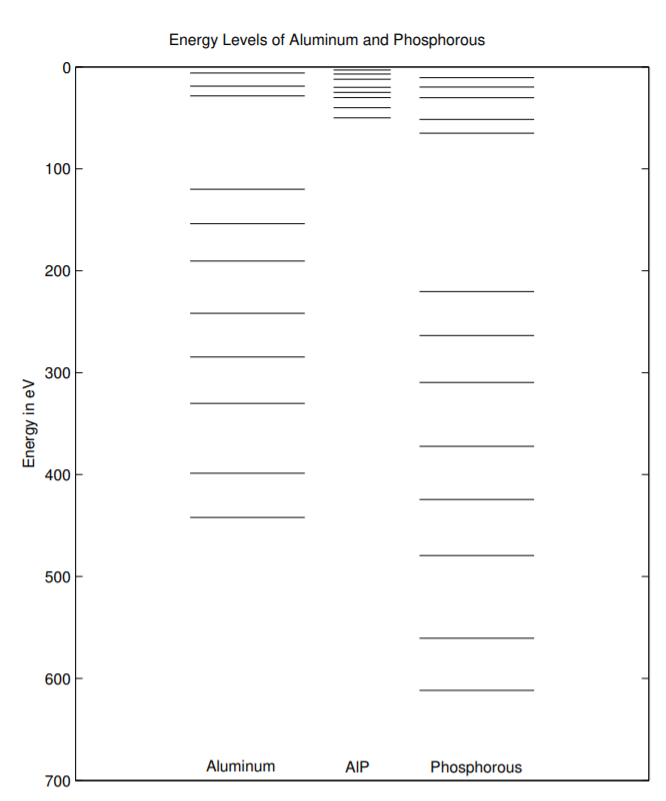
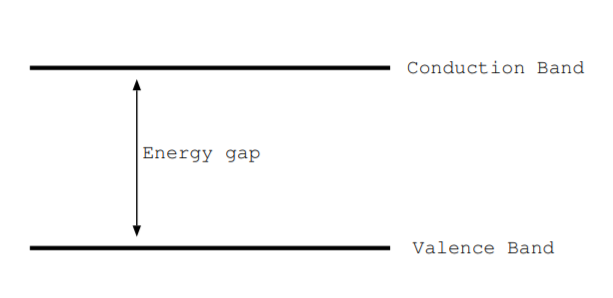
Los niveles de energía debido a los electrones compartidos entre los átomos en un semiconductor sólido se denominan bandas de energía. El nivel de energía lleno más cercano a la parte superior de un diagrama de nivel de energía para un semiconductor se llama banda de valencia. El nivel de energía por encima de él se llama la banda de conducción. La brecha de energía\(E_g\), también llamada banda prohibida, es la diferencia de energía desde la parte superior de la banda de valencia hasta la parte inferior de la banda de conducción. El término electrón de valencia se refiere a un electrón de capa externa mientras que el término banda de valencia se refiere a un posible nivel de energía que pueda ocupar. En\(T = 0\) K, la banda de valencia se llena típicamente, y la banda de conducción puede estar vacía o parcialmente vacía. A menudo solo nos interesan las bandas de valencia y conducción porque nos interesan los procesos de conversión de energía que involucran pequeñas cantidades de energía. Por esta razón, a menudo trazamos diagramas de nivel de energía ampliados verticalmente para mostrar solo estos dos niveles de energía como se muestra en la Fig. \(\PageIndex{5}\).
Si el cristal de AlP tiene defectos o impurezas, los niveles de energía se amplían un poco porque el potencial eléctrico (en voltios) visto por cada átomo de Al y cada P es ligeramente diferente del potencial visto por otros átomos de Al y P en el cristal. Por lo tanto, se necesitan cantidades de energía ligeramente diferentes para arrancar cada electrón. Por esta razón, los niveles de energía en los materiales amorfos son bastante más amplios que los niveles de energía en cristales de la misma composición [10]. Si el cristal de AlP tiene defectos o impurezas, pueden estar presentes niveles de energía adicionales permitidos. Algunos de estos niveles de energía pueden incluso caer dentro de la brecha energética.
Niveles de energía de AlP a\(T > 0\) K
Al igual que con los átomos aislados, existen dos diferencias entre los niveles de energía para cristales como AlP a\(T > 0\) K en comparación con K en comparación con\(T = 0\) K. Primero, los niveles de energía se amplían. Segundo, algunos electrones se excitan a niveles de energía más altos y rápidamente, tal vez en unos microsegundos, vuelven a caer.
Definiciones de conductores, dieléctricos y semiconductores
Los conductores, dieléctricos y semiconductores se definieron en la sección 1.5.1. Ahora que hemos visto ejemplos de diagramas de nivel de energía, deberíamos revisar estas definiciones así como definir el término semimetal. En presencia de una tensión externa aplicada, campo eléctrico, campo óptico u otra fuente de energía, los electrones de valencia fluyen fácilmente en un conductor [10, p. 429] [11, ch. 4]. En un conductor, la banda de conducción está parcialmente llena de electrones, por lo que hay muchos estados de energía disponibles para los electrones que permanecen en la banda de conducción. Con solo un poco de energía externa, posiblemente incluso de vibraciones que ocurren naturalmente en\(T > 0\) K, los electrones de valencia fluyen fácilmente. Los electrones de la capa interna pueden ser arrancados de sus átomos y flujo, pero se necesita significativamente más energía para arrancar la capa interna que los electrones de valencia.
En presencia de una tensión externa aplicada, campo eléctrico, campo óptico u otra fuente de energía, los electrones no fluyen fácilmente en un aislante [10, p. 429] [11, ch. 4]. La banda de valencia está llena y la banda de conducción está vacía. La brecha de energía entre la banda de valencia y la banda de conducción en un aislante es típicamente superior a 3 eV. Un poco de calor o energía de las vibraciones no es suficiente para excitar un electrón de un estado energético permitido a otro. Sin embargo, si se aplica una fuente externa de energía lo suficientemente grande, un electrón puede ser excitado o arrancado de un aislante.
En la Sec. 3.3, se discutieron los materiales electro-ópticos. Algunos aisladores son electro-ópticos lo que significa que en presencia de un campo eléctrico u óptico externo, la distribución espacial de los electrones cambia ligeramente lo que provoca que se acumule una polarización material. Los fotones del campo eléctrico u óptico externo en este caso no tienen suficiente energía para excitar electrones en el aislador, por lo que el impulso interno de los electrones en el material no cambia. El efecto electro-óptico ocurre en aisladores e involucra energías externas demasiado pequeñas para excitar electrones de un estado de energía permitido a otro, mientras que los efectos discutidos en la Sec. 6.2 involucran semiconductores y energías externas lo suficientemente grandes como para excitar electrones de un nivel de energía a otro.
A\(T = 0\) K en un semiconductor, la banda de valencia está llena y la banda de conducción está vacía. La brecha de energía de un semiconductor es pequeña, en el rango\(0.5 eV \lesssim E_g \lesssim 3 eV\). En presencia de un pequeño voltaje aplicado, campo eléctrico o campo óptico, un semiconductor actúa como aislante. En presencia de una gran tensión aplicada u otra fuente de energía, un semiconductor actúa como conductor y los electrones fluyen. Los fotodiodos y las células solares están hechos de semiconductores. Si se suministra suficiente energía a un fotodiodo, por ejemplo desde un haz óptico, fluirán los electrones de valencia. Más específicamente, los fotones del haz óptico externo deben tener más energía que la brecha de energía del semiconductor para que fluyan los electrones de valencia.
El término semimetal se utiliza para describir conductores con baja concentración de electrones. Similar a los conductores, en un semimetal a\(T = 0\) K, no hay brecha de energía porque la banda de conducción está parcialmente llena de electrones, y hay muchos estados de energía disponibles. La concentración de electrones para semimetales, sin embargo, está en el rango\(n < 10^{22} \frac{electrons}{cm^3}\) mientras que\(n\) es mayor para los conductores [26, p. 304].
¿Por qué las células solares y los fotodetectores están hechos de semiconductores?
Los diagramas de nivel de energía para AlP fueron ilustrados arriba. La brecha energética de AlP es\(E_g = 2.45 eV\), por lo que es un semiconductor [9] [10, p. 432,543]. Si\(E < 2.45 eV\) se aplica un haz de luz con fotones de energía a una pieza de AlP, los fotones no serán absorbidos, y no se excitarán electrones. Si se aplica un haz de luz con fotones de energía\(E \geq 2.45 eV\) a una pieza de AlP, algunos de esos fotones pueden ser absorbidos. Cuando se absorbe un fotón, un electrón se excitará de la banda de valencia a la banda de conducción. Un fotón azul con energía\(E = 3.1 eV\) será absorbido por AlP, por ejemplo, pero un fotón rojo con energía no\(E = 1.9 eV\) lo hará. Cuando el electrón es excitado, el impulso interno del electrón necesariamente cambia. El electrón excitado rápidamente decae espontáneamente de nuevo a su estado de energía más bajo, y puede emitir un fotón o un fonón en el proceso. Si se aplica un haz de luz con fotones de energía significativamente mayor a una pieza de AlP, es posible arrancar electrones completamente de su átomo.
¿Por qué las células solares y los fotodetectores ópticos están hechos de semiconductores en lugar de aisladores? La luz solar se compone de luz a múltiples longitudes de onda, y es más intensa en longitudes de onda que corresponden a la luz amarilla y verde. Los fotones verdes tienen energías cercanas\(E \approx 2.2 eV\), y los fotones visibles tienen energías en el rango\(1.9 eV < E < 3.1 eV\). Las células solares están hechas de materiales con una brecha de energía menor que la energía de la mayoría de los fotones de la luz solar. Se utilizan semiconductores porque la energía de cada fotón es lo suficientemente grande como para excitar los electrones en el material. No se utilizan aisladores porque la mayoría de los fotones de luz visible no tienen suficiente energía para excitar electrones en el material. El material no debe tener una brecha de energía que sea demasiado grande de lo contrario los fotones no serán absorbidos.
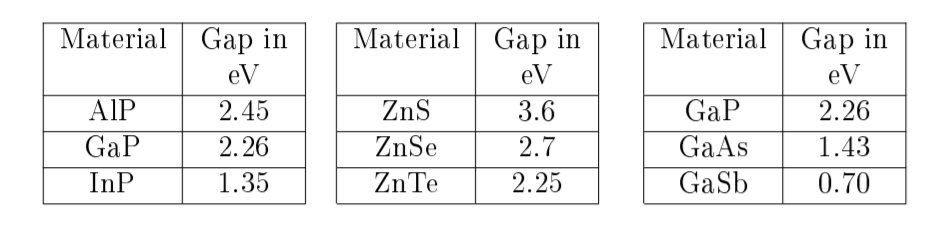
Tabla\(\PageIndex{1}\): Brecha de energía de varios semiconductores.
¿Por qué las células solares y los fotodetectores ópticos están hechos de semiconductores en lugar de conductores? Cuando la luz brilla sobre una célula solar o fotodetector, los fotones de luz son absorbidos por el material. Si el fotón absorbido tiene una energía mayor que la brecha de energía del material, el electrón decae rápidamente a la parte superior de la banda de conducción. Con algo más de tiempo, decae de nuevo al estado energético más bajo. En una célula solar o fotodetector, se utiliza una unión pn para hacer que los electrones fluyan antes de decaer de nuevo al estado fundamental. La cantidad de energía convertida en electricidad por electrón excitado depende de la brecha de energía del material, no de la energía del fotón entrante. Solo la energía\(E_g\) por fotón absorbido se convierte en electricidad independientemente de la energía original del fotón. Así, la brecha de energía del material utilizado para hacer una célula solar o fotodetector debe ser grande para que la mayor cantidad de energía por electrón excitado se convierta en electricidad como sea posible. El material no debe tener una brecha energética que sea demasiado pequeña de lo contrario muy poca energía se convertirá en electricidad. El electrón y el agujero liberarán el exceso de energía\(hf - E_g\),, rápidamente en forma de vibraciones de calor o celosía llamadas fonones.
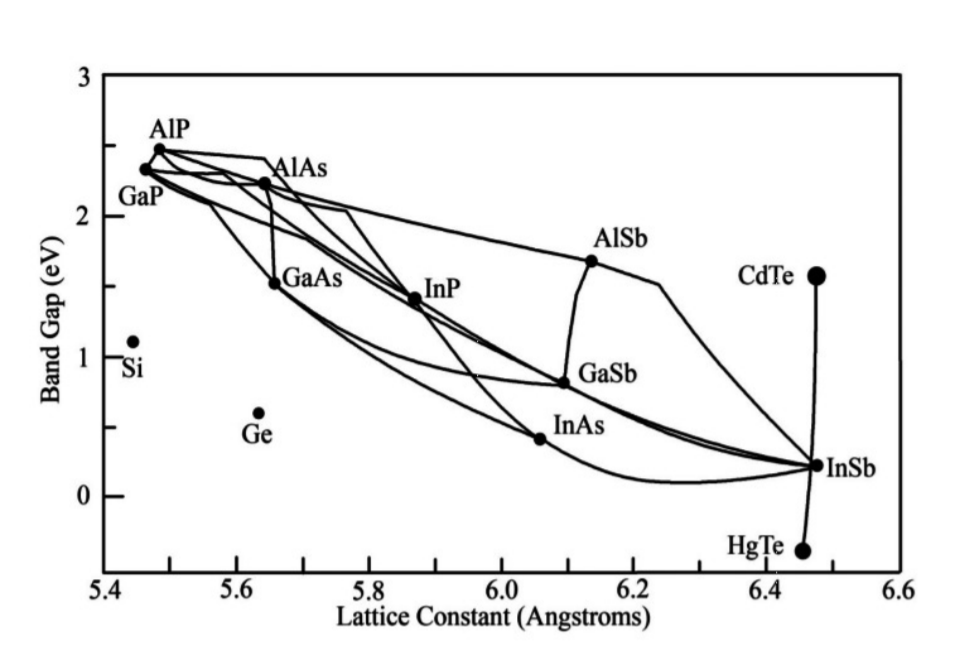
Cada semiconductor tiene una brecha de energía diferente\(E_g\). Muchas células solares y fotodetectores están hechos de silicio, que es un semiconductor con\(E_g = 1.1 eV\). Predecir la brecha de energía de un material es bastante difícil. Sin embargo, todo lo demás igual, si un elemento de un semiconductor es reemplazado por uno debajo de él en la tabla periódica, la brecha de energía tiende a hacerse más pequeña. Esta tendencia se ilustra en la Tabla\(\PageIndex{1}\). Los datos para la tabla provienen de [9]. Esta tendencia también se ilustra en la Fig. \(\PageIndex{6}\), que traza la brecha de energía y la constante de celosía para diversos semiconductores. La figura\(\PageIndex{6}\) se toma de la referencia [71]. El eje horizontal representa el espaciado interatómico en unidades de angstroms, donde un angstrom equivale a\(10^{10}\) metros. El eje vertical representa la brecha de energía en eV. Esta figura ilustra huecos de energía y constantes de celosía para materiales de una amplia gama de composiciones. Por ejemplo, la brecha de energía para el fosfuro de aluminio se puede encontrar desde el punto etiquetado AlP, y la brecha de energía del arseniuro de aluminio se puede encontrar desde el punto etiquetado AlAs. La brecha de energía para semiconductores de composición se\(\text{AlAs}_xP_{1−x}\) puede encontrar a partir de la línea entre estos puntos.
Algunas células solares están hechas de material en capas con el material de brecha de energía más grande en la parte superior. Por ejemplo, una célula solar podría estar hecha de una capa superior de ZnS, una capa media de ZnSe y una capa inferior de ZnTe. Los fotones con energía\(E > 3.6 eV\) serían absorbidos en la capa de ZnS. Los fotones con energía\(2.7 eV< E <3.6 eV\) serían absorbidos por la capa de ZnSe, y los fotones con energía\(2.25 eV< E <2.7 eV\) serían absorbidos por la capa de ZnTe. Cada fotón de energía absorbida por la capa de ZnS y convertida en electricidad tendría más energía que cada fotón absorbido por la capa de ZnSe. Las células solares hechas de capas de esta manera pueden ser más eficientes para convertir energía de energía óptica a electricidad que las células solares equivalentes hechas de un solo material.
La foto en la Fig. \(\PageIndex{7}\)muestra sulfuro de zinc natural, también llamado esfalerita, recolectado cerca de la tienda Sheffler's Rock cerca de Alexandria, Missouri. El mineral oscuro incrustado en el medio de la roca es la esfalerita.

Distribución de energía electrónica
El nivel de energía Fermi de un semiconductor, denotado\(E_f\), representa el nivel de energía en el que la probabilidad de encontrar un electrón es la mitad [9] [10, p. 432,543]. El nivel de Fermi depende de la temperatura, y depende de las impurezas en el semiconductor. Los químicos alguna vez llaman al nivel Fermi por el nombre potencial químico,\(\mu_{chem}\).
En un semiconductor puro a\(T = 0 \) K, todos los electrones ocupan los estados más bajos posibles. La banda de valencia está completamente llena, y la banda de conducción está completamente vacía. El nivel Fermi,\(E_f\), es el nivel de energía en la mitad de la brecha energética. No se encuentran electrones en la energía\(E_f\) porque ningún electrón puede tener una energía dentro de la brecha de energía. Sin embargo, el nivel de Fermi es una medida útil para describir el material.
En un semiconductor puro a\(T > 0\) K, algunos electrones se excitan en niveles de energía más altos. A medida que aumenta la temperatura, es probable que se encuentren más electrones en niveles de energía más altos con mayor frecuencia. La probabilidad de que un electrón esté en nivel de energía\(E\) varía con la temperatura como\(e^{-E/k_BT}\) [9] [10]. La cantidad\(kB\) es la constante de Boltzmann.
\[k_B = 1.381 \cdot 10^{-23}\frac{J}{K} = 8.617 \cdot 10^{-5} \frac{eV}{K} \nonumber \]
El nivel de Fermi para un material con\(T > 0\) K es ligeramente superior al nivel de Fermi para un material con\(T = 0\) K porque es probable que se exciten más electrones.
La probabilidad de encontrar un electrón a nivel de energía\(E\) a temperatura\(T\) es
\[F(E,T) = \frac{1}{1 + e^{(E-E_f)/k_BT}}. \label{6.2.2} \]
La ecuación\ ref {6.2.2} se llama la distribución de Fermi Dirac, y como cualquier probabilidad, varía\(0 \leq F \leq 1\). Para niveles de energía muy por encima de la banda de conducción, (\(E − E_f\)) es grande y positivo, por lo que es muy poco probable que se encuentren electrones,\(F \approx 0\). Para los niveles de energía muy por debajo de la banda de valencia, (\(E − E_f\)) es grande y negativo, por lo que es muy probable que se encuentren electrones,\(F \approx 1\).
La concentración y el tipo de impurezas influyen en la energía del nivel de Fermi. Un material tipo p tiene una falta de electrones. Por esta razón en un material tipo p,\(E_f\) está más cerca de la banda de valencia que a la mitad de la brecha de energía. Un material tipo n tiene un exceso de electrones. Por esta razón en un material tipo n,\(E_f\) está más cerca de la banda de conducción.


