1.2: Energía de biogás a partir de desechos orgánicos
- Page ID
- 80974
Hamed El Mashad
Departamento de Ingeniería Biológica y Agropecuaria
Universidad de California, Davis
Davis, CA, Estados Unidos
y
Departamento de Ingeniería Agropecuaria
Universidad de Mansoura
El Mansoura, Egipto
Ruihong Zhang
Departamento de Ingeniería Biológica y Agropecuaria
Universidad de California, Davis
Davis, CA, Estados Unidos
| Términos Clave |
| Digestores anaerobios | Crecimiento suspendido | Dimensionamiento |
| Procesos bioquímicos y físicos | Limpieza de biogás | Estimación de rendimiento |
| Crecimiento fijo | Mejoramiento de biogás | Usos comerciales |
Variables
Introducción
El combustible fósil es actualmente la principal fuente de energía en el mundo. Con sus limitados suministros y la contaminación ambiental causada por su uso, existe la necesidad de incrementar el uso de energía renovable. Las fuentes de energía renovable incluyen el sol, los vientos, las mareas, las olas, la lluvia, el calor geotérmico y la biomasa. La biomasa es material vegetal o animal que puede ser utilizado para producir bioenergía como calor o combustible. Las tecnologías para convertir la biomasa en bioenergía pueden clasificarse como tecnologías bioquímicas, fisicoquímicas y termoquímicas. Las principales tecnologías bioquímicas incluyen la digestión anaerobia para producir biogás y la fermentación para producir alcoholes como el etanol y el butanol. La principal tecnología fisicoquímica es la transesterificación para producir biodiesel, y las principales tecnologías termoquímicas son la combustión para producir calor, la torrefacción para producir combustibles sólidos, la pirólisis para producir petróleo y la gasificación para producir gas de síntesis. La selección de una tecnología específica depende de la composición de la biomasa disponible, así como de la bioenergía deseada considerando la economía, las implicaciones sociales y el impacto ambiental.
La energía del biogás es producida por la digestión anaeróbica de la materia orgánica, la cual es llevada a cabo por un consorcio de microorganismos en ausencia de oxígeno. Para el proceso se utilizan recipientes herméticos llamados digestores o reactores. El biogás es una mezcla de metano (CH 4), dióxido de carbono (CO 2) y trazas de otros gases, como amoníaco (NH 3) y sulfuro de hidrógeno (H 2 S). La tecnología de digestión anaeróbica se puede utilizar para tratar materiales orgánicos, como residuos de alimentos y aguas residuales, reduciendo así la cantidad de material a desechar, al tiempo que se genera bioenergía.
Este capítulo introduce la producción de biogás mediante digestión anaeróbica de desechos orgánicos (por ejemplo, restos de alimentos, estiércol animal, recortes de pasto y pajitas). Introduce los procesos involucrados en la digestión anaeróbica, los principales factores que influyen en estos procesos, el biogás producido y los tipos comunes de digestores. También presenta métodos para determinar los rendimientos de biogás y metano.
Resultados
Después de leer este capítulo, deberías poder:
- • Explicar los procesos microbiológicos, químicos y físicos en la digestión anaeróbica
- • Describir los tipos de digestores anaerobios utilizados para la producción de biogás y los factores que influyen en su desempeño
- • Describir algunos métodos de limpieza del biogás para la generación de energía
- • Estimar la cantidad de biogás, metano y energía que se puede producir a partir de un material orgánico
- • Calcular el volumen de un digestor para tratar una cierta cantidad de un sustrato
Conceptos
La digestión anaeróbica es un proceso de bioconversión que se lleva a cabo por microorganismos anaerobios incluyendo bacterias anaerobias y arqueas metanogénicas para descomponer y convertir la materia orgánica en biogás, que es principalmente una mezcla de CH 4 y CO 2.
Procesos Bioquímicos
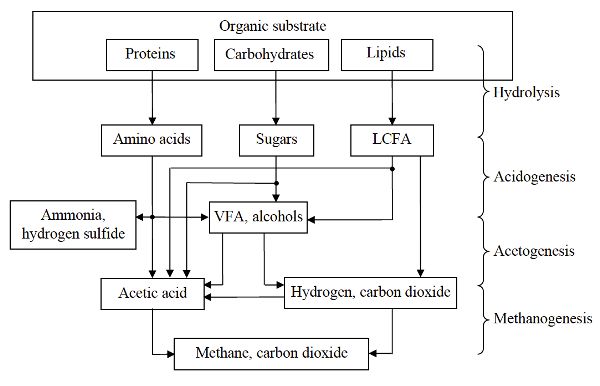
La digestión anaerobia implica cuatro procesos bioquímicos principales: hidrólisis, acidogénesis, acetogénesis y metanogénesis. La figura\(\PageIndex{1}\) muestra estos procesos para la conversión de sustratos orgánicos (como proteínas, carbohidratos y lípidos) en biogás.
La hidrólisis convierte la materia orgánica compleja usando enzimas extracelulares e intracelulares de los microorganismos en componentes monoméricos o diméricos, como aminoácidos, azúcares simples y ácidos grasos de cadena larga (LCFA). Durante la acidogénesis, los productos de hidrólisis son convertidos por bacterias acidógenas en moléculas más pequeñas como ácidos grasos volátiles (VFA), alcoholes, hidrógeno y NH 3. En la acetogénesis, los alcoholes y VFA (distintos del acetato) se convierten en ácido acético o hidrógeno y CO 2. Las bacterias acidógenas y acetogénicas son un grupo diverso de microbios anaerobios facultativos y obligatorios, incluyendo Clostridium, Peptococcus, Bifidobacterium, Corynebacterium, Lactobacillus, Actinomyces, Staphylococcus, Streptococcus, Desulfomonas, Pseudomonas, Selemonas, Micrococcus y Escherichia coli (Kosaric y Blaszczyk, 1992). Durante la metanogénesis, el ácido acético y el metanol (un alcohol) se convierten en CH 4 y CO 2. Además, el CO 2 y el hidrógeno se convierten en CH 4. Las arqueas metanogénicas incluyen un grupo diverso de anaerobios obligados como Methanobacterium formicicum, Methanobrevibacter ruminantium, Methanococcus vannielli, Methanomicrobium mobile, Methanogenium cariaci, Methanospirilum hungatei, y Methanosarcina barkei (Kosaric y Blaszczyk, 1992). En la Tabla se muestran ejemplos de la conversión de compuestos seleccionados durante la digestión anaerobia\(\PageIndex{1}\).
| Subprocesos | Ejemplos |
|---|---|
|
Hidrólisis |
Conversión de carbohidratos y proteínas: \( \text { Cellulose }+\mathrm{H}_{2} \mathrm{O} \rightarrow \text { sugars } \) \( \text { Proteins }+\mathrm{H}_{2} \mathrm{O} \rightarrow \text { amino acids } \) |
|
Acidogénesis |
Conversión de glucosa en ácidos acético y propiónico: \( \mathrm{C}_{6} \mathrm{H}_{12} \mathrm{O}_{6} \rightarrow 3 \mathrm{CH}_{3} \mathrm{COOH} \) \( \mathrm{C}_{6} \mathrm{H}_{12} \mathrm{O}_{6}+2 \mathrm{H}_{2} \rightarrow 2 \mathrm{CH}_{3} \mathrm{CH}_{2} \mathrm{COOH}+2 \mathrm{H}_{2} \mathrm{O} \) |
|
Acetogénesis |
Conversión de propionato y butirato en acetato e hidrógeno como sigue: \( \mathrm{CH}_{3} \mathrm{CH}_{2} \mathrm{COO}^{-}+3 \mathrm{H}_{2} \mathrm{O} \rightarrow \mathrm{CH}_{3} \mathrm{COO}^{-}+\mathrm{HCO}_{3}^{-}+\mathrm{H}^{+}+3 \mathrm{H}_{2} \) \( \mathrm{CH}_{3} \mathrm{CH}_{2} \mathrm{CH}_{2} \mathrm{COO}^{-}+2 \mathrm{H}_{2} \mathrm{O} \rightarrow 2 \mathrm{CH}_{3} \mathrm{COO}^{-}+\mathrm{H}^{+}+2 \mathrm{H}_{2} \) \( 4 \mathrm{H}_{2}+2 \mathrm{HCO}_{3}^{-}+\mathrm{H}^{+} \rightarrow \mathrm{CH}_{3} \mathrm{COO}^{-}+4 \mathrm{H}_{2} \mathrm{O} \) |
|
Metanogénesis |
Conversión de ácido acético, dióxido de carbono e hidrógeno, y metanol a metano: \( 4 \mathrm{CH}_{3} \mathrm{COOH} \rightarrow 4 \mathrm{CO}_{2}+4 \mathrm{CH}_{4} \) \( \mathrm{CO}_{2}+4 \mathrm{H}_{2} \rightarrow \mathrm{CH}_{4}+2 \mathrm{H}_{2} \mathrm{O} \) \( 4 \mathrm{CH}_{3} \mathrm{OH}+6 \mathrm{H}_{2} \rightarrow 3 \mathrm{CH}_{4}+2 \mathrm{H}_{2} \mathrm{O} \) |
Tipos de Digestores Anaerobios
Los digestores anaeróbicos se pueden clasificar en función de cómo interactúan los microorganismos dentro del digestor con el sustrato. Se utilizan tres atributos: (1) cómo se cultivan los microorganismos: crecimiento suspendido o crecimiento fijo, (2) la alimentación del sustrato en el recipiente como un lote, un tapón, o continuamente y (3) el número de etapas, individuales o multietapas. Otras consideraciones de diseño son si los contenidos se mezclan activamente, si la orientación es predominantemente vertical u horizontal, y si el flujo a través del recipiente es hacia abajo o hacia arriba.
Digestores anaerobios de crecimiento suspendido
Los digestores de crecimiento suspendido se utilizan generalmente para sustratos con un alto contenido de sólidos suspendidos, como aguas residuales municipales y desechos sólidos diluidos. Se pueden operar como un proceso discontinuo (Figura\(\PageIndex{2}\)) o como flujo de tapón (Figura\(\PageIndex{3}\)), donde un lote de sustrato se mueve a través del recipiente como un bloque de material, llamado tapón. Los microorganismos se dispersan por todo el reactor cuando se mezclan los contenidos del digestor, tales como reactores de tanque agitado continuo (CSTR), o reactor de contacto anaeróbico (ACR) que es un CSTR con sólidos efluentes reciclados de un tanque de sedimentación para sólidos. En un CSTR, el tiempo de retención de sólidos (SRT) es igual al tiempo de retención hidráulica (HRT), que es el tiempo promedio que los sólidos y el líquido permanecen en el recipiente del biorreactor. Los sistemas CSTR son operados en HRT y SRT que van de 10 a 30 días. El ACR tiene un SRT más largo (>50 días) que el HRT (0.5—5 días) debido a que parte de los sólidos efluentes se recicla de nuevo al digestor.
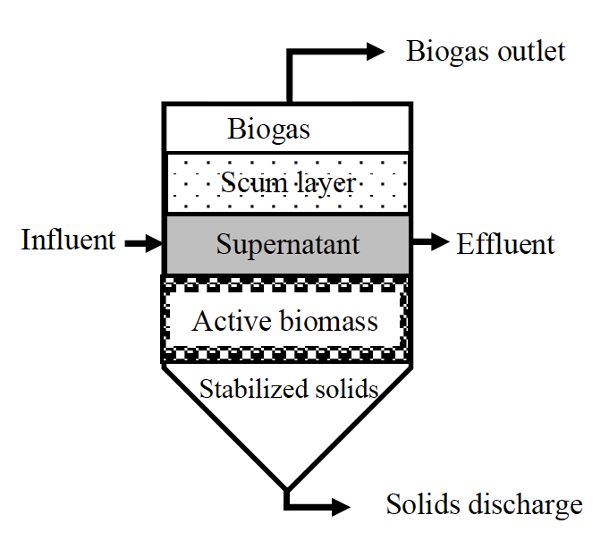
La Figura\(\PageIndex{2}\) muestra un esquema de un digestor anaerobio por lotes de crecimiento suspendido. Estos son simples de diseñar y operar. Por lo general, son un recipiente hermético con puertos de entrada y salida para suministrar sustrato fresco y eliminar sustrato gastado, un puerto de salida de biogás y un puerto para eliminar sólidos. Estos sistemas son comúnmente desplegados a pequeña escala y para probar la biodegradabilidad anaeróbica de diferentes materiales. La operación comienza mezclando una cantidad fija de sustrato con inóculo, que es cultivo bacteriano activo tomado directamente de un reactor en funcionamiento. Posteriormente, se mantienen las condiciones anaeróbicas para el tiempo de digestión (es decir, el tiempo de retención), lo que debería asegurar el agotamiento de todo el sustrato disponible.
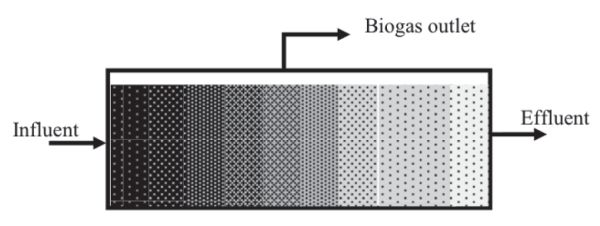
El CSTR se utiliza típicamente para tratar desechos agrícolas y municipales con un contenido total de sólidos (TS) de 3% a 12%. Por lo general, se operan a temperaturas controladas, por lo que el buque, construido ya sea por debajo o por encima del suelo, está equipado con un sistema de calefacción y aislamiento térmico para mantener una temperatura interna constante. Los digestores de flujo de tapón (Figura\(\PageIndex{3}\)) se construyen como tuberías o canales largos, por encima o por debajo del suelo, con una cubierta hermética a los gases. Los contenidos del digestor viajan a través del recipiente donde se convierten en biogás hasta llegar a la salida. El tiempo de residencia está determinado por el tiempo transcurrido entre la alimentación del sustrato fresco y la descarga de los materiales digeridos. Se utilizan para tratar TS relativamente altos de 12% a 16%.
Las lagunas cubiertas se utilizan comúnmente para tratar aguas residuales con bajo contenido de sólidos (< 3%), como estiércol animal purgado. Las lagunas de estiércol en las granjas ganaderas pueden ser mejoradas para ser lagunas cubiertas anaeróbicas utilizando una cubierta no permeable para recolectar el biogás y revestimientos sintéticos dobles para evitar la contaminación del agua subterránea por filtración del contenido del digestor. Los digestores de laguna cubiertos pueden ser mezclados o no mezclados (es decir, tienen agitación mecánica o no) y pueden operarse como sistemas de flujo pistón o CSTR. Suelen operar a temperaturas ambiente dictadas por el clima local.
También existe una clase de sistemas de crecimiento suspendido llamados sistemas de alta tasa, los cuales se caracterizan por usar SRT más largos que HRT. Estos sistemas suelen utilizarse para aguas residuales diluidas con un SRT >20 días, lo que se logra al retener los microorganismos en el digestor. El SRT largo permite el tratamiento a altas tasas de carga orgánica (cantidad de material orgánico procesado por unidad de tiempo). La HRT puede variar de horas a días, dependiendo de las características de las aguas residuales. Los diseños incluyen reactores de lecho de lodo anaeróbico (ASBR) y reactores de manto de lodo de flujo ascendente (UASB). En el ASBR, la retención de microorganismos se logra mediante la sedimentación de sólidos en el reactor antes de la eliminación del efluente. En la UASB, los microorganismos forman gránulos y se retienen en el reactor.
Digestores anaerobios de crecimiento fijo
En digestores de crecimiento fijo, los microorganismos se cultivan en medios sólidos permitiendo una SRT más larga que la HRT. Estos sistemas también son sistemas de alta tasa. Los digestores anaerobios de crecimiento fijo se utilizan para tratar desechos orgánicos solubles (es decir, bajo contenido de sólidos en suspensión) que no requieren hidrólisis. Los medios, como el plástico o las rocas, suelen utilizarse para apoyar la unión y el crecimiento de microorganismos, los cuales forman biopelículas. A medida que las aguas residuales pasan sobre los medios de crecimiento, los contaminantes son absorbidos y adsorbidos por las biopelículas y degradados. Por lo tanto, estos digestores pueden operarse a mayores tasas de carga orgánica que los digestores de crecimiento suspendido.
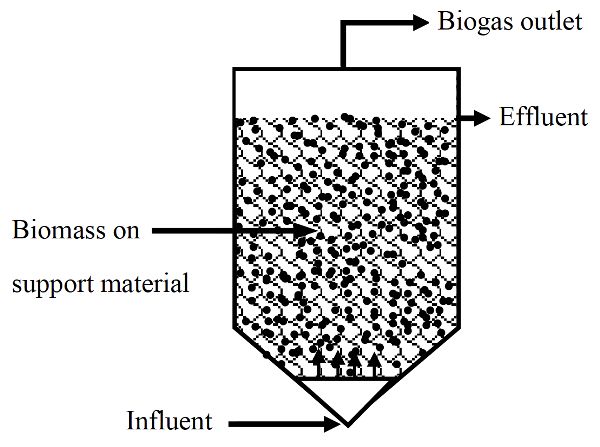
Los filtros anaerobios son un tipo de digestor anaerobio de crecimiento fijo (Figura\(\PageIndex{4}\)). En estos sistemas, gran parte del lodo que contiene microorganismos activos se retiene dentro del digestor al ser unido como biopelícula a un material portador sólido (inerte). Los filtros anaeróbicos se operan en modo de flujo ascendente, lo que significa que el flujo de entrada está por debajo de la salida en la cámara de digestión
Factores que afectan la digestión anaerobia y la producción de biogás
Los procesos de digestión anaeróbica se ven afectados por muchos factores, incluyendo la composición del sustrato, la temperatura, el pH, la carga orgánica, el tiempo de retención y la mezcla, que a su vez afectan el rendimiento y la tasa de producción de biogás. La estabilidad del proceso (es decir, la consistencia de la tasa de producción de biogás) depende del mantenimiento del equilibrio bioquímico entre los microorganismos acidógenos y metanogénicos. La estabilidad del proceso también depende de la composición química y las propiedades físicas del sustrato, la configuración del digestor y los parámetros del proceso como la temperatura, el pH y la concentración de NH 3.
Composición y características del sustrato
La composición del sustrato, particularmente las características físicas y químicas, es un factor importante que afecta el diseño de los sistemas de manejo y digestión de biomasa, el rendimiento de la digestión anaeróbica, el rendimiento de biogás y el procesamiento posterior de los materiales digeridos. Los materiales con grandes tamaños de partículas (por ejemplo, residuos de cultivos y cultivos energéticos) pueden necesitar ser molidos antes de ser alimentados en el digestor anaeróbico. El proceso de molienda puede ayudar en el proceso de conversión porque las partículas pequeñas pueden degradarse más rápido que las grandes. Además, la molienda puede ayudar a manipular el sustrato y mezclar el contenido del digestor. Los desechos mixtos, como los residuos sólidos municipales, generalmente contienen materiales inorgánicos (por ejemplo, metales y desechos de construcción) y necesitan un proceso de separación para eliminar estos materiales inorgánicos. La materia orgánica está compuesta principalmente por carbono (C), hidrógeno (H) y oxígeno (O). También contiene muchos elementos nutritivos incluyendo macronutrientes (por ejemplo, nitrógeno (N), potasio, magnesio y fósforo) y micronutrientes (zinc, manganeso, cobalto, níquel y cobre). Las composiciones de ejemplo se dan en la Tabla 1.2.2. Todos estos nutrientes son necesarios por los microorganismos para descomponer y convertir la materia orgánica en biogás. Una proporción apropiada de C: N en el sustrato está en el rango de 20—25 C a 1 N. La mayoría de los desechos orgánicos, como el estiércol animal y los desechos de alimentos, contienen suficientes nutrientes para apoyar el crecimiento de microorganismos.
El contenido de materia orgánica de un sustrato se describe en términos de sólidos volátiles (VS), demanda química de oxígeno (DQO) o demanda bioquímica de oxígeno (DBO). Los VS se utilizan para caracterizar sustratos con alto contenido de sólidos, mientras que DQO y DBO se utilizan para caracterizar sustratos que tienen un bajo contenido de sólidos, como las aguas residuales. VS es la fracción orgánica de sólidos totales (TS) o materia seca. El DBO se utiliza para describir la biodegradabilidad de un sustrato, mientras que la DQO es la cantidad de oxígeno necesaria para oxidar químicamente la materia orgánica en un sustrato. Si se conoce la composición química de un sustrato, la DQO se puede calcular usando la reacción química:
\( \mathrm{C}_{\mathrm{a}} \mathrm{H}_{\mathrm{b}} \mathrm{O}_{\mathrm{c}} \mathrm{N}_{\mathrm{d}}+\left(a+\frac{b}{4}-\frac{c}{2}-\frac{3 d}{4}\right) \mathrm{O}_{2} \rightarrow a \mathrm{CO}_{2}+\left(\frac{b}{2}-\frac{3 d}{2}\right) \mathrm{H}_{2} \mathrm{O}+d \mathrm{NH}_{3} \)
donde a, b, c y d son el número de átomos de carbono, hidrógeno, oxígeno y nitrógeno, respectivamente, y permiten el cálculo de la cantidad de oxígeno requerida para la reacción, es decir,
\( \left[\left(a+\frac{b}{4}-\frac{c}{2}-\frac{3 d}{4}\right) \mathrm{O}_{2}\right]=\mathrm{COD} \).
| Muestra | C/N | C (%) |
N (%) |
P (%) |
K (%) |
S (%) |
Ca (%) |
Mg (%) |
B (ppm) |
Zn (ppm) |
Mn (ppm) |
Fe (ppm) |
Cu (ppm) |
Na (ppm) |
Co (ppm) |
Ni (ppm) |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
Residuos de tomate |
13.0 |
40.3 |
3.1 |
0.3 |
1.1 |
0.3 |
2.4 |
0.7 |
72.9 |
40.1 |
183.6 |
4482.8 |
23.6 |
1528.5 |
2.5 |
14.0 |
|
Orujo de tomate |
17.0 |
57.8 |
3.5 |
0.5 |
1.0 |
0.2 |
0.3 |
0.3 |
17.6 |
40.1 |
53.8 |
510.3 |
14.3 |
477.0 |
0.4 |
3.0 |
|
Paja de arroz |
77.0 |
38.6 |
0.5 |
0.1 |
2.8 |
0.1 |
0.2 |
0.2 |
6.6 |
33.5 |
492.2 |
432.2 |
4.9 |
2054.0 |
1.3 |
2.0 |
|
Residuos líquidos de huevo |
8.0 |
61.8 |
7.8 |
0.6 |
0.7 |
0.7 |
0.4 |
0.1 |
1.3 |
18.1 |
1.5 |
68.0 |
15.9 |
7165.0 |
<0.1 |
5.0 |
|
Residuos comerciales de alimentos |
16.0 |
43.7 |
2.7 |
0.5 |
2.4 |
0.3 |
3.5 |
0.2 |
18.7 |
170.8 |
34.1 |
443.7 |
9.1 |
3443.0 |
0.4 |
2.0 |
|
Residuos vegetales de supermercado |
22.0 |
45.6 |
2.1 |
0.4 |
2.9 |
0.2 |
0.3 |
0.2 |
38.6 |
126.6 |
22.0 |
187.1 |
10.4 |
1669.5 |
0.2 |
15.0 |
|
Cartón |
231.0 |
46.2 |
0.2 |
0.0 |
0.0 |
0.2 |
0.4 |
0.0 |
42.4 |
18.6 |
26.3 |
255.8 |
10.3 |
1950.5 |
0.3 |
3.0 |
|
Estiércol lácteo |
18.0 |
34.0 |
1.9 |
0.8 |
2.6 |
0.5 |
1.5 |
1.5 |
70.0 |
280.0 |
210.0 |
2100 |
110.0 |
7790 |
<20 |
|
|
Estiércol de pollo |
9.0 |
31.9 |
3.7 |
1.8 |
2.8 |
0.6 |
10.3 |
0.6 |
34.6 |
325.3 |
312.2 |
739.4 |
36.1 |
4162.0 |
0.5 |
12.0 |
Temperatura
La temperatura es un factor importante que afecta el rendimiento de la digestión anaeróbica porque afecta la cinética de los procesos. Los microorganismos suelen clasificarse por la temperatura óptima y el rango de temperatura en el que crecen. La clasificación normal es psicrófila (<25°C), mesófila (25 a 45°C) y termófila (45 a 65°C), pero en teoría existe el extremo de arqueas anaerobias hipertermófilas y bacterias que pueden crecer en ambientes geotérmicos con temperaturas de crecimiento óptimas de 80°C a 110°C (Stetter, 1996). La digestión termófila puede producir biogás con un mayor contenido de CO 2 que la digestión mesofílica debido a la baja solubilidad del CO 2 en agua a altas temperaturas.
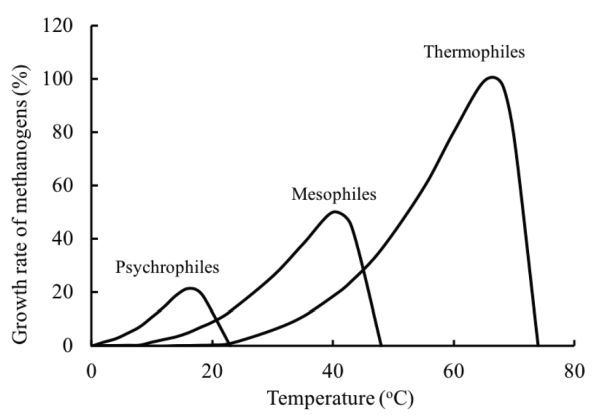
La tasa de crecimiento de microorganismos aumenta con el aumento de la temperatura hasta un óptimo. Por encima de la temperatura óptima, el crecimiento disminuye debido a la desnaturalización térmica de la proteína celular. El crecimiento cesará cuando se destruya la proteína esencial de la célula. La Figura 1.2.5 muestra la tasa de crecimiento relativo de los metanógenos en diferentes rangos de temperatura. Dentro del rango de temperatura de una especie, la tasa de crecimiento aumenta exponencialmente con la temperatura. Termodinámicamente, la mayoría de las reacciones bioquímicas requieren menos energía para proceder a altas temperaturas. La tasa de la mayoría de las reacciones químicas se duplica aproximadamente con un aumento de temperatura de 10°C (Stanier et al., 1972). La energía requerida para calentar el sustrato y mantener el digestor a la temperatura deseada es mayor a temperaturas más altas.
pH
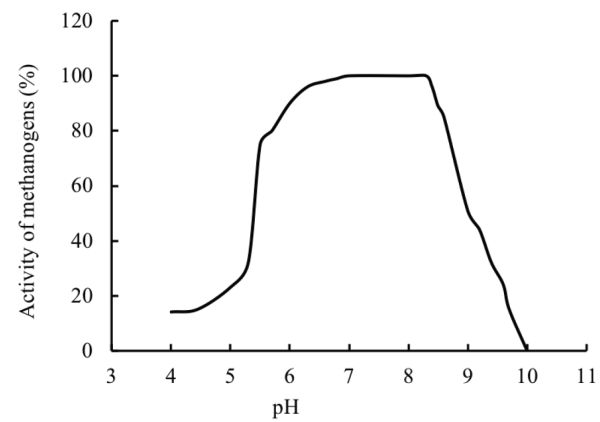
El pH de un digestor se ve afectado por la interacción entre la composición del sustrato, su capacidad amortiguadora y el equilibrio entre las tasas de acidificación y metanogénesis. Si la tasa de metanogénesis es menor que la acidogénesis, el pH podría alcanzar valores por debajo de 6, lo que puede causar inhibición a las arqueas metanogénicas. La relación entre el pH y la actividad metanogénica es una curva en forma de campana (Figura\(\PageIndex{6}\)) con una actividad metanogénica máxima a valores de pH entre aproximadamente 6.8 y 8 (Speece, 1996; Khanal, 2008). Se debe mantener un pH óptimo cerca de la neutralidad en el digestor anaeróbico para la producción de biogás.
Cargando Orgánico
La carga orgánica (o carga inicial) es una medida de la cantidad de materia orgánica, expresada en términos de la cantidad de VS o DQO que ingresa a un digestor discontinuo al inicio de un ciclo de proceso. Es un parámetro importante que afecta el tamaño del digestor porque determina la concentración de biomasa microbiana funcional por unidad de masa de sustrato. Para digestores alimentados continuamente, la tasa de carga orgánica (OLR), generalmente definida como la cantidad de materia orgánica alimentada por unidad de volumen del digestor por día, depende de la cinética de biodegradación del sustrato, el diseño del digestor y las condiciones de operación. Por ejemplo, un CSTR que trata estiércol animal con un contenido de TS de 1— 6% generalmente se opera a una OLR de 1.6 a 4.8 kg m 3 día −1 y una HRT de 15 a 30 días.
Tiempo de Retención
El tiempo de retención es el tiempo para que el sustrato permanezca en el digestor para ser procesado por los microorganismos. El tiempo de retención adecuado depende de las características químicas y físicas del sustrato y de la tasa de metabolismo microbiano. Los sustratos complejos, como los desechos agrícolas (por ejemplo, estiércol animal), suelen tener bajas tasas de biodegradación y, por lo tanto, necesitan tiempos de retención más largos (20 a 30 días), mientras que los materiales altamente biodegradables, como los desechos de alimentos, pueden necesitar tiempos de retención más cortos (<15 días) para convertir la materia orgánica biodegradable en biogás.
Mezclar
La mezcla afecta el rendimiento de los digestores anaerobios al asegurar la homogeneización del contenido del reactor al romper las partículas del sustrato y exponer grandes áreas superficiales del sustrato a microorganismos. La mezcla adecuada evita el desarrollo de estratificación dentro de digestores, lo que podría resultar en microambientes desfavorables para los metanógenos, como regiones ricas en compuestos tóxicos o con pH bajo. La mezcla también ayuda a mantener una temperatura uniforme en el digestor y evita la formación de una capa de espuma. El requisito para lograr una mezcla adecuada depende de la forma del digestor, el tipo de sistemas de mezcla y el contenido de sólidos dentro del digestor. Por ejemplo, un tanque rectangular plantea dificultades para mezclar en comparación con los reactores cilíndricos y en forma de huevo porque es difícil mezclarlo en las esquinas. Los digestores se pueden mezclar con mezcladores mecánicos, recirculación de biogás o recirculación del contenido del reactor. La selección del sistema de mezcla depende de la densidad del sustrato (es decir, concentración de sólidos), intensidad de mezcla requerida, homogeneidad, disponibilidad y costo del equipo de mezcla, y costos de mantenimiento y consumo de energía.
Configuración de procesos
Los procesos de digestión anaerobia se pueden llevar a cabo en digestores de una sola etapa o en digestores multietapa. Los digestores de una sola etapa se utilizan generalmente para materiales que tienen tasas de degradación equilibradas de hidrólisis, acidogénesis y metanogénesis y tienen suficiente capacidad de tampón para mantener el pH del digestor alrededor de neutro. Sin embargo, para materiales altamente biodegradables, como el desperdicio de alimentos, generalmente se utilizan sistemas de digestión de múltiples etapas (en su mayoría dos etapas). En estos sistemas, la hidrólisis y la acidogénesis son los procesos predominantes en la primera etapa, con pH bajo (4—6) debido a las altas concentraciones de AGV. El biogás producido desde la primera etapa contiene altos contenidos de CO 2 e hidrógeno y bajo contenido de CH 4. En la segunda etapa, la metanogénesis predomina cuando los AGV son consumidos por las arqueas metanogénicas y el pH está en el rango de 6.8—8. El biogás producido a partir de la segunda etapa tiene un alto contenido de CH 4 (50— 70%).
Concentración de amoníaco
La digestión anaerobia de sustratos ricos en proteínas puede producir altas concentraciones de NH 3 que pueden causar inhibición o incluso toxicidad a microorganismos anaerobios. Los microorganismos necesitan N para su síntesis celular. Aproximadamente 6.5% del N afluente se utiliza para la producción celular. Las bacterias fermentativas generalmente pueden utilizar tanto aminoácidos como NH 3, pero las bacterias metanogénicas solo usan NH 3 para la síntesis de células bacterianas (Hobson y Richardson, 1983). Las concentraciones altas de NH 3 pueden causar inhibición, o incluso toxicidad, a microorganismos metanogénicos. La inhibición está indicada por una disminución en la producción de NH 3 y el aumento de las concentraciones de VFA. Cuando hay un cese total de la actividad metanogénica, el NH 3 libre suele ser la causa principal. Esto se debe a que las células de microorganismos son más permeables al NH 3 libre que a los iones amonio. La concentración de NH 3 libre depende del NH 3 total, la temperatura y el pH.
Estimación de rendimientos de biogás y metano
Estimación teórica del rendimiento
Los rendimientos de biogás y CH 4 pueden estimarse teóricamente a partir de la composición química del sustrato o medirse mediante experimentos de digestión por lotes. El biogás y el rendimiento de CH 4 a partir de un sustrato orgánico completamente biodegradable con la composición (C a H b O c N d) se pueden determinar usando la ecuación de Buswell (Buswell y Mueller, 1952):
\( \mathrm{C}_{\mathrm{a}} \mathrm{H}_{\mathrm{b}} \mathrm{O}_{\mathrm{c}} \mathrm{N}_{\mathrm{d}}+\left(\frac{4 a-b-2 c+3 d}{4}\right) \mathrm{H}_{2} \mathrm{O} \rightarrow\left(\frac{4 a+b-2 c-3 d}{8}\right) \mathrm{CH}_{4}+\left(\frac{4 a-b+2 c+3 d}{8}\right) \mathrm{CO}_{2}+d \mathrm{NH}_{3} \)
Esta ecuación no considera las necesidades de materia orgánica para el mantenimiento celular y el anabolismo. A partir de la ecuación de Buswell, la cantidad total de biogás producida a partir de un mol del sustrato orgánico biodegradable puede calcularse como una suma de CH 4 y CO 2, es decir:
\( \left[\left(\frac{4 a+b-2 c-3 d}{8}\right)+\left(\frac{4 a-b+2 c+3 d}{8}\right)\right] \)
El volumen del rendimiento de biogás o metano por cada gramo del sustrato L g −1 [VS] se puede calcular usando el volumen molar de un gas ideal como 22.4 L a la temperatura y presión estándar como:
\[ M_{\mathrm{y}}=\frac{\left(\frac{4 a+b-2 c-3 d}{8}\right) \times 22.4}{12 a+b+16 c+14 d} \]
donde M y = contenido de metano en el biogás,% (moles/mol o v/v).
Suponiendo que el biogás está compuesto principalmente por metano y dióxido de carbono y la producción de amoníaco es insignificante, el contenido de metano en el biogás se puede calcular de la siguiente manera:
\[ M_{\mathrm{C}}=\frac{\left(\frac{4 a+b-2 c-3 d}{8}\right) \times 100}{\left(\frac{4 a+b-2 c-3 d}{8}\right)+\left(\frac{4 a-b+2 c+3 d}{8}\right)} \]
donde M c = contenido de metano en el biogás,% (moles/mol o v/v).
La producción de CH 4 después de un largo tiempo de degradación se llama potencial de metano. El rendimiento de metano se puede expresar como el volumen de gas producido por unidad de masa del sustrato (L [CH 4] /kg [sustrato]), VS (L [CH 4] /kg [VS]) o DQO (L [CH 4] /kg [DQO]). El rendimiento teórico de CH 4 y el contenido de sustratos seleccionados calculados usando la ecuación de Buswell (Cuadro 1.2.3) generalmente se subestiman porque el CO 2 es más soluble en agua que el CH 4. En digestores anaerobios, el contenido de CH 4 del biogás oscila entre 55% y 70%, dependiendo del sustrato y las condiciones de operación de los digestores (Cuadro 1.2.3). Los sustratos ricos en lípidos deben producir biogás rico en metano.
| Tipo de Sustrato | Fórmula | Rendimiento de gas [a] (L g −1 [VS]) | Contenido de Metano [b] (%) | ||
|---|---|---|---|---|---|
| CH 4 | CO 2 | NH 3 | |||
|
Carbohidratos |
(C 6 H 10 O 5) n |
0.415 |
0.415 |
0.000 |
50.0 |
|
Proteína |
C 5 H 7 NO 2 |
0.496 |
0.496 |
0.198 |
50.0 |
|
Lípido |
C 57 H 104 O 6 |
1.014 |
0.431 |
0.000 |
70.2 |
|
Acetato |
C 2 H 4 O 2 |
0.374 |
0.374 |
0.000 |
50.0 |
|
Etanol |
C 2 H 6 O |
0.731 |
0.244 |
0.000 |
75.0 |
|
Propionato |
C 3 H 6 O 2 |
0.530 |
0.379 |
0.000 |
58.3 |
|
[a] Los rendimientos están a temperatura y presión estándar (ver texto). [b] Suponiendo que el biogás está compuesto por metano y dióxido de carbono. |
|||||
Modelado del proceso de digestión anaeróbica para estimar el rendimiento
Existen modelos mecanicistas que describen el proceso de digestión anaeróbica, los cuales pueden ser utilizados para predecir el desempeño de digestores anaeróbicos. Uno de los más utilizados es el Modelo de Digestión Anaeróbica No. 1 (ADM1), desarrollado por la International Water Association Task Group for Mathematical Modeling of Anaerobic Digestion Process (Batstone et al., 2002). La ADM1 se estructura en torno a subprocesos bioquímicos, incluyendo hidrólisis, acidogénesis, acetogénesis y metanogénesis. Si bien un enfoque de modelado mecanicista es necesario para un diseño avanzado, se puede usar un modelo cinético simple de primer orden para calcular el rendimiento de metano de diferentes sustratos, como desechos de alimentos, estiércol animal y residuos de cultivos, y usarse para el diseño preliminar. La cinética de primer orden para un digestor por lotes se puede escribir como:
\[ \frac{d S}{\mathrm{dt}}=-k S \]
donde t = tiempo de digestión (días)
k = constante de velocidad cinética de degradación de primer orden (día -1)
S = concentración de la materia orgánica biodegradable (expresada como VS, DQO o DBO) en el digestor (kg m −3)
Con la concentración del sustrato biodegradable al inicio del tiempo de digestión designada como S 0 (kg m −3), la ecuación puede expresarse como:
\[ S=S_{0} \mathrm{e}^{-\mathrm{kt}} \]
La ecuación 1.2.4 puede usarse para predecir la concentración de sustrato restante (S) en el digestor después de un período de tiempo de digestión (t) si se conocen la concentración inicial de sustrato (S 0) y la constante de velocidad cinética de degradación. La cantidad de materia orgánica degradada que se convierte en metano, y la cantidad de metano producido se pueden calcular como:
\[ S_{\mathrm{deg}}=V_{\mathrm{w}}\left(S_{0}-S\right) \]
\[ M_{\mathrm{p}}=M_{\mathrm{y}} S_{\mathrm{deg}} \]
donde S grados = materia orgánica degradada en el digestor (kg)
V w = volumen de trabajo del digestor (es decir, volumen de líquido dentro del digestor) (m 3)
M p = cantidad de metano producido (m 3)
M y = rendimiento de metano (m 3 kg −1)
Las ecuaciones 1.2.4, 1.2.5 y 1.2.6 se pueden utilizar para ajustar datos experimentales que describen la concentración de sustrato en etapas de tiempo a lo largo del proceso para determinar la constante de velocidad cinética de degradación de primer orden. También se pueden usar para predecir la materia orgánica degradada en el digestor y el rendimiento de metano en diferentes tiempos de digestión si la constante de velocidad cinética de degradación de primer orden se conoce de la literatura o de experimentos.
Estimación de la producción de energía a partir de un sustrato
La cantidad de energía contenida en un combustible (por ejemplo, biogás) se expresa usando el valor calorífico más alto (HHV) o el valor calorífico inferior (LHV). El HHV es el calor total producido a partir de una combustión completa de una unidad (generalmente 1 m 3) del gas bajo una presión constante y toda el agua formada por la reacción de combustión condensada al estado líquido. El LHV es el valor calórico neto producido por la combustión de una cantidad unitaria del combustible y toda el agua formada durante la reacción de combustión permanece en estado vapor. El metano se utiliza para calcular la cantidad de energía contenida en el biogás porque es el principal gas combustible. A temperatura y presión estándar, el metano tiene un LHV de aproximadamente 36 MJ m −3. Por lo tanto, el LHV del biogás que contiene 65% de metano es aproximadamente 23.4 MJ m −3, el cual se calcula multiplicando el LHV de metano por el contenido de metano del biogás.
La cantidad de energía que se produce a partir de un digestor anaeróbico se puede estimar utilizando la cantidad de materia orgánica que se trata en un cierto período de tiempo (por ejemplo, día), rendimiento de biogás del sustrato y contenido de metano del biogás. Con base en el contenido de TS y VS del sustrato, la cantidad de materia orgánica a tratar puede calcularse como:
\[ \phi_{\mathrm{om}}=Q \times T_{\mathrm{sc}} \times V_{\mathrm{sc}} \]
donde φ om = cantidad de materia orgánica a tratar por día, kg [VS] día −1
Q = cantidad de materia prima a tratar (kg día −1)
T sc = contenido total de sólidos,%, base húmeda
V sc = contenido de sólidos volátiles,% de T sc
La producción diaria de biogás y metano se puede calcular de la siguiente manera:
\[ B_{\mathrm{dp}}=\phi_{\mathrm{om}} B_{\mathrm{y}} \]
\[ M_{\mathrm{dp}}=B_{\mathrm{dp}} M_{\mathrm{C}} \]
donde B dp = producción diaria de biogás, m 3 día −1
B y = producción de rendimiento de biogás, m 3 kg −1 [VS]
M dp = producción diaria de metano, m 3 día −1
M c = contenido de metano en el biogás,% vol vol −1
La producción diaria de energía a partir del biogás se puede calcular de la siguiente manera:
\[ E_{\mathrm{dp}}=B_{\mathrm{dp}} \times C_{\mathrm{vb}} \]
o
\[ E_{\mathrm{dp}}=M_{\mathrm{dp}} \times C_{\mathrm{vm}} \]
donde E dp = producción diaria de energía, MJ día −1
C vb = poder calorífico del biogás, MJ m −3
C vm = valor calorífico del metano, MJ m −3
Dimensionando Digestores Anaerobios
El rendimiento del digestor anaeróbico está controlado por el número de microorganismos activos que están en contacto con el sustrato. Por lo tanto, aumentar el número de bacterias activas puede aumentar la tasa de conversión y, en consecuencia, se pueden utilizar mayores tasas de carga orgánica. El volumen total (V t) de un digestor se calcula a partir del volumen de trabajo (V w) y el volumen del espacio de cabeza (V h) como:
\[ V_{\mathrm{t}}=V_{\mathrm{w}}+V_{\mathrm{h}} \]
El volumen del espacio superior es el volumen de gas por encima del líquido que a veces se usa para el almacenamiento de gas. El volumen del espacio de cabeza suele ser aproximadamente el 10% del volumen de trabajo. El volumen de trabajo requerido de un digestor anaerobio alimentado continuamente se puede determinar a partir de la cantidad de materia orgánica (expresada como VS o DQO) a tratar por día y el OLR:
\[ V_{\mathrm{w}}=\frac{\phi_{\mathrm{om}}}{\mathrm{OLR}} \]
donde V w = volumen de trabajo del digestor, m 3
OLR = tasa de carga orgánica
El volumen de trabajo también se puede determinar a partir del volumen de residuos a tratar por día y el tiempo de retención hidráulica del digestor:
\[ V_{\mathrm{w}}=V_{\mathrm{df}} \times \mathrm{HRT} \]
donde V df = alimentación volumétrica al digestor, m 3 día −1
HRT = tiempo de retención hidráulica
Limpieza y Mejoramiento de Biogás
Los procesos de limpieza y mejora del biogás son importantes para eliminar compuestos dañinos e indeseados y aumentar la calidad del biogás como combustible. La limpieza de biogás es la eliminación de impurezas como sulfuro de hidrógeno y compuestos orgánicos, y la mejora es la eliminación de CO 2 y vapor de agua, lo que resulta en un metano (biometano) relativamente puro que puede usarse como combustible para automóviles o inyectarse en un gasoducto de gas natural.
En el cuadro 1.2.4 se muestra una composición típica del biogás procedente de la digestión de residuos agrícolas y de los vertederos de residuos sólidos municipales.
Limpieza de Biogás
La eliminación del sulfuro de hidrógeno es importante antes de usar biogás porque es corrosivo y tóxico. En presencia de vapor de agua, el sulfuro de hidrógeno forma ácido sulfúrico, lo que puede provocar una grave corrosión de los componentes metálicos del digestor y del equipo de manejo de biogás. La eliminación del sulfuro de hidrógeno se puede llevar a cabo usando precipitación química mediante la adición de iones metálicos (generalmente iones férricos) al recipiente digestor o absorción química pasando el biogás a través de una solución férrica (por ejemplo, cloruro férrico (conocido como esponja de hierro)) como:
| Componente | Residuos Agrícolas | Vertederos de residuos sólidos municipales |
|---|---|---|
|
Metano |
50— 80% |
45— 65% |
|
Dióxido de carbono |
30— 50% |
34— 55% |
|
Vapor de agua |
Saturado |
Saturado |
|
Sulfuro de hidrógeno |
100—7,000 ppm |
0.5—100 ppm |
|
Hidrógeno |
0— 2% |
0— 1% |
|
Amoníaco |
50—100 ppm |
Rastro |
|
Monóxido de carbono |
0— 1% |
Rastro |
|
Nitrógeno |
0— 1% |
0— 20% |
|
Oxígeno |
0— 1% |
0— 5% |
|
Compuestos orgánicos volátiles |
Rastro |
5—100 ppm |
\( 3 \mathrm{H}_{2} \mathrm{~S}+2 \mathrm{FeCl}_{3} \rightarrow \mathrm{Fe}_{2} \mathrm{~S}_{3} \downarrow+6 \mathrm{H}^{+}+6 \mathrm{Cl} \)
Además, el sulfuro de hidrógeno se puede eliminar mediante oxidación biológica por bacterias quimiotróficas como Thiobacillus thioparus. Sin embargo, la aplicación comercial de la oxidación biológica es limitada.
Los siloxanos son compuestos orgánicos volátiles que generalmente se encuentran en el biogás producido a partir de los vertederos. Durante las reacciones de combustión, se convierten en dióxido de silicio (SiO 2) y cuarzo microcristalino que se depositan en las piezas del motor, provocando problemas como el desgaste. El carbón activado o gel de sílice se utilizan comúnmente como adsorbentes para eliminar estos compuestos orgánicos del biogás.
Mejoramiento de Biogás
La remoción de CO 2 es importante para aumentar el contenido energético del biogás, reducir los volúmenes requeridos para el almacenamiento de biogás y lograr la calidad necesaria para cumplir con las especificaciones del gas natural para distribución con gas fósil y las especificaciones para motores de gas natural comprimido. Además, la presencia de CO 2 puede causar corrosión en equipos y tuberías si se mezcla con agua para formar ácido carbónico. El dióxido de carbono se puede eliminar del biogás con agua o sistemas de depuración química, en los que el agua o disolventes químicos (por ejemplo, hidróxido de sodio y amina) reaccionan con CO 2:
CO 2 + H 2 O ↔ H 2 CO 3
CO 2 + NaOH → NaHCO 3
El dióxido de carbono también se puede eliminar del biogás mediante el uso de membranas y sistemas de adsorción por oscilación de presión (PSA). Las membranas tienen permeabilidad selectiva. Permiten que diferentes compuestos (por ejemplo, gases) se muevan a través de la membrana a diferentes velocidades. Cuando el biogás se bombea bajo presión (hasta 4000 kPa) a través de una membrana hecha de polímeros, el dióxido de carbono se separa del metano. En el sistema de adsorción por oscilación de presión, el biogás fluye bajo presión (hasta 1000 kPa) a través de un material poroso que permite el paso del metano mientras absorbe y elimina el dióxido de carbono. Los materiales adsorbentes en sistemas comerciales incluyen tamices moleculares de carbono, carbón activado, gel de sílice y zeolitas. Antes de que el material adsorbente esté completamente saturado con dióxido de carbono, necesita ser regenerado y luego reutilizado. El proceso de regeneración se lleva a cabo reduciendo la presión en el recipiente a presiones cercanas a la ambiente y luego al vacío.
Algunos materiales adsorbentes utilizados para el dióxido de carbono también pueden adsorber sulfuro de hidrógeno, oxígeno y nitrógeno. Sin embargo, la absorbancia de sulfuro de hidrógeno en estos materiales no es reversible.
El biogás recolectado de los digestores se satura con vapor de agua. El contenido de agua del biogás depende de la temperatura de funcionamiento del digestor. A temperaturas más bajas habrá menos vapor de agua en el biogás. El vapor de agua se elimina para proteger tuberías y equipos de la corrosión a través de la formación de ácidos (por ejemplo, ácidos sulfúrico y carbónico). El vapor de agua se puede eliminar por condensación o secado químico (por ejemplo, absorción). La condensación de vapor de agua se puede forzar reduciendo el punto de rocío usando un sistema de enfriamiento como un enfriador e intercambiador de calor. Un fluido se enfría en el enfriador y se bombea a través de un lado del intercambiador de calor para reducir la temperatura del biogás que fluye en el otro lado del intercambiador de calor. En el secado químico, se utilizan agentes como gel de sílice, óxido de magnesio, óxido de aluminio o carbón activado para absorber el vapor de agua. Después de la saturación, los agentes secantes se regeneran calentando a alrededor de 200°C. Para mantener operaciones continuas, se utilizan dos columnas rellenas con los agentes secantes para asegurarse de que se usa agente de secado insaturado mientras se regenera la saturada.
Aplicaciones
Experimentación para determinar las propiedades de digestión
Los rendimientos de biogás y metano se pueden determinar mediante el uso de configuraciones experimentales de digestión anaeróbica discontinua que van desde lo muy simple (Figura\(\PageIndex{7}\)) hasta un sofisticado sistema automatizado de prueba de potencial de metano (AMPTS) (Figura 1.2.8). Las pruebas anaeróbicas de digestión por lotes se pueden realizar a pequeña escala (0.1—1 litro) para determinar los rendimientos de biogás y biometano y la biodegradabilidad de un sustrato. El método simple por lotes se puede realizar utilizando equipos de laboratorio asequibles; un AMPTS es más costoso pero se puede automatizar y es más preciso. El AMPTS permite medir la producción de biogás a través del tiempo.
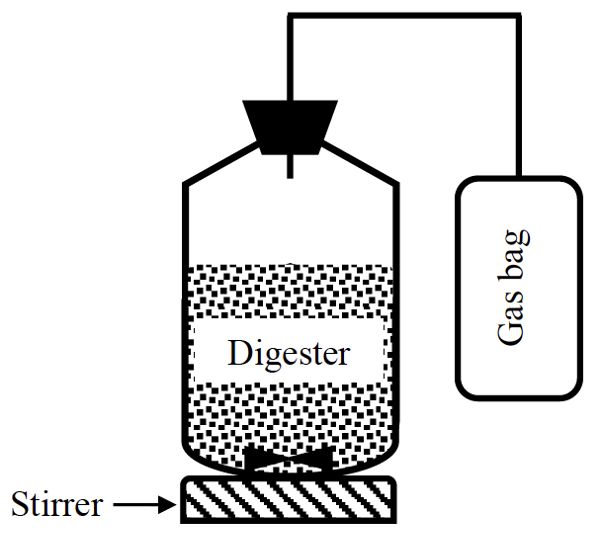
Un simple sistema anaeróbico de digestión por lotes (Figura\(\PageIndex{7}\)) está compuesto por un recipiente, que normalmente es una botella sellada con una tapa y una abertura para dejar salir el biogás. Con base en la composición (TS y VS) del sustrato, se utiliza una cantidad del sustrato que da 3 g VS para iniciar la digestión. El sustrato se pone en el recipiente y se agrega inóculo. El inóculo es un material de semilla tomado de un digestor anaerobio activo. El pH del digestor debe ser aproximadamente 7. El digestor se enjuaga con un gas inerte, como helio o argón, durante aproximadamente dos minutos para asegurar la condición anaeróbica al eliminar el oxígeno tanto del líquido como del espacio de cabeza. El digestor se sella con un tapón de goma y se conecta a una bolsa de gas (llamada bolsa Tedlar) para recoger el biogás. El digestor se incuba a temperatura constante (35°—50°C) hasta por 25 días. Durante el tiempo de incubación, los contenidos se mezclan intermitentemente usando un agitador o mediante agitación manual durante aproximadamente un minuto, pero sin romper el sello de la botella. Cada tratamiento debe ser replicado y se utiliza un testigo usando solo inóculo para estimar el biogás producido por el inóculo solo. El biogás recolectado se puede medir usando desplazamiento de líquido o jeringa hermética a gases. El pH se mide al final del tiempo de digestión. El rendimiento de biogás (L g −1 VS) se determina dividiendo el biogás acumulado por la cantidad inicial del VS en el digestor al inicio de la digestión. El rendimiento de metano se calcula multiplicando el rendimiento de biogás por el contenido de metano del biogás que se puede medir mediante un cromatógrafo de gases.

Un AMPTS (Figura\(\PageIndex{8}\)) se compone de tres partes: un baño de agua con control de temperatura, una unidad de fijación de CO 2 y un medidor de punta de gas. Los recipientes se incuban en el baño de agua a temperatura constante. Todos los recipientes se mezclan continuamente utilizando mezcladores mecánicos. La unidad de fijación de CO 2 se utiliza para eliminar CO 2 del biogás. La unidad de medición de gas (medidor de punta) puede determinar la cantidad de producción de metano de cada digestor individual. El medidor de punta está conectado a un registrador de datos que registra continuamente la producción de metano. Todos los procedimientos para la preparación de digestores simples anaerobios por lotes también se aplican en el AMPTS.
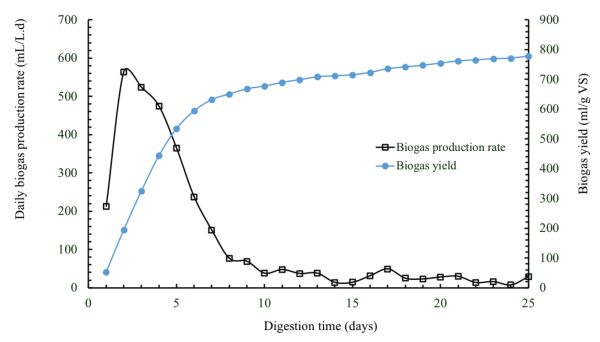
La figura\(\PageIndex{9}\) muestra la producción diaria de biogás y el rendimiento acumulado de biogás determinado a partir de un digestor anaeróbico discontinuo, con una capacidad de 1 L, tratando los residuos de comida de cafetería a una carga VS inicial de 4 g L −1 y una temperatura de 50°C. digestión por lotes y luego disminuir hasta llegar a casi cero. Esto se debe a la reducción de la materia orgánica contenida en el sustrato a lo largo del tiempo de digestión hasta que toda la materia orgánica disponible es consumida por microorganismos.
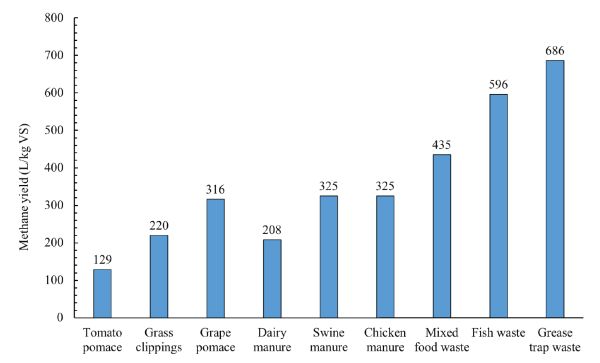
Los datos de producción de metano y concentración de sustrato restante en pruebas de digestión por lotes se pueden utilizar para determinar la constante de velocidad cinética de degradación de primer orden usando las Ecuaciones 1.2.4, 1.2.5 y 1.2.6. La producción de metano se calcula multiplicando la producción de biogás por el contenido de metano del biogás (que generalmente se mide mediante cromatografía de gases). La Figura 1.2.10 muestra los rendimientos de metano de diversos desechos orgánicos después de un tiempo de digestión de 25 días. Como se puede observar, la composición del sustrato afecta el rendimiento de metano. Los datos experimentales de las pruebas de digestión por lotes podrían usarse para determinar la TRH y el tamaño de los vasos adecuados para sistemas piloto y a escala completa para tratar una cantidad específica de sustrato. Por ejemplo, el tiempo de digestión requerido para convertir toda o parte de la materia orgánica biodegradable en un determinado sustrato en biogás podría usarse como base para determinar el HRT adecuado para convertir el sustrato en biogás en un digestor de alimentación continua a la misma temperatura. Una vez determinada la TRH, el volumen efectivo se puede determinar usando la Ecuación 1.2.14.
Usos comerciales del biogás
Además de utilizar biogás para la generación de electricidad usando generadores y celdas de combustible, y para fines de calefacción, el biogás puede actualizarse a biometano (también conocido como gas natural renovable, RNG). El biometano es muy similar al gas natural, por lo tanto, la mayoría de los equipos utilizados para el gas natural pueden ser operados con biometano. El biometano puede ser utilizado como combustible de transporte en forma de gas natural comprimido renovable (GNC) o gas natural licuado (GNL). La Agencia de Protección Ambiental de Estados Unidos definió el GNC y el GNL renovables como biogás o “gas de calidad de tubería” derivado del biogás que se licua o comprime para fines de transporte. Para estos usos, el biogás debe limpiarse y actualizarse, ya sea in situ adyacente al digestor o bombeado a una instalación central que procesa biogás a partir de múltiples digestores en las cercanías. El biometano también podría venderse a empresas de servicios públicos por inyección en gasoductos naturales. El biometano debe cumplir con altos estándares de calidad para inyección en los ductos (Tabla\(\PageIndex{5}\)).
| Parámetro de calidad | Valor |
|---|---|
|
Contenido de agua (kg por 1000 m 3 a 55.15 bar) |
0.11 |
|
Sulfuro de hidrógeno (ppm) |
4 |
|
Azufre total (ppm) |
17 |
|
Dióxido de carbono (%) |
1 |
|
Hidrógeno (%) |
0.1 |
Ejemplos
Ejemplo\(\PageIndex{1}\)
Ejemplo 1: Producción teórica de metano
Problema:
Una cafetería quiere manejar los residuos de alimentos utilizándolos como materia prima para un digestor anaeróbico. ¿Cuál es la producción teórica de metano a temperatura y presión estándar a partir de 1,000 kg de desechos orgánicos de alimentos con la fórmula química C 3.7 H 6.4 O 1.8 N 0.2? ¿Cuál es el contenido esperado de metano del biogás asumiendo que consiste solo en metano y dióxido de carbono?
Solución
Aplicando la ecuación de Buswell:
\( \mathrm{C}_{3.7} \mathrm{H}_{64} \mathrm{O}_{18} \mathrm{~N}_{0.2}+\left(\frac{4(3.7)-6.4-2(1.8)+3(0.2)}{4}\right) \mathrm{H}_{2} \mathrm{O} \rightarrow\left(\frac{4(3.7)+6.4-2(1.8)-3(0.2)}{8}\right) \mathrm{CH}_{4}+\left(\frac{4(3.7)-6.4+2(1.8)+3(0.2)}{8}\right) \mathrm{CO}_{2}+0.2 \mathrm{NH}_{3} \)
\( \mathrm{C}_{3.7} \mathrm{H}_{6.4} \mathrm{O}_{1.8} \mathrm{~N}_{0.2}+1.35 \mathrm{H}_{2} \mathrm{O} \rightarrow 2.125 \mathrm{CH}_{4}+1.575 \mathrm{CO}_{2}+0.2 \mathrm{NH}_{3} \)
Esto significa que 1 mol (82.4 g) de los residuos orgánicos de alimentos producen 2.125 moles de CH 4 y 1.575 moles de CO 2.
Calcular el rendimiento de metano usando la Ecuación 1.2.1:
\( M_{\mathrm{y}}=\frac{\left(\frac{4 a+b-2 c-3 d}{8}\right) \times 22.4}{12 a+b+16 c+14 d} \)(Ecuación\(\PageIndex{1}\))
\( M_{\mathrm{y}}=\frac{2.125 \times 22.4}{82.4}=0.577 \mathrm{~L} \mathrm{~g}^{-1}[\mathrm{VS}] \)
\( \text { Amount of methane production from } 1,000 \mathrm{~kg}=0.577 \times 1,000 \times 1,000=575,000 \mathrm{~L}=577 \mathrm{~m}^{3} \)
Calcular el contenido de metano usando la Ecuación 1.2.2:
\( M_{\mathrm{C}}=\frac{\left(\frac{4 a+b-2 c-3 d}{8}\right) \times 100}{\left(\frac{4 a+b-2 c-3 d}{8}\right)+\left(\frac{4 a-b+2 c+3 d}{8}\right)} \)(Ecuación\(\PageIndex{2}\))
\( M_{\mathrm{C}}=\frac{2.125 \times 100}{2.125+1.575}=57.4 \% \)
Ejemplo\(\PageIndex{2}\)
Ejemplo 2: Diseño de un digestor anaerobio para estiércol lácteo
Problema:
Un lechero quiere construir un digestor anaeróbico para tratar el estiércol producido a partir de mil vacas. Cada vaca produce 68 kg de estiércol al día. El sólido volátil (VS) del estiércol es de 11% (base húmeda). El digestor debe operarse a una tasa de carga orgánica de 2 kg [VS] m −3 día −1 y una temperatura de 35°C. El volumen del espacio de cabeza de gas es del 10% del volumen de trabajo. El rendimiento de biogás del estiércol es de 288 L kg −1 [VS] y el contenido de metano es de 65%. Supongamos que todo el estiércol producido en la lechería será tratado en el digestor. Calcular:
- a) el volumen del digestor requerido,
- b) la producción diaria de biogás y metano, y
- (c) la producción diaria de energía a partir del biogás si el biogás tiene un valor calorífico de 23 MJ m −3.
Solución
La cantidad de materia orgánica a tratar por día (φ om) se puede calcular utilizando el número de vacas, la cantidad de estiércol producido de cada vaca por día y el contenido de sólidos volátiles del estiércol de la siguiente manera:
\ (\ begin {aligned}
&\ text {La cantidad de materia orgánica a tratar por}\ nombreoperador {día}\ left (\ phi_ {\ mathrm {m}}\ right) =\ text {número de vacas}\ veces\ text {cantidad de estiércol producido de cada vaca}\ veces\ text {contenido de sólidos volátiles de estiércol} =1,000\ veces 68\ veces\ left (\ frac {11 } {100}\ derecha) =7.480\ mathrm {~kg} [\ mathrm {VS}]\ texto {día} ^ {-1}\ end {alineado}
Calcular el volumen de trabajo del digestor usando la Ecuación 1.2.13:
\( V_{\mathrm{w}}=\frac{\phi_{\mathrm{Om}}}{\mathrm{OLR}}=\frac{7,480}{2}=3,740 \mathrm{~m}^{3} \)
Calcular el volumen total (V t) del digestor usando la Ecuación 1.2.12:
\( V_{\mathrm{t}}=V_{\mathrm{w}}+V_{\mathrm{h}} \)
\( V_{\mathrm{t}}=3,740+\left(\frac{10}{100}\right)(3,740)=4,114 \mathrm{~m}^{3} \)
Calcular la producción diaria de biogás usando la Ecuación 1.2.8:
\( B_{\mathrm{dp}}=\phi_{\mathrm{om}} B_{\mathrm{y}} \)
\( B_{dp}=7,480 \times \frac{288}{1,000} = 2,154.2 \text{m}^{3} \text {day}^{-1} \)
Calcular la producción de metano usando la Ecuación 1.2.9:
\( M_{dp}=B_{dp} \times M_{C} \)
\( M_{dp} = 2,154.2 \times \frac{65}{100} = 1,400.2 \text{m}^3 \text{day}^{-1} \)
Calcular la producción de energía usando la Ecuación 1.2.10:
\( E_{dp} = B_{dp} \times CV_{B} \)
\( E_{dp} = 2,154.2 \times 23 = 49,546.6 \ MJ \ \text{day}^{-1} \)
Ejemplo\(\PageIndex{3}\)
Ejemplo 3: Modelado y cinética
Problema:
Un digestor discontinuo con un volumen de 5 L trata un sustrato orgánico con una carga inicial de 5 g [VS] L −1 durante 25 días. El sustrato tiene un rendimiento final de metano de 350 mL g −1 [VS] degradado. Determinar la concentración del sustrato biodegradable en el efluente y la cantidad total de metano producido a lo largo de 25 días si la constante de velocidad cinética de degradación de primer orden es de 0.12 días −1.
Solución
Solución:
La concentración del VS biodegradable en el efluente del digestor se puede calcular usando la Ecuación 1.2.4:
\( S=S_{0}e^{-kt} \)(Ecuación\(\PageIndex{4}\))
Después de un día de digestión, la concentración de VS es:
\( S=5[e^{-0.12(1)}]=4.434 \ \text{g} \ \text{L}^{-1} \)
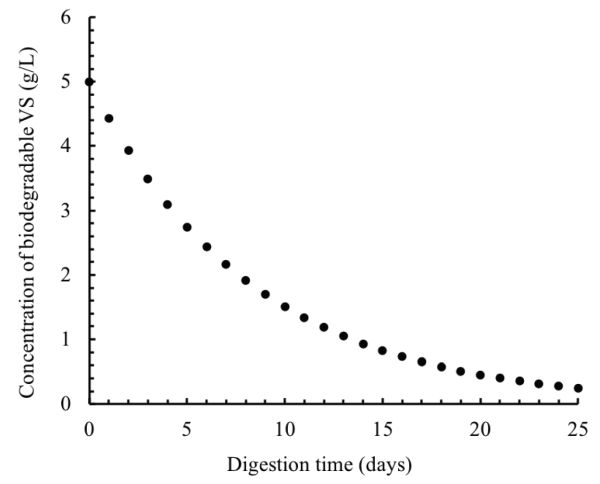
Este cálculo puede repetirse por cada día a lo largo del tiempo de digestión (25 días). Los resultados de estos cálculos se trazan en la Figura\(\PageIndex{11}\).
Las cantidades de materia orgánica degradada y metano producidos pueden predecirse usando las Ecuaciones 1.2.5 y 1.2.6. Después de un día de la digestión, estas cantidades se pueden calcular como:
\( S_{deg}=V_{w}(S_{0}-S) \)(Ecuación\(\PageIndex{5}\))
\( S_{deg}=5(5-4.434)=2.83 \ \text{g} \)
\( M_{p}=M_{y}S_{deg} \)(Ecuación\(\PageIndex{6}\))
\( M_{p}=350 \times 2.83 = 989.45 \ \text{mL} =0.9894 \ \text{L} \)
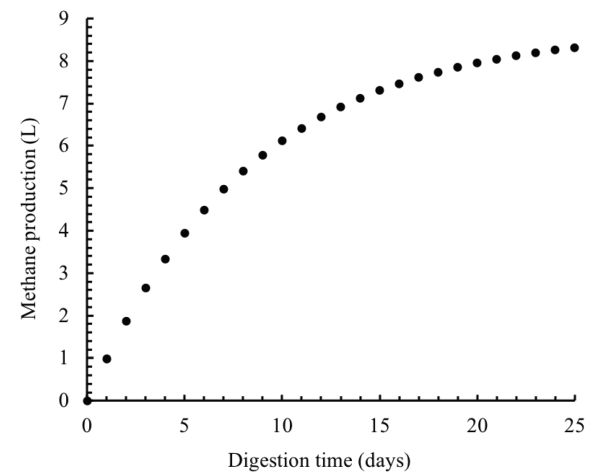
Estos cálculos se pueden repetir por cada día a lo largo del tiempo de digestión (25 días). Los resultados de estos cálculos se trazan en la Figura\(\PageIndex{12}\).
Créditos de imagen
Figura 1. El Mashad, H. & Zhang, R. (CC Por 4.0). (2020). Los pasos de la digestión anaeróbica de materia orgánica compleja en biogás (derivado de Pavlostathis y Giraldo-Gomez, 1991 y El Mashad, 2003).
Figura 2. El Mashad, H. & Zhang, R. (CC Por 4.0). (2020). Un esquema de digestor anaerobio de crecimiento suspendido.
Figura 3. El Mashad, H. & Zhang, R. (CC Por 4.0). (2020). Un esquema de un digestor de flujo pistón.
Figura 4. El Mashad, H. & Zhang, R. (CC Por 4.0). (2020). Un esquema de un filtro anaeróbico.
Figura 5. El Mashad y Zhang. (CC By 4.0). (2020). Tasa de crecimiento relativo de metanógenos en condiciones psicrófilas, mesofílicas y termófilas (derivado de Lettinga, et al., 2001. https://www.sciencedirect.com/science/article/pii/S0167779901017012#FIG1)
Figura 6. El Mashad, H. y Zhang, R. (CC Por 4.0). (2020). Actividad relativa de arqueas metanogénicas a diferentes pH (derivada de Speece, 1996; Khanal, 2008).
Figura 7. El Mashad, H. & Zhang, R. (CC Por 4.0). (2020). Esquema de una configuración experimental de un sistema digestor discontinuo.
Figura 8. Control de Bioprocesos. (2020). Configuración experimental del Sistema Automatizado de Prueba de Potencial Metano (AMPTS) Adaptado de https://www.bioprocesscontrol.com/. [Uso justo].
Figura 9. El Mashad, H. & Zhang, R. (CC Por 4.0). (2020). Producción diaria de biogás y rendimiento acumulado de biogás de residuos de comida de cafetería.
Figura 10. El Mashad, H. & Zhang, R. (CC Por 4.0). (2020). Rendimiento de metano de desechos orgánicos seleccionados.
Figura 11. El Mashad, H. & Zhang, R. (CC Por 4.0). (2020). Concentración de VS biodegradable en el digestor.
Figura 12. El Mashad, H. & Zhang, R. (CC Por 4.0). (2020). Producción total de metano acumulado.
Referencias
Angelidaki, I., & Sanders, W. (2004). Evaluación de la biodegradabilidad anaeróbica de macrocontaminantes. Rev. Environ. Sci. Biotechnol. , 3 (2), 117-129.
Batstone, D. J., Keller, J., Angelidaki, I., Kalyuzhnui, S. V., Pavlostanthis, S. G., Rozzi, A.,. Vavilin, V. A. (2002). Digestión Anaeróbica Modelo No. 1. Grupo de trabajo IWA para modelización matemática de procesos de digestión anaeróbica. Londres: IWA Publishing.
Buswell, A. M., & Mueller, H. F. (1952). Mecanismo de fermentación de metano. Ind. Ing. Chem. , 44 (3), 550-552. https://doi.org/10.1021/ie50507a033.
Coca-Cola, C. (2018). Inyección por tubería de biometano en California. BioCiclo, 59 (3), 32. Recuperado de https://www.biocycle.net/2018/03/12/pipeline-injection-biomethane-california/.
Coombs, J. (1990). El presente y futuro de la digestión anaerobia. En A. Wheatley (Ed.), Digestión anaeróbica: Una tecnología de tratamiento de residuos. Rep. Crítico Appl. Chem. , 31, 93-138.
El Mashad, H. M. (2003). Reactor anaerobio termofílico solar (STAR) para la producción de energía renovable. Tesis de doctorado. Países Bajos: Universidad de Wageningen. Recuperado de edepot.wur.nl/121501.
Hobson, P. N., & Richardson, A. J. (1983). La microbiología de la digestión anaerobia. En B. F. Pain & R. Q. Hepherd (Eds.), Digestión anaeróbica de residuos agrícolas. Boletín Técnico 7. Reading, Reino Unido: El Instituto Nacional de Investigación en Lácteos.
Khanal, S. K. (2008). Biotecnología anaeróbica para la producción de bioenergía: Principios y aplicaciones. Ames, IA: Wiley-Blackwell.
Kosaric, N., & Blaszczyk, R. (1992). Procesamiento industrial de efluentes. En: J. Lederberg (Ed.), Enciclopedia de microbiología (Vol. 2, pp. 473—491). Nueva York, NY: Prensa Académica.
Lettinga, G., Rebac, S., & Zeeman, G. (2001). Desafío del tratamiento de aguas residuales psicrófilas anaerobias. Tendencias en Biotechnol. 19 (9), 363-370. https://doi.org/10.1016/S0167-7799(01)01701-2.
Pavlostathis, S. G,. & Giraldo-Gómez, E. (1991). Cinética del tratamiento anaeróbico: Una revisión crítica. Crítico. Rev. Environ. Control, 21 (5/6), 411-490. https://doi.org/10.1080/10643389109388424.
Speece, R. E. (1996). Biotecnología anaeróbica para tratamientos de aguas residuales industriales. Nashville, TN: Prensa Archae.
Stanier, R. Y., Doudoroff, M., & Adelberg, E. A. (1972). Microbiología general. Englewood Cliffs, NJ: Prentice-Hall.
Stetter, K. O. (1996). Procariotos hipertermófilos. FEMS Microbiol. Rev., 18, 149-158. https://doi.org/10.1111/j.1574-6976.1996.tb00233.x.
Zhang, M. (2017). Recuperación de energía y nutrientes a partir de desechos orgánicos mediante digestión anaeróbica y tratamiento de digestatos. Doctorado diss. Davis, CA: Universidad de California, Davis.


