3.4: Otras unidades para concentraciones de soluciónes
- Page ID
- 1814
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)habilidades para desarrollar
- Definir las unidades de concentración de porcentaje de masa, porcentaje de volumen, porcentaje de volumen de masa, partes por millón (ppm) y partes por billón (ppb)
- Hacer calculaciones que relacionan la concentración de una solución y los volúmenes y/o masas de sus componentes usando estas unidades
En la sección anterior, introducimos la molaridad, una unidad de medida muy útil para evaluar la concentración de soluciones. Sin embargo, la molaridad es solo una medida de concentración. En esta sección, presentaremos otras unidades de concentración que se usan comúnmente en varias aplicaciones, ya sea por conveniencia o por convención.
El porcentaje de masa
Anteriormente en este capítulo, presentamos la composición porcentual como una medida de la cantidad relativa de un elemento dado en un compuesto. Los porcentajes también se usan comúnmente para expresar la composición de mezclas y soluciones. El porcentaje de masa de un componente de la solución se define como la relación de la masa del componente a la masa de la solución, expresada como un porcentaje:
\[ \text{mass percentage} = \dfrac{\text{mass of component}}{\text{mass of solution}} \times100\% \label{3.5.1}\]
En general, estamos más interesados en los porcentajes de masa de solutos, pero también es posible calcular el porcentaje de masa del solvente.
El porcentaje de masa también se conoce con nombres similares, como porcentaje de masa, porcentaje de peso, peso/porcentaje de peso, y otras variaciones sobre este tema. El símbolo más común para el porcentaje de masa es simplemente el signo de porcentaje,%, aunque a veces se usan símbolos más detallados que incluyen% masa,% peso y (w/w)%. El uso de estos símbolos más detallados puede evitar la confusión de los porcentajes en masa con otros tipos de porcentajes, como los porcentajes en volumen (que se analizarán más adelante en esta sección).
Los porcentajes de masa son unidades de concentración populares para productos de consumo. La etiqueta de una botella típica de blanqueador (Figura \(\PageIndex{1}\)) indica que la concentración de su ingrediente activo, hipoclorito de sodio (NaOCl), es del 7,4%. Por lo tanto, una muestra de 100,0 g de blanqueador contendría 7,4 g de NaOCl.

Ejemplo \(\PageIndex{1}\): Cálculo del Porcentaje de Masa
Una muestra de 5,0 g de líquido espinal contiene 3,75 mg (0,00375 g) de glucosa. ¿Cuál es el porcentaje de masa de glucosa en el fluido espinal?
Solución
La muestra de líquido espinal contiene aproximadamente 4 mg de glucosa en 5000 mg de líquido, por eso la fracción de masa de glucosa debe ser un poco menos que una parte en 1000, o aproximadamente el 0.1%. Sustituyendo las masas dadas en la ecuación definiendo los rendimientos porcentuales de masa:
\[\mathrm{\%\,glucose=\dfrac{3.75\;mg \;glucose \times \frac{1\;g}{1000\; mg}}{5.0\;g \;spinal\; fluid}=0.075\%}\]
El porcentaje de masa calculado está de acuerdo con nuestra estimación aproximada (es un poco menos del 0,1%).
Tenga en cuenta que, aunque cualquier unidad de masa se puede usar para calcular un porcentaje de masa (mg, g, kg, oz, etc.), se debe usar la misma unidad para el soluto y para la solución, para que las unidades de masa se cancelen, lo que da como resultado relación adimensional. En este caso, convertimos las unidades de soluto en el numerador de mg a g para que coincidan con las unidades en el denominador. Podríamos haber convertido el denominador de g a mg con la misma facilidad. Mientras se usen unidades de masa idénticas para el soluto y para la solución, el porcentaje de masa calculado será correcto.
Ejercicio \(\PageIndex{1}\)
Una botella de un limpiador de azulejos contiene 135 g de HCl y 775 g de agua. ¿Cuál es el porcentaje de masa de HCl en este limpiador?
- Respuesta
-
14,8%
Ejemplo \(\PageIndex{2}\): CÁLCULOS USANDO PORCENTAJE DE MASA
El ácido clorhídrico "concentrado" es una solución acuosa de HCl al 37,2% que se usa comúnmente como reactivo de laboratorio. La densidad de esta solución es de 1,19 g / mL. ¿Qué masa de HCl está contenida en 0,500 L de esta solución?
Solución
La concentración de HCl es alrededor de 40%, por eso una porción de 100 g de esta solución contendría aproximadamente 40 g de HCl. Ya que la densidad de la solución no es muy diferente de la del agua (1 g/ml), una estimación razonable de la masa de HCl en 500 g (0,5 L) de la solución es aproximadamente cinco veces más que en una porción de 100 g o \(\mathrm{5\times40=200\:g}\). Para derivar la masa de soluto en una solución de su porcentaje de masa, necesitamos saber la masa correspondiente de la solución. Usando la densidad de solución dada, podemos convertir el volumen de la solución a masa, y luego usar el porcentaje de masa dado para calcular la masa del soluto. Este enfoque matemático se describe en este diagrama de flujo:
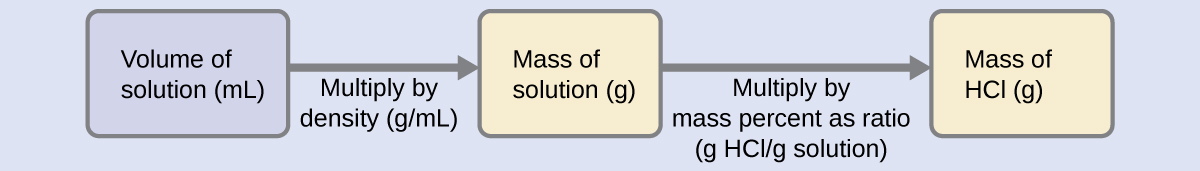
Para una cancelación adecuada de unidades, el volumen de 0,500-L se convierte a 500 mL, y el porcentaje de masa se expresa como una proporción, 37,2 g de solución de HCl/g:
\[ \mathrm{500\; mL\; solution \left(\dfrac{1.19\;g \;solution}{mL \;solution}\right) \left(\dfrac{37.2\;g\; HCl}{100\;g \;solution}\right)=221\;g\; HCl}\]
Esta masa de HCl es consistente con nuestra estimación de aproximadamente 200 g.
Ejercicio \(\PageIndex{2}\)
¿Qué volumen de solución de HCl concentrado contiene 125 g de HCl?
- Respuesta
-
282 mL
El porcentaje de volumen
Los volúmenes de líquidos en un amplio rango de magnitudes se miden convenientemente usando equipos de laboratorio comunes y relativamente económicos. La concentración de una solución formada por disolviendo un soluto líquido en un solvente líquido a veces se expresa como un porcentaje en volumen,% vol o (v/v)%:
Ejemplo \(\PageIndex{3}\): CÁLCULOS USANDO EL PORCENTAJE DE VOLUMEN
El alcohol de frotamiento (isopropanol) se vende generalmente como una solución acuosa al 70% vol. Si la densidad del alcohol isopropílico es de 0,785 g/mL, ¿Cuántos gramos de alcohol isopropílico hay en una botella de 355 mL de alcohol?
Solución
Según la definición de porcentaje de volumen, el volumen de isopropanol es el 70% del volumen total de la solución. Al multiplicar el volumen de isopropanol por su densidad, se obtiene la masa solicitada:
Ejercicio \(\PageIndex{3}\)
El vino contiene aproximadamente 12% de etanol (\(\ce{CH_3CH_2OH}\)) por volumen. El etanol tiene una masa molar de 46,06 g/mol y una densidad de 0,789 g/mL. ¿Cuántos moles de etanol hay en una botella de vino de 750 mL?
- Respuesta
-
1,5 mol de etanol
El porcentaje de volumen-masa
Las unidades porcentuales "mixtas", derivadas de la masa de soluto y el volumen de solución, son populares para ciertas aplicaciones bioquímicas y médicas. Un porcentaje de volumen de masa es una relación de la masa de un soluto al volumen de la solución, expresada como un porcentaje. Las unidades específicas usadas para la masa del soluto y el volumen de la solución pueden variar, dependiendo de la solución. Por ejemplo, la solución de salina fisiológica, usada para preparar líquidos por vía intravenosa, tiene una concentración de 0,9% de masa/volumen (m/v), esto indica que la composición es de 0,9 g de soluto por cada 100 mL de solución. La concentración de glucosa en la sangre (comúnmente conocida como "azúcar en la sangre") también se expresa típicamente en términos de una relación de masa-volumen. Aunque no se expresa explícitamente como un porcentaje, normalmente su concentración se da en miligramos de glucosa por decilitro (100 mL) de sangre (Figura \(\PageIndex{2}\)).

Partes por millón y partes por billón
A veces, las concentraciones muy bajas de soluto se expresan usando unidades apropiadamente pequeñas, como partes por millón (ppm) o partes por billón (ppb). Como las unidades de porcentaje ("parte por cien"), ppm y ppb se pueden definir en términos de masas, volúmenes o unidades de volumen de masas mixtas. También hay unidades de ppm y ppb definidas con respecto a la cantidad de átomos y moléculas.
Las definiciones basadas en masa de ppm y ppb se dan aquí:
\[\text{ppm}=\dfrac{\text{mass solute}}{\text{mass solution}} \times 10^6\; \text{ppm} \label{3.5.3A}\]
\[\text{ppb}=\dfrac{\text{mass solute}}{\text{mass solution}} \times 10^9\; \text{ppb} \label{3.5.3B}\]
Ambas unidades de ppm y ppb son convenientes para informar las concentraciones de contaminantes y otros contaminantes traza en el agua. Las concentraciones de estos contaminantes son típicamente muy bajas en aguas tratadas y naturales, y sus niveles no pueden exceder los umbrales de concentración relativamente bajos sin causar efectos adversos en la salud y la vida silvestre. Por ejemplo, la EPA ha identificado que el nivel máximo seguro de ión fluoruro en el agua del grifo es de 4 ppm. Los filtros de agua en línea están diseñados para reducir la concentración de fluoruro y varios otros contaminantes a nivel de trazas en el agua del grifo (Figura \(\PageIndex{3}\)).

Ejemplo \(\PageIndex{4}\): PARTES POR MILLÓN Y PARTES POR BILLONES DE CONCENTRACIONES
Según la EPA, cuando la concentración de plomo en el agua del grifo alcanza las 15 ppb, se deben tomar ciertas acciones correctivas. ¿Cuál es esta concentración en ppm? A esta concentración, ¿Qué masa de plomo (μg) estaría contenida en un vaso de agua típico (300 mL)?
Solución
Las definiciones de las unidades de ppm y ppb se pueden usar para convertir una concentración dada de ppb a ppm. Comparando estas dos definiciones de unidades muestra que ppm es 1000 veces más que ppb (1 ppm = 103 ppb). Así:
\[ \mathrm{15\; \cancel{ppb} \times \dfrac{1\; ppm}{10^3\;\cancel{ppb}} =0.015\; ppm}\]
La definición de la unidad ppb se puede usar para calcular la masa solicitada si la masa de la solución se da. Sin embargo, solamente el volumen de la solución se da (300 mL), por eso debemos usar la densidad para derivar la masa correspondiente. Podemos asumir que la densidad del agua del grifo es similar a la densidad del agua pura (1,00 g/mL), ya que las concentraciones de cualquier sustancia disuelta no deben ser muy grandes. Reorganizando la ecuación definiendo la unidad de ppb y sustituyendo los rendimientos de las cantidades dadas:
\[\text{ppb}=\dfrac{\text{mass solute}}{\text{mass solution}} ×10^9\; \text{ppb}\]
\[\text{mass solute} = \dfrac{\text{ppb} \times \text{mass solution}}{10^9\;\text{ppb}}\]
\[\text{mass solute}=\mathrm{\dfrac{15\:ppb×300\:mL×\dfrac{1.00\:g}{mL}}{10^9\:ppb}=4.5 \times 10^{-6}\;g}\]
Finalmente, convirtiendo esta masa a la unidad solicitada de microgramos:
\[\mathrm{4.5 \times 10^{−6}\;g \times \dfrac{1\; \mu g}{10^{−6}\;g} =4.5\; \mu g}\]
Ejercicio \(\PageIndex{4}\)
Se determinó que una muestra de 50,0 g de aguas residuales industriales contenía 0,48 mg de mercurio. Exprese la concentración de mercurio de las aguas residuales en unidades de ppm y ppb.
- Respuesta
-
9,6 ppm, 9600 ppb
Resumen
Además de la molaridad, una serie de otras unidades de concentración de la solución se usan en diversas aplicaciones. Las concentraciones porcentuales basadas en las masas, los volúmenes, o ambos de los componentes de la solución son útiles para expresar concentraciones relativamente altas, mientras que las concentraciones más bajas se expresan convenientemente usando unidades de ppm o ppb. Estas unidades son populares en campos ambientales, médicos, y otros en donde las unidades basadas en moles, como la molaridad, no se usan tan comúnmente.
Glosario
- porcentaje de masa
- Relación de masa de soluto a solución expresada como porcentaje.
- partes por billones (ppb)
- Relación de masa de soluto a solución multiplicada por 109
- partes por millón (ppm)
- Relación de masa de soluto a solución multiplicada por 106
- porcentaje de volumen
- Relación de volumen de soluto a solución expresada como porcentaje.
- porcentaje de volumen de masa
- Relación de masa de soluto a volumen de solución, expresada como un porcentaje.
Contribuyentes
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


