12.3: Los factores que afectan las tasas de reacción
- Page ID
- 1895
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)habilidades para desarrollar
- Describir los efectos del carácter químico, el estado físico, la temperatura, la concentración y la catálisis en las tasas de las reacción.
Las velocidades a las que se consumen los reactivos y los productos que se forman durante una reacción química varían mucho. Podemos identificar cinco factores que afectan las tasas de las reacciones químicas: el carácter químico de las sustancias que reaccionan, el estado de subdivisión (un bulto grande versus muchas partículas pequeñas) de los reactivos, la temperatura de los reactivos, la concentración de los reactivos, y la presencia de un catalizador.
El carácter químico de las sustancias que reaccionan
La velocidad de una reacción depende de las características de las sustancias participantes. Las reacciones que parecen similares pueden tener diferentes velocidades en las mismas condiciones, dependiendo de la identidad de los reactivos. Por ejemplo, cuando pequeñas piezas de los metales hierro y sodio están expuestas al aire, el sodio reacciona completamente con el aire durante la noche, mientras que el hierro apenas se ve afectado. Los metales activos de calcio y sodio reaccionan con el agua para formar el hidrógeno gaseoso y una base. Sin embargo, el calcio reacciona a una tasa moderada mientras que el sodio reacciona tan rápidamente que la reacción es casi explosiva.
El estado de subdivisión de los reactivos
A excepción de las sustancias en estado gaseoso o en solución, las reacciones ocurren en el límite o interfaz entre dos fases. Por lo tanto, la velocidad de reacción entre dos fases depende en gran medida del contacto superficial entre ellas. Un sólido finamente dividido tiene más área de superficie disponible para la reacción que una pieza grande de la misma sustancia. Así, un líquido reaccionará más rápidamente con un sólido finamente dividido que con una pieza grande del mismo sólido. Por ejemplo, grandes piezas de hierro reaccionan lentamente con ácidos; el hierro finamente dividido reacciona mucho más rápidamente (Figura \(\PageIndex{1}\)). Las piezas grandes de madera arden lentamente, las piezas más pequeñas arden rápidamente y el polvo de la sierra arde explosivamente.

Video \(\PageIndex{1}\): La reacción del cesio con el agua en cámara lenta y una discusión sobre cómo el estado de los reactivos y el tamaño de las partículas afectan las velocidades de la reacción.
Temperatura de los reactivos
Las reacciones químicas en general ocurren más rápidamente a temperaturas más altas. Por ejemplo, la comida se puede echar a perder rápidamente cuando se deja en la encimera de la cocina. Sin embargo, la temperatura más baja dentro de un refrigerador ralentiza ese proceso para que la misma comida permanezca fresca durante días. Usamos un quemador o una placa caliente en el laboratorio para aumentar la velocidad de las reacciones que se producen lentamente a temperaturas normales. En muchos casos, un aumento de temperatura de solo 10 ° C duplicará aproximadamente la velocidad de una reacción en un sistema homogéneo.
Concentraciones de los reactivos
Las velocidades de muchas reacciones dependen de las concentraciones de los reactivos. Las tasas generalmente aumentan cuando aumenta la concentración de uno o más de los reactivos. Por ejemplo, el carbonato de calcio (\(\mathrm{CaCO_3}\)) se deteriora como resultado de su reacción con el dióxido de azufre contaminante. La velocidad de esta reacción depende de la cantidad de dióxido de azufre en el aire (Figura \(\PageIndex{2}\)). Como el óxido acidico, el dióxido de azufre se combina con el vapor de agua en el aire para producir ácido sulfuroso en la siguiente reacción:
\[\ce{SO}_{2(g)}+\ce{H_2O}_{(g)}⟶\ce{H_2SO}_{3(aq)} \label{12.3.1}\]
El carbonato de calcio reacciona con el ácido sulfuroso de la siguiente manera:
\[\ce{CaCO}_{3(s)}+\ce{H_2SO}_{3(aq)}⟶\ce{CaSO}_{3(aq)}+\ce{CO}_{2(g)}+\ce{H_2O}_{(l)} \label{12.3.2}\]
En una atmósfera contaminada donde la concentración de dióxido de azufre es alta, el carbonato de calcio se deteriora más rápidamente que en el aire menos contaminado. Del mismo modo, el fósforo se quema mucho más rápidamente en una atmósfera de oxígeno puro que en el aire, que es solo un 20% de oxígeno.

Figur \(\PageIndex{2}\): Las estatuas hechas de compuestos de carbonato, como la piedra caliza y el mármol, generalmente se desgastan lentamente con el tiempo debido a las acciones del agua y la expansión y contracción térmica. Sin embargo, los contaminantes como el dióxido de azufre pueden acelerar la meteorización. A medida que aumenta la concentración de contaminantes del aire, el deterioro de la piedra caliza se produce más rápidamente. (crédito: James P Fisher III).
Video \(\PageIndex{2}\): El fósforo se quema rápidamente en el aire, pero se quemará aún más rápidamente si la concentración de oxígeno es más alta.
La presencia de un catalizador
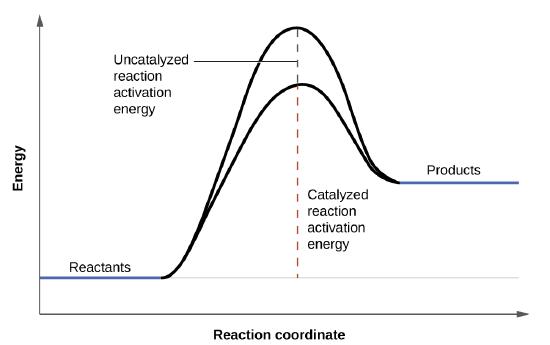
Las soluciones de peróxido de hidrógeno forman espuma cuando se vierten sobre una herida abierta porque las sustancias en los tejidos expuestos actúan como catalizadores, aumentando la velocidad de descomposición del peróxido de hidrógeno. Sin embargo, en ausencia de estos catalizadores (por ejemplo, en la botella en el botiquín), la descomposición completa puede llevar meses. Un catalizador es una sustancia que aumenta la velocidad de una reacción química al disminuir la energía de activación sin ser consumida por la reacción. La energía de activación es la cantidad mínima de energía requerida para que una reacción química avance en la dirección hacia adelante. Un catalizador aumenta la velocidad de reacción al proporcionar una vía o mecanismo alternativo para que la reacción siga (Figura \(\PageIndex{3}\)). La catálisis se discutirá con mayor detalle más adelante en este capítulo, ya que se relaciona con los mecanismos de reacción.
Las reacciones químicas ocurren cuando las moléculas chocan entre sí y experimentan una transformación química. Antes de realizar físicamente una reacción en un laboratorio, los científicos pueden usar simulaciones de modelado molecular para predecir cómo los parámetros discutidos anteriormente influirán en la velocidad de una reacción. Utilice el interactivo de Reacciones y tasas de PhET para explorar cómo la temperatura, la concentración y la naturaleza de los reactivos afectan las tasas de reacción.
Resumen
La velocidad de una reacción química se ve afectada por varios parámetros. Las reacciones que involucran dos fases proceden más rápidamente cuando hay un mayor contacto del área superficial. Si aumenta la temperatura o la concentración de un reactivo, la velocidad de una reacción dada generalmente también aumenta. Un catalizador puede aumentar la velocidad de una reacción al proporcionar una vía alternativa que hace que disminuya la energía de activación de la reacción.
Glosario
- Catalizador
- sustancia que aumenta la velocidad de una reacción sin ser consumida por la reacción
Contribuyentes
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


