18.2: La ocurrencia y preparación de los metales representativos
( \newcommand{\kernel}{\mathrm{null}\,}\)
Habilidades para desarrollar
- Identificar los orígenes naturales de los metales representativos
- Describir los procesos de reducción química y electrolítica usada para preparar estos elementos a partir de los orígenes naturales
Debido a su reactividad, no encontramos los metales más representativos como los elementos libres en la naturaleza. Sin embargo, los compuestos que contienen los iones de los metales más representativos están en abundancia. En esta sección, consideraremos las dos técnicas más comunes que se usan para aislar los metales de estos compuestos: la electrólisis y reducción química.
Estos metales se encuentran principalmente en los minerales, con el litio en los minerales de silicato o fosfato, y el sodio y el potasio en depósitos de sal de la evaporación de mares antiguos y en silicatos. Los metales alcalinotérreos se presentan como silicatos y, con la excepción del berilio, como carbonatos y sulfatos. El berilio se presenta como el mineral berilo, Be3Al2Si6O18, que, con ciertas impurezas, puede ser la piedra preciosa esmeralda o aguamarina. El magnesio se encuentra en el agua de mar y, junto con los metales alcalinotérreos más pesados, se presenta como silicatos, carbonatos y sulfatos. El aluminio se encuentra abundantemente en muchos tipos de arcilla y en la bauxita, un hidróxido de óxido de aluminio impuro. El principal mineral de estaño es el óxido de casiterita, SnO2, y el principal mineral de plomo y talio son los sulfuros o los productos de la meteorización de los sulfuros. Los metales representativos restantes se presentan como impurezas en minerales de zinc o aluminio.
La Electrolisis
Los iones de los metales de los grupos 1 y 2, junto con el aluminio, son muy difíciles de reducir; por lo tanto, es necesario preparar estos elementos por la electrólisis, un proceso importante que se analiza en el capítulo sobre la electroquímica. Brevemente, la electrólisis involucra el uso de la energía eléctrica para impulsar las reacciones químicas desfavorables; es útil en el aislamiento de los metales reactivos en sus formas puras. El sodio, el aluminio y el magnesio son ejemplos típicos.
La preparación del sodio
El método más importante para la producción del sodio es la electrólisis del cloruro de sodio fundido; se usa el proceso de Downs, que se muestra en la Figura 18.2.1. La reacción involucrada en este proceso es:
2NaCl(l)electrolysis→600°C2Na(l)+Cl2(g)
La celda de electrólisis contiene el cloruro de sodio fundido (con un punto de fusión 801 °C), al que se le ha agregado el cloruro de calcio para reducir el punto de fusión a 600 °C (un efecto coligativo). Pasando una corriente continua a través de la celda hace que los iones de sodio se muevan al cátodo, con una carga negativa y recojan electrones, reduciendo los iones a sodio metálico. Los iones de cloruro se mueven al ánodo con una carga positiva, pierden electrones y se oxidan a cloro gaseoso. La reacción de celda general viene de agregar las siguientes reacciones:
La separación del sodio y el cloro fundidos evita que la recombinación ocurra. El sodio líquido, que es menos denso que el cloruro de sodio fundido, flota hacia la superficie y fluye hacia un colector. El cloro gaseoso va a los tanques de almacenamiento. El cloro también es un producto importante.
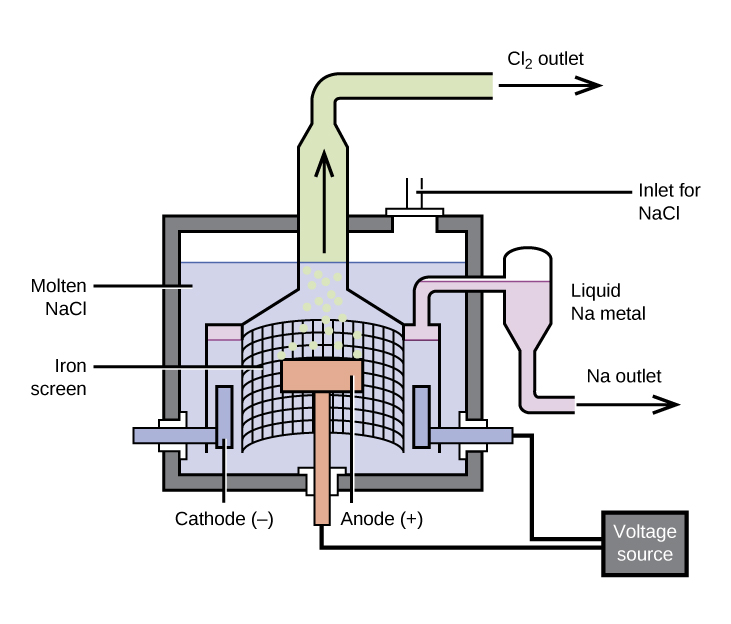
Figura18.2.1: El sodio metálico puro se aísla usando la electrólisis de cloruro de sodio fundido usando el proceso de Downs. No es posible aislar el sodio por la electrólisis de soluciones acuosas de sales de sodio porque los iones de hidrógeno se reducen más fácilmente que los iones de sodio; como resultado, se forma el hidrógeno en el cátodo en lugar del metal de sodio deseado. La alta temperatura requerida para fundir el NaCl significa que se forma el sodio metálico en la forma de un líquido.
La preparación del aluminio
La preparación del aluminio usa un proceso inventado en 1886 por Charles M. Hall, quien comenzó a trabajar en el problema mientras estudiaba en Oberlin College ubicado en Ohio. Paul L. T. Héroult descubrió el proceso independiente uno o dos meses más tarde en Francia. En honor a los dos inventores, esta celda de electrólisis se conoce como la celda Hall-Héroult. La celda Hall – Héroult es una celda de electrólisis para la producción del aluminio. La figura 18.2.2 ilustra la celda Hall – Héroult.
La producción del aluminio comienza con la purificación de la bauxita, la fuente más común de aluminio. La reacción de la bauxita, AlO(OH), con el hidróxido de sodio caliente forma aluminato de sodio soluble, mientras que la arcilla y otras impurezas permanecen sin disolver:
AlO(OH)(s)+NaOH(aq)+H2O(l)⟶Na[Al(OH)4](aq)
Después de la eliminación de las impurezas usando la filtración, la adición del ácido al aluminato causa la reprecipitación del hidróxido de aluminio:
Na[Al(OH)4](aq)+H3O+(aq)⟶Al(OH)3(s)+Na+(aq)+2H2O(l)
El siguiente paso es eliminar el hidróxido de aluminio precipitado usando la filtración. El calentamiento del hidróxido produce el óxido de aluminio, Al2O3, que se disuelve en una mezcla fundida de criolita, Na3AlF6 y fluoruro de calcio, CaF2. La electrólisis de esta solución ocurre en una celda como la que se muestra en la Figura 18.2.2. La reducción de los iones de aluminio al metal se produce en el cátodo, mientras se forma el oxígeno, monóxido de carbono y dióxido de carbono en el ánodo.
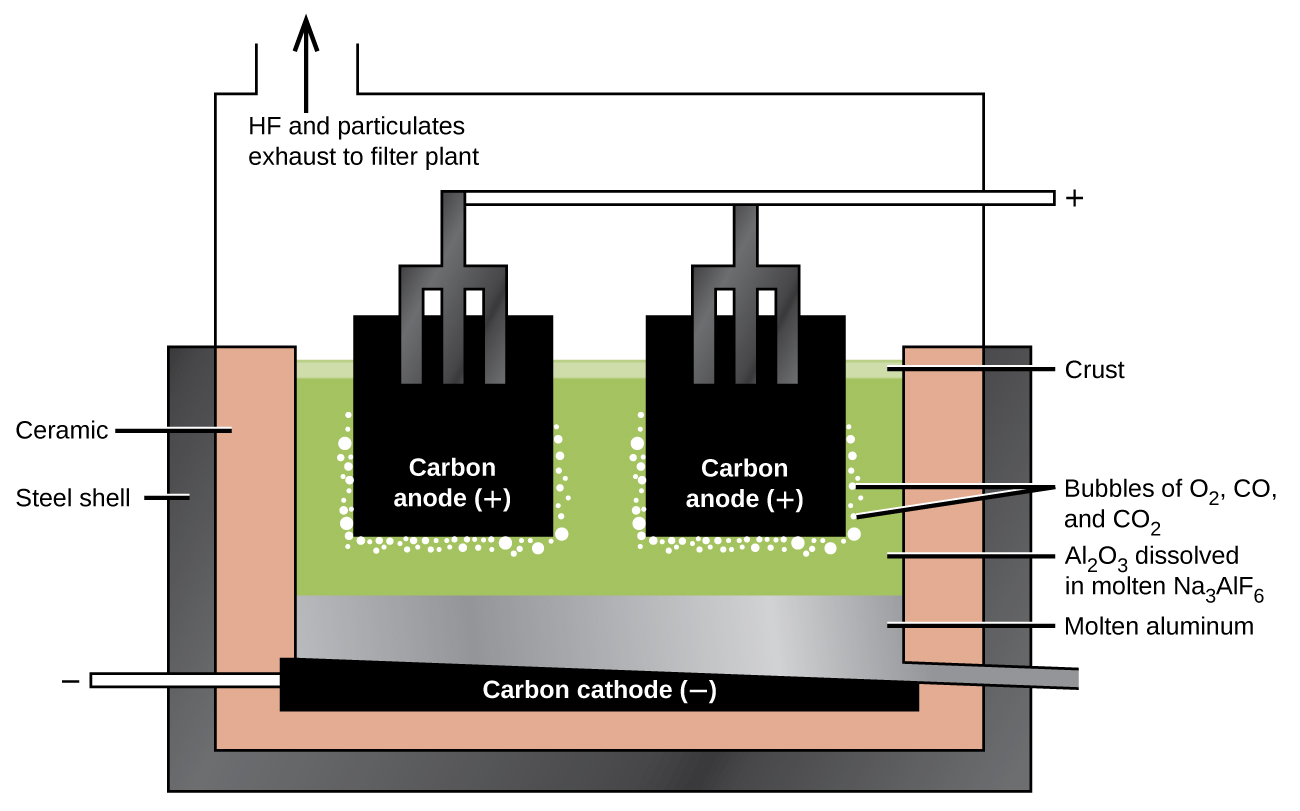
Figura 18.2.2: Se usa una celda electrolítica para la producción del aluminio. La electrólisis de una solución de criolita y fluoruro de calcio produce el aluminio metálico en el cátodo y el oxígeno, monóxido de carbono y dióxido de carbono en el ánodo.
La preparación del magnesio
El magnesio es el otro metal que se aísla en grandes cantidades por la electrólisis. El agua de mar, que contiene aproximadamente un 0.5% de cloruro de magnesio, es la fuente principal del magnesio. La adición del hidróxido de calcio al agua de mar precipita el hidróxido de magnesio. La adición del ácido clorhídrico al hidróxido de magnesio, seguido por la evaporación de la solución acuosa resultante, deja cloruro de magnesio puro como uno producto. La electrólisis del cloruro de magnesio fundido forma el magnesio líquido y el cloro gaseoso:
MgCl2(aq)+Ca(OH)2(aq)⟶Mg(OH)2(s)+CaCl2(aq)
Mg(OH)2(s)+2HCl(aq)⟶MgCl2(aq)+2H2O(l)
MgCl2(l)⟶Mg(l)+Cl2(g)
Algunas instalaciones de producción se han parado de usar la electrólisis completamente. En la siguiente sección, veremos cómo el proceso Pidgeon causa la reducción química del magnesio.
La reducción química
Es posible aislar muchos de los metales representativos mediante una reducción química usando otros elementos como agentes reductores. En general, la reducción química es más barata que la electrólisis y, por esta razón, la reducción química es el método de elección para el aislamiento de estos elementos. Por ejemplo, es posible producir el potasio, rubidio y cesio por la reducción química, ya que es posible reducir los cloruros fundidos de estos metales con el sodio metálico. Esto puede ser sorprendente porque estos metales son más reactivos que el sodio; sin embargo, los metales formados son más volátiles que el sodio y se pueden destilar para su recolección. La eliminación del vapor de metal causa un cambio en el equilibrio para producir más metal (a través del principio de Le Chatelier). La producción del magnesio, zinc y estaño y nos da ejemplos adicionales de la reducción química.
La preparación del magnesio
El proceso Pidgeon involucra la reacción de óxido de magnesio con el silicio elemental a altas temperaturas para formar el magnesio puro:
\ce{Si}(s)+\ce{2MgO}(s)\xrightarrow{Δ}\ce{SiO2}(s)+\ce{2Mg}(g)
Aunque esta reacción es desfavorable en términos de la termodinámica, la eliminación del vapor de magnesio producido se aprovecha del principio de Le Chatelier para continuar el progreso de la reacción. Más del 75% de la producción mundial de magnesio, principalmente en China, proviene de este proceso.
La preparación del zinc
Los minerales de zinc generalmente contienen el sulfuro de zinc, óxido de zinc o carbonato de zinc. Después de la separación de estos compuestos de los minerales, el calentamiento en el aire convierte el mineral en óxido de zinc mediante una de las siguientes reacciones:
\ce{2ZnS}(s)+\ce{3O2}(g)\xrightarrow{Δ}\ce{2ZnO}(s)+\ce{2SO2}(g)
\ce{ZnCO3}(s)\xrightarrow{Δ}\ce{ZnO}(s)+\ce{CO2}(g)
El carbono, en forma de carbón, reduce el óxido de zinc para formar el vapor de zinc:
\ce{ZnO}(s)+\ce{C}(s)⟶\ce{Zn}(g)+\ce{CO}(g)
El zinc se puede destilar (punto de ebullición 907 °C) y condensar. Este zinc contiene impurezas de cadmio (767 °C), hierro (2862 ° C), plomo (1750 ° C) y arsénico (613 ° C). La redestilación cuidadosa produce el zinc puro. El arsénico y el cadmio se destilan del zinc porque tienen puntos de ebullición más bajos. A temperaturas más altas, el zinc se destila de las otras impurezas, principalmente plomo y hierro.
La preparación del estaño
La reducción rápida del óxido de estaño (IV) por las brasas calientes de una fogata fue el conocimiento del estaño en el mundo antiguo. En el proceso moderno, el tostado de minerales de estaño que contienen SnO2 elimina contaminantes como el arsénico y el azufre como óxidos volátiles. El tratamiento del material que sobra con el ácido clorhídrico elimina los óxidos de otros metales. Calentando el mineral purificado con el carbón a una temperatura superior a 1000°C produce el estaño:
\ce{SnO2}(s)+\ce{2C}(s)\xrightarrow{Δ}\ce{Sn}(s)+\ce{2CO}(g)
El estaño fundido se acumula en el fondo del horno y se extrae y se hace en bloques.
Resumen
Debido a su reactividad química, es necesario producir los metales representativos en sus formas puras usando la reducción de los compuestos naturales. La electrólisis es importante en la producción del sodio, potasio y aluminio. La reducción química es el método principal para el aislamiento del magnesio, zinc y estaño. Procedimientos similares son importantes para los otros metales representativos.
Glosario
- reducción química
- método de preparación de un metal representativo usando un agente reductor
- Proceso de Downs
- Una celda electroquímica usada para la preparación comercial del sodio metálico (y cloro) a partir de cloruro de sodio fundido
- Celda Hall – Héroult
- Aparato de electrólisis usado para aislar el metal de aluminio puro de una solución de alúmina en criolita fundida
- Proceso Pidgeon
- proceso de reducción química usado para producir el magnesio a través de la reacción térmica de óxido de magnesio con silicio
Contribuyentes y Atribuciones
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


