21.1: Introducción al Estudio de Superficies
- Page ID
- 78802
Hasta ahora hemos considerado métodos para analizar las propiedades de volumen de las muestras, como determinar la identidad o concentración de un ion en una solución, de una molécula en un gas, o de varios elementos en un sólido. Al hacerlo, no nos preocupamos por la homogeneidad o heterogeneidad de la muestra. En este capítulo consideramos cómo podemos recopilar información sobre la composición de la superficie de una muestra y cómo difiere de la composición a granel de la muestra. Pero primero, consideremos varias preguntas importantes.
¿Qué es una superficie?
Una superficie es un límite, o interfaz, entre dos fases, como un sólido y un gas (el tipo de interfaz de particular interés para nosotros en este capítulo). Esta es una descripción útil, pero no suficiente. También es de interés la cuestión de la profundidad. ¿Una superficie es solo la capa más externa de átomos, iones o moléculas, o extiende varias capas en la muestra? ¿De qué manera podría diferir la composición de una muestra en la superficie de su composición en el interior a granel de la muestra? Y, ¿qué pasa con las variaciones en la composición a través de una superficie? ¿La superficie misma es homogénea o heterogénea en su composición? Diferentes métodos analíticos muestrearán la superficie a diferentes profundidades y con diferentes áreas superficiales, lo que significa que el volumen de muestra analizada variará de método a método. Por esta razón, solemos definir la superficie de una muestra como lo que se analiza mediante el método analítico que estamos utilizando.
¿Por qué son las superficies de interés?
La figura\(\PageIndex{1}\) muestra la estructura cristalina de AgCl (s), que consiste en un patrón repetitivo de iones Ag + y iones Cl —. Si miras los iones en el interior de la estructura, verás que cada ion Ag + está rodeado por seis iones Cl — y cada ion Cl — está rodeado por seis iones Ag +. En la superficie, sin embargo, vemos que los iones Cl — y los iones Ag + ya no están rodeados por seis iones de carga opuesta. Como resultado, los iones Ag + y los iones Cl — en la superficie son más reactivos químicamente que los del interior y pueden servir como sitios para una química interesante. Es probable que las propiedades químicas y físicas de la superficie de una muestra sean muy diferentes a las propiedades a granel de la muestra.
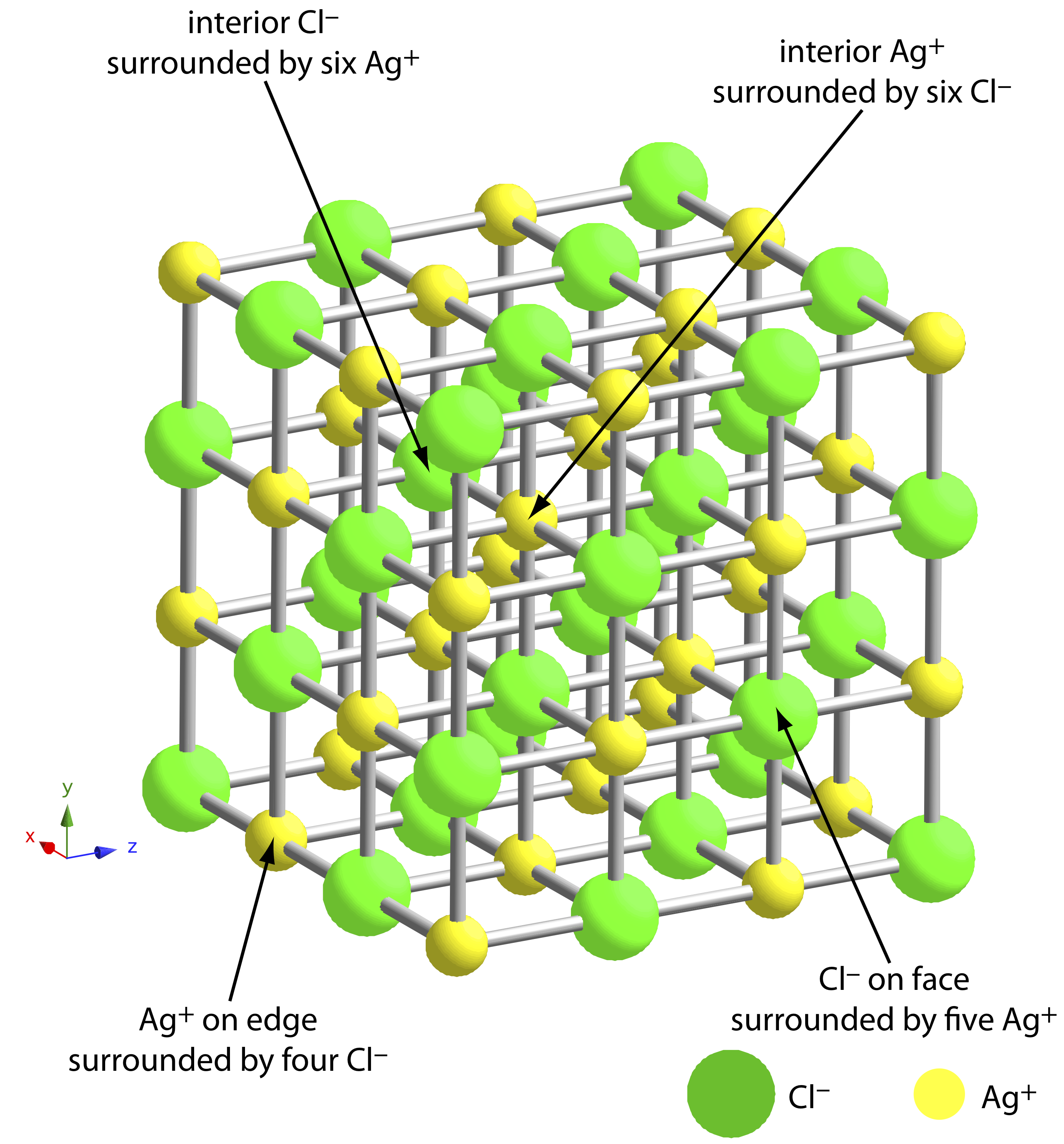
¿Qué desafíos presenta una superficie?
Supongamos que estamos interesados en estudiar la superficie de una pieza de zinc metálico utilizando una sonda que muestrea solo la capa más externa de átomos y que muestrea una superficie circular que es de 1 µm 2. ¿Cuántos átomos de Zn podríamos esperar que encuentre nuestra sonda? Aquí hay alguna información útil sobre el zinc: tiene una masa molar de 65.38 g/mol, tiene una densidad de 7.14 g/cm 3, y tiene un radio atómico de aproximadamente 0.13 nm. A partir de esto calculamos los átomos por unidad de volumen como
\[\frac{7.14 \text{ g}}{\text{cm}^{3}} \times \frac{100 \text{ cm}}{\text{m}} \times \frac{1 \text{m}}{10^9 \text{ nm}} \times \frac{1 \text{ mol}}{65.38 \text{ g}} \times \frac{6.002 \times 10^{23} \text{ atoms}}{\text{mol}} = \frac{6.6 \times 10^{15} \text{ atoms}}{\text{cm}^2 \text{ nm}} \nonumber \]
Las unidades en el denominador pueden parecerle extrañas, pero escribirlas de esta manera enfatiza que nos interesa tanto la profundidad desde la que se recibe la información (dada aquí en nanómetros, nm) como en la superficie de la que se recibe la información (dada aquí en centímetros cuadrados, cm 2). Multiplicar este valor por el grosor de una capa atómica de zinc, que es el doble de su radio atómico, sugiere que estamos analizando aproximadamente
\[\frac{6.6 \times 10^{15} \text{ atoms}}{\text{cm}^2 \text{ nm}} \times 0.26 \text{ nm} = 1.7 \times 10^{15} \frac{\text{atoms}}{\text{cm}^2} \nonumber \]
Si multiplicamos este valor por la superficie de la que estamos muestreando, entonces estamos interactuando con aproximadamente
\[ 1.7 \times 10^{15} \frac{\text{atoms}}{\text{cm}^2} \times \left(\frac{100 \text{ cm}^2}{\text{m}}\right)^2 \times \left(\frac{1 \text{m}}{10^6 \text{µm}} \right)^2 = 1.7 \times 10^7 \text{ atoms of Zn} \nonumber \]
Si bien 17 millones pueden parecer un número grande, no se trata de un número particularmente grande de átomos sobre los que realizar un análisis. Ahora, supongamos que la superficie tiene una impureza de 10 ppm de átomos de cobre; es decir, hay 10 átomos de cobre por cada 10 6 átomos de zinc. En este caso, nuestra sonda de la muestra involucra solo
\[1.7 \times 10^7 \text{ atoms of Zn} \times \frac{10 \text{ atoms of Cu}}{10^6 \text{ atoms of Zn}} = 170 \text{ atoms of Cu} \nonumber \]
Como comparación, si analizamos una muestra en la que el analito está presente a una concentración que está\(1 \times 10^{-6} \text{ mol/L}\) utilizando un método analítico que recopila información de un volumen que es de apenas 1 mm 3, entonces estamos muestreando
\[\frac{1 \times 10^{-6} \text{ mol}}{\text{L}} \times \frac{1 \text{L}}{1000 \text{ cm}^3} \times \left( \frac{1 \text{cm}}{10 \text{ mm}}\right)^3 \times 1 \text{ mm}^3 \times 6.022 \times 10^{23} \text{ mol}^{-1} = 6.0 \times 10^{11} \text{ particles of analyte} \nonumber \]
Un desafío adicional cuando intentamos analizar una superficie es que una superficie recién expuesta se contamina con una capa absorbida de moléculas de gas casi instantáneamente cuando se sienta en una mesa de laboratorio, y en unos pocos segundos a unos minutos a presiones en el rango de 10 a 6 torr a 10 —8 torr. El análisis de una superficie requiere una cuidadosa atención a cómo se prepara la superficie.
¿Qué oportunidades presenta una superficie?
En comparación con muchos de los métodos de los Capítulos 6-20 y en los Capítulos 22-34, el uso de una sonda que muestrea de un área pequeña permite mover la sonda a través de la superficie, esto se llama rasterización, desarrollando una imagen bidimensional de la superficie. Cuando se usa un haz energético que puede marcar un agujero en la muestra, podemos obtener información en profundidad, un proceso llamado perfil de profundidad, que proporciona información en una tercera dimensión. Estas son fortalezas particularmente importantes de los métodos analíticos de superficie.
¿Cómo podemos sondear la superficie?
Para estudiar una superficie, ponemos energía en ella en forma de haz de fotones, electrones o iones y luego medimos la energía que sale de la superficie en forma de haz de fotones, electrones o iones. \(\PageIndex{1}\)La tabla muestra algunas de las posibilidades. También se incluyen en esta tabla métodos en los que un campo aplicado genera una respuesta desde la superficie. Las entradas en negrita reciben atención en este capítulo. La espectroscopia Raman mejorada de superficie recibió una breve mención en el Capítulo 18. Tenga en cuenta que la espectroscopia electrónica Auger aparece dos veces ya que la emisión de electrones puede seguir la entrada de fotones de rayos X o electrones.
|
energía hacia fuera\(\rightarrow\) energía en\(\downarrow\) |
fotón | electrón | ion | campo |
|---|---|---|---|---|
| \ (\ fila derecha\) energía en\(\downarrow\) “>fotón |
espectroscopía Raman mejorada en superficie (SERS) Estructura fina de absorción extendida de rayos X (EXAFS) |
Espectroscopia fotoelectrónica de rayos X (XPS) Espectroscopia electrónica de barrena (AES) Espectroscopía fotoelectrónica UV (UPS) |
Espectrometría de masas con microsonda láser (LAMMA) | — |
| \ (\ fila derecha\) energía en\(\downarrow\) “>electrón |
espectroscopía de rayos X dispersiva de energía (EDS) microsonda electrónica (EM) |
Espectroscopia electrónica de barrena (AES) microscopía electrónica de barrido (SEM) difracción de electrones de baja energía (LEED) |
— | — |
| \ (\ fila derecha\) energía en\(\downarrow\) “>ion | — | — |
Dispersión de espalda de Rutherford (RBS) Espectrometría de masas de iones secundarios (SIMS) |
|
| \ (\ fila derecha\) energía en\(\downarrow\) “>campo | — | microscopía de túnel de barrido (STM) | — | Microscopía de fuerza atómica (AFM) |
Hay otras formas de sondear una superficie poniendo energía en ella, incluyendo la aplicación de energía térmica y el uso de especies neutras. Ver el texto Métodos de Análisis de Superficie, Czanderna, A. Editor, Elsevier: Amsterdam (1975) y el artículo “Química analítica de superficies” de D. M. Hercules y S. H. Hercules, J. Chem. Educ. 1984, 61, 402—409 para revisiones detalladas. Aunque tampoco es una publicación reciente, ambas proporcionan una excelente introducción al análisis de superficies.


