25.1: Señales y Corrientes de Excitación Potencial en Voltamperometría
- Page ID
- 79022
En voltamperometría aplicamos un potencial dependiente del tiempo a una celda electroquímica y medimos la corriente resultante en función de ese potencial.
Señales de excitación potenciales
Como se muestra en la Figura\(\PageIndex{1}\), el potencial puede consistir en (a) una exploración lineal o (b) una serie de pulsos. Para el escaneo lineal en (a), la dirección del escaneo puede invertirse y repetirse para ciclos adicionales. La serie de pulsos en (b) muestra solo una de varias señales de excitación de potencial pulsado diferentes; consideraremos otros trenes de pulsos en la sección de polarografía.
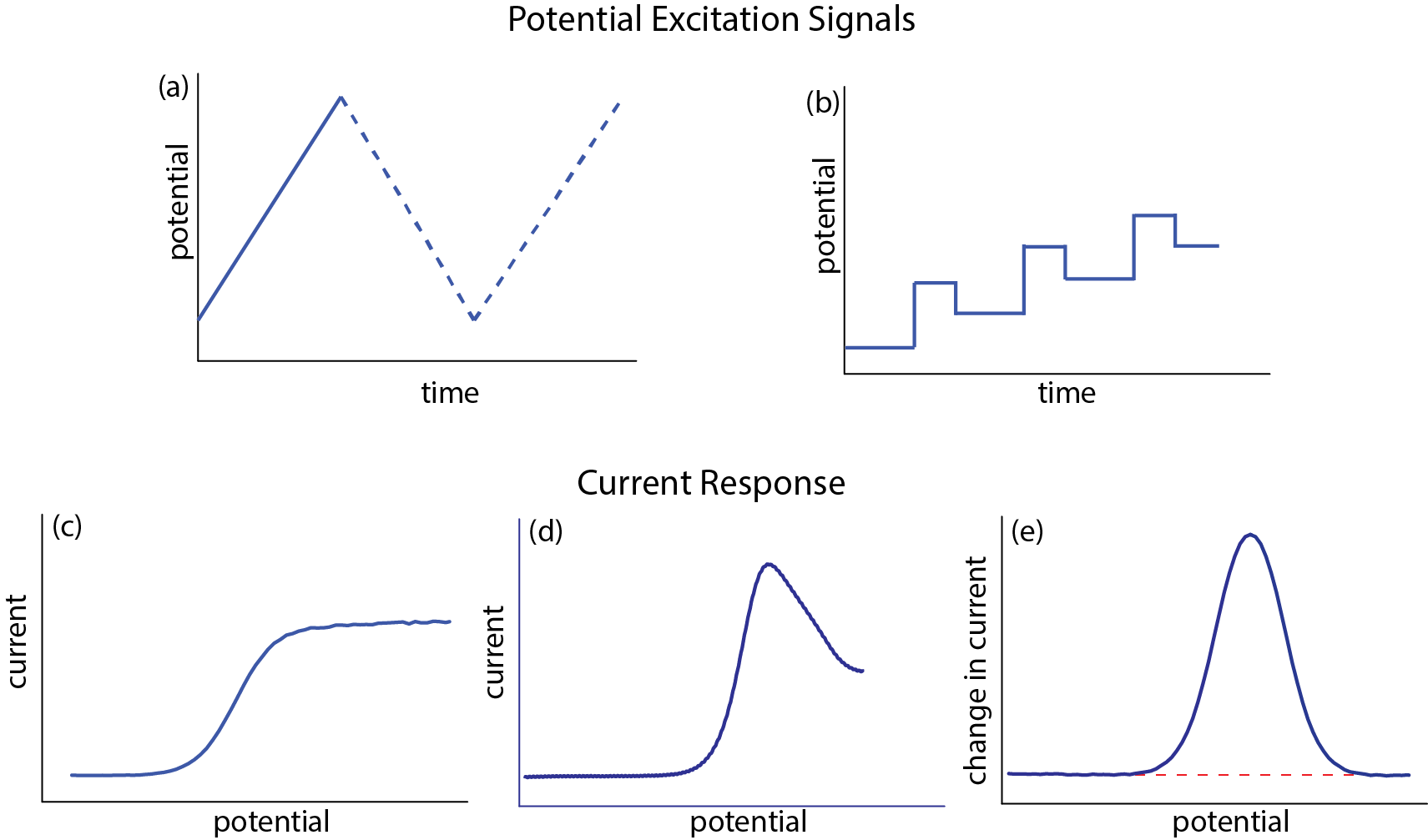
Actual
Las respuestas actuales en la Figura\(\PageIndex{1}\) muestran los tres tipos comunes de señales. En (c) y (d) la corriente es monitoreada directamente a medida que se cambia el potencial. En (e) se registra un cambio en la corriente utilizando la corriente inmediatamente antes y después de la aplicación de un pulso potencial. La corriente en sí tiene tres componentes: corriente farádica de la oxidación o reducción del analito, una corriente de carga y corrientes residuales.
Corriente Faradaica
La corriente farádica es el resultado de la oxidación o reducción del analito en el electrodo de trabajo. La facilidad con la que los electrones se mueven entre el electrodo y las especies que reaccionan en el electrodo afecta a la corriente faradiaca. Cuando la cinética de transferencia de electrones es rápida, la reacción redox está en equilibrio. En estas condiciones la reacción redox es electroquímicamente reversible y se aplica la ecuación de Nernst. Si la cinética de transferencia de electrones es suficientemente lenta, la concentración de reactivos y productos en la superficie del electrodo y, por lo tanto, la magnitud de la corriente faradaica, no son lo que predice la ecuación de Nernst. En este caso el sistema es electroquímicamente irreversible.
Corrientes de Carga
Además de la corriente faradaica de una reacción redox, la corriente en una celda electroquímica incluye otras fuentes no faradáicas. Supongamos que la carga en un electrodo es cero y de repente cambiamos su potencial para que la superficie del electrodo adquiera una carga positiva. Los cationes cerca de la superficie del electrodo responderán a esta carga positiva migrando lejos del electrodo; los aniones, por otro lado, migrarán hacia el electrodo. Esta migración de iones ocurre hasta que la carga superficial positiva del electrodo y la carga negativa de la solución cerca del electrodo son iguales. Debido a que el movimiento de iones y el movimiento de electrones son indistinguibles, el resultado es una pequeña corriente no faradaica de corta duración que llamamos corriente de carga. Cada vez que cambiamos el potencial del electrodo, fluye una corriente de carga transitoria.
La migración de iones en respuesta a la carga superficial del electrodo conduce a la formación de una interfaz estructurada electrodo-solución que llamamos la doble capa eléctrica, o EDL. Cuando cambiamos el potencial de un electrodo, la corriente de carga es el resultado de una reestructuración de la EDL. La estructura exacta de la doble capa eléctrica no es importante en el contexto de este texto, pero puede consultar los recursos adicionales de este capítulo para obtener información adicional. Consulte el Capítulo 22.1 para obtener detalles adicionales.
Corriente Residual
Incluso en ausencia de analito, una pequeña corriente medible fluye a través de una celda electroquímica. Además de la corriente de carga comentada anteriormente, la corriente residual incluye una corriente faradaica procedente de la oxidación o reducción de trazas de impurezas en la muestra. Los métodos para discriminar entre la corriente faradaica del analito y la corriente residual se discuten más adelante en este capítulo.


