3.3: Principios básicos de Cromatografía de Fluidos Supercríticos y Extracción de Fluidos Supercrtical
- Page ID
- 71221
El descubrimiento de fluidos supercríticos condujo a nuevas aplicaciones analíticas en los campos de la cromatografía y extracción conocidas como cromatografía de fluidos supercríticos (SFC) y extracción de fluidos supercríticos (SFE). La cromatografía de fluidos supercríticos se acepta como método de cromatografía en columna junto con cromatografía de gases (GC) y cromatografía líquida de alta resolución (HPLC). Debido a las propiedades de los fluidos supercríticos, SFC combina cada una de las ventajas tanto de GC como de HPLC en un solo método. Además, la extracción de fluidos supercríticos es una técnica analítica avanzada.
Definición y Formación de Fluidos Supercríticos
Un fluido supercrítico es la fase de un material a temperatura crítica y presión crítica del material. La temperatura crítica es la temperatura a la que un gas no puede convertirse en líquido mientras no haya presión extra; y, la presión crítica es la cantidad mínima de presión para licuar un gas a su temperatura crítica. Los fluidos supercríticos combinan propiedades útiles de las fases gaseosa y líquida, ya que pueden comportarse tanto como gas como líquido en términos de diferentes aspectos. Un fluido supercrítico proporciona una característica similar al gas cuando llena un recipiente y toma la forma del recipiente. El movimiento de las moléculas es bastante similar al de las moléculas de gas. Por otro lado, un fluido supercrítico se comporta como un líquido porque su propiedad de densidad está cerca del líquido y, así, un fluido supercrítico muestra una similitud con el efecto de disolución de un líquido.
Las propiedades características de un fluido supercrítico son densidad, difusividad y viscosidad. Los valores supercríticos para estas características tienen lugar entre líquidos y gases. Tabla\(\PageIndex{1}\) muestra valores numéricos de propiedades para gas, fluido supercrítico y líquido.
| Gas | Fluido supercrítico | Líquido | |
|---|---|---|---|
| Densidad (g/cm 3) | 0.6 x 10 -3 -2.0 x 10 -3 | 0.2-0.5 | 0.6-2.0 |
| Difusividad (cm 2 /s) | 0.1-0.4 | 10 -3 -10 -4 | 0.2 x 10 -5 -2.0 x 10 -5 |
| Viscosidad (cm/s) | 1 x 10 -4 -3 x 10 -4 | 1 x 10 -4 -3 x 10 -4 | 0.2 x 10 -2 -3.0 x 10 -2 |
La formación de un fluido supercrítico es el resultado de un equilibrio dinámico. Cuando un material se calienta a su temperatura crítica específica en un sistema cerrado, a presión constante, se genera un equilibrio dinámico. Este equilibrio incluye el mismo número de moléculas que salen de la fase líquida a la fase gaseosa al ganar energía y entrar a la fase líquida de la fase gaseosa al perder energía. En este punto particular, la curva de fase entre las fases líquida y gaseosa desaparece y aparece material supercrítico.
Para entender mejor la definición de SF, se puede utilizar un diagrama de fases simple. La figura\(\PageIndex{1}\) muestra un diagrama de fases ideal. Para un material puro, un diagrama de fases muestra los campos donde el material está en forma de sólido, líquido y gas en términos de diferentes valores de temperatura y presión. Las curvas, donde dos fases (sólido-gas, sólido-líquido y líquido-gas) existen juntas, definen los límites de las regiones de fase. Estas curvas, por ejemplo, incluyen la sublimación para el límite sólido-gas, la fusión para el límite sólido-líquido y la vaporización para el límite líquido-gas. Aparte de estas curvas de existencia binaria, hay un punto donde las tres fases están presentes juntas en equilibrio; el punto triple (TP).
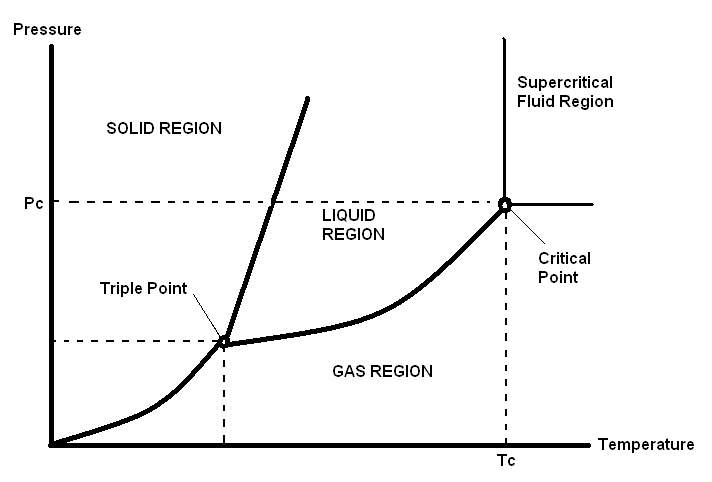
Hay otro punto característico en el diagrama de fases, el punto crítico (CP). Este punto se obtiene a temperatura crítica (T c) y presión crítica (P c). Después del CP, no importa cuánta presión o temperatura se incremente, el material no puede transformarse de gas a líquido o de líquido a fase gaseosa. Esta forma es la forma de fluido supercrítico. El aumento de la temperatura no puede dar como resultado que se convierta en gas, y el aumento de la presión no puede dar como resultado que se vuelva líquido En el diagrama de fases, el campo por encima de los valores T c y P c se define como la región supercrítica.
En teoría, la región supercrítica se puede alcanzar de dos maneras:
- Aumentar la presión por encima del valor P c del material manteniendo la temperatura estable y luego aumentando la temperatura por encima del valor T c a un valor de presión estable.
- Aumentando la temperatura primero por encima del valor T c y luego aumentando la presión por encima del valor P c.
El punto crítico es característico para cada material, resultante de los valores característicos de T c y P c para cada sustancia.
Propiedades Físicas de Fluidos Supercríticos
Como se mencionó anteriormente, SF comparte algunas características comunes tanto con gases como con líquidos. Esto nos permite aprovechar una correcta combinación de las propiedades.
Densidad
La densidad característica de un fluido supercrítico se encuentra entre la de un gas y un líquido, pero más cercana a la de un líquido. En la región supercrítica, la densidad de un fluido supercrítico aumenta con el aumento de la presión (a temperatura constante). Cuando la presión es constante, la densidad del material disminuye con el aumento de la temperatura. El efecto de disolución de un fluido supercrítico depende de su valor de densidad. Los fluidos supercríticos también son mejores portadores que los gases gracias a su mayor densidad. Por lo tanto, la densidad es un parámetro esencial para las técnicas analíticas que utilizan fluidos supercríticos como solventes.
Difusividad
La difusividad de un fluido supercrítico puede ser 100 x la de un líquido y de 1/1,000 a 1/10,000 x menos que un gas. Debido a que los fluidos supercríticos tienen más difusividad que un líquido, es lógico pensar que un soluto puede mostrar mejor difusividad en un fluido supercrítico que en un líquido. La difusividad es paralela a la temperatura y contrariamente a la presión. El aumento de la presión afecta a las moléculas de fluido supercrítico para acercarse entre sí y disminuye la difusividad en el material. La mayor difusividad da a los fluidos supercríticos la oportunidad de ser portadores más rápidos para aplicaciones analíticas. Por lo tanto, los fluidos supercríticos juegan un papel importante en los métodos de cromatografía y extracción.
Viscosidad
La viscosidad para un fluido supercrítico es casi la misma que un gas, siendo aproximadamente 1/10 de la de un líquido. Por lo tanto, los fluidos supercríticos son menos resistentes que los líquidos hacia los componentes que fluyen. La viscosidad de los fluidos supercríticos también se distingue de la de los líquidos en que la temperatura tiene un pequeño efecto sobre la viscosidad del líquido, donde puede influir dramáticamente en la viscosidad del fluido supercrítico.
Estas propiedades de viscosidad, difusividad y densidad están relacionadas entre sí. El cambio de temperatura y presión puede afectar a todos ellos en diferentes combinaciones. Por ejemplo, aumentar la presión provoca un aumento de la viscosidad y el aumento de la viscosidad da como resultado una disminución de la difusividad
Cromatografía Súper Fluida (SFC)
Al igual que los fluidos supercríticos combinan los beneficios de líquidos y gases, SFC reúne las ventajas y los aspectos fuertes de HPLC y GC. La SFC puede ser más ventajosa que la HPLC y la GC cuando se analizan compuestos que se descomponen a altas temperaturas con GC y no tienen grupos funcionales para ser detectados por sistemas de detección por HPLC.
Hay tres cualidades principales para las cromatografías en columna:
- Selectividad.
- Eficacia.
- Sensibilidad.
Generalmente, la HPLC tiene mejor selectividad que la SFC debido a fases móviles cambiables (especialmente durante una ejecución experimental particular) y una amplia gama de fases estacionarias. Aunque SFC no tiene la selectividad de HPLC, tiene buena calidad en términos de sensibilidad y eficiencia. La SFC permite el cambio de algunas propiedades durante el proceso cromatográfico. Esta capacidad de afinación permite la optimización del análisis. Además, SFC tiene una gama más amplia de detectores que la HPLC. SFC supera a GC para el análisis de sustancias fácilmente descomponibles; estos materiales pueden ser utilizados con SFC debido a su capacidad para trabajar con temperaturas más bajas que la GC.
Instrumentación para SFC
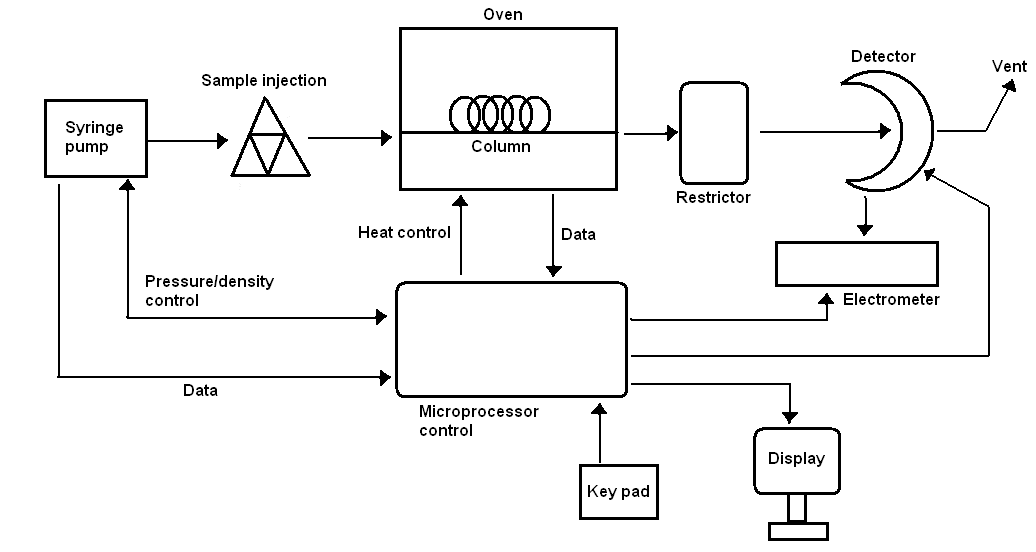
Como se puede observar en la Figura\(\PageIndex{2}\) SFC tiene una configuración similar a un instrumento de HPLC. Utilizan fases estacionarias similares con tipos de columnas similares. Sin embargo, existen algunas diferencias. La temperatura es crítica para los fluidos supercríticos, por lo que debe haber una herramienta de control de calor en el sistema similar a la de GC. Además, debe existir un mecanismo de control de presión, un restrictor, ya que la presión es otro parámetro esencial para que los materiales de fluidos supercríticos se mantengan en el nivel requerido. Se coloca un mecanismo de microprocesador en el instrumento para SFC. Esta unidad recopila datos de presión, temperatura del horno y rendimiento del detector para controlar las piezas relacionadas del instrumento.
Fase Estacionaria
Las columnas SFC son similares a las columnas de HPLC en términos de materiales de recubrimiento. Las columnas tubulares abiertas y las columnas empaquetadas son los dos tipos más comunes utilizados en SFC. Se prefieren los tubulares abiertos y tienen similitudes con las columnas de sílice fundida por HPLC. Este tipo de columna contiene un recubrimiento interno de un material de siloxano reticulado como fase estacionaria. El espesor del recubrimiento puede ser de 0.05-1.0 μm. La longitud de la columna puede variar de 10 a 20 m.
Fases Móviles
Existe una amplia variedad de materiales utilizados como fase móvil en SFC. La fase móvil se puede seleccionar entre los grupos disolventes de disolventes inorgánicos, hidrocarburos, alcoholes, éteres, haluros; o puede ser acetona, acetonitrilo, piridina, etc. El fluido supercrítico más común que se usa en SFC es el dióxido de carbono porque su temperatura y presión críticas son fáciles de alcanzar. Adicionalmente, el dióxido de carbono es de bajo costo, fácil de obtener, inerte frente a los rayos UV, no venenoso y un buen disolvente para moléculas no polares. Además de dióxido de carbono, etano, n-butano, N 2 O, diclorodifluorometano, éter dietílico, amoníaco, tetrahidrofurano se pueden usar. En la tabla se\(\PageIndex{2}\) muestran los solventes seleccionados y sus valores de T c y P c.
| Solvente | Temperatura crítica (°C) | Presión crítica (bar) |
|---|---|---|
| Dióxido de carbono (CO 2) | 31.1 | 72 |
| Óxido nitroso (N 2 O) | 36.5 | 70.6 |
| Amoníaco (NH 3) | 132.5 | 109.8 |
| Etano (C 2 H 6) | 32.3 | 47.6 |
| N-butano (C 4 H 10) | 152 | 70.6 |
| Éter dietílico (Et 2 O) | 193.6 | 63.8 |
| Tetrahidrofurano (THF, C 4 H 8 O) | 267 | 50.5 |
| Diclorodifluorometano (CCl 2 F 2) | 111.7 | 109.8 |
Detectores
Una de las mayores ventajas de SFC sobre HPLC es la gama de detectores. El detector de ionización de llama (FID), que normalmente está presente en la configuración de GC, también se puede aplicar a SFC. Dicho detector puede contribuir a la calidad de los análisis de SFC ya que el FID es un detector altamente sensible. El SFC también se puede acoplar con un espectrómetro de masas, un espectrómetro UV-Visible o un espectrómetro IR más fácilmente de lo que se puede hacer con una HPLC. Algunos otros detectores que se utilizan con HPLC se pueden unir a SFC como espectrómetro de emisión de fluorescencia o detectores termiónicos.
Ventajas de trabajar con SFC
Las propiedades físicas de los fluidos supercríticos entre líquidos y gases permiten que la técnica SFC se combine con los mejores aspectos de HPLC y GC, ya que la menor viscosidad de los fluidos supercríticos hace que SFC sea un método más rápido que la HPLC. Una viscosidad más baja conduce a una alta velocidad de flujo para la fase móvil.
Gracias a la presión crítica de los fluidos supercríticos, algunos materiales frágiles que son sensibles a las altas temperaturas pueden analizarse a través de SFC. Estos materiales pueden ser compuestos que se descomponen a altas temperaturas o materiales que tienen baja presión/volatilidad de vapor tales como polímeros y moléculas biológicas grandes. Las condiciones de alta presión brindan la oportunidad de trabajar con una temperatura más baja de la que normalmente se necesita. Por lo tanto, los componentes sensibles a la temperatura se pueden analizar a través de SFC. Además, la difusión de los componentes que fluyen a través de un fluido supercrítico es mayor que la observada en HPLC debido a la mayor difusividad de los fluidos supercríticos sobre las fases móviles de los líquidos tradicionales. Esto da como resultado una mejor distribución en la fase móvil y una mejor separación.
Aplicaciones de SFC
Las aplicaciones de SFC van desde la industria alimentaria hasta las industrias ambientales y farmacéuticas. De esta manera, pesticidas, herbicidas, polímeros, explosivos y combustibles fósiles son todas clases de compuestos que pueden analizarse. SFC se puede utilizar para analizar una amplia variedad de compuestos farmacológicos como antibióticos, prostaglandinas, esteroides, taxol, vitaminas, barbitúricos, agentes antiinflamatorios no esteroideos, etc. Se pueden realizar separaciones quirales para muchos compuestos farmacéuticos. El SFC se usa predominantemente para compuestos no polares debido a la baja eficiencia del dióxido de carbono, que es la fase móvil de fluido supercrítico más común, para disolver solutos polares. El SFC se utiliza en la industria petrolera para la determinación del contenido total de aromáticos, así como otras separaciones de hidrocarburos.
Extracción de Fluidos Supercríticos (SFE)
Las propiedades físicas únicas de los fluidos supercríticos, que tienen valores de densidad, difusividad y viscosidad entre líquidos y gases, permiten la extracción de fluidos supercríticos para los procesos de extracción que no pueden ser realizados por líquidos debido a su alta densidad y baja difusividad y por gases debido a su densidad inadecuada para extraer y llevar a cabo los componentes.
Las mezclas complicadas que contienen muchos componentes deben someterse a un proceso de extracción antes de que se separen por cromatografía. Un procedimiento de extracción ideal debe ser rápido, sencillo y económico. Además, no se debe experimentar pérdida o descomposición de la muestra al final de la extracción. Después de la extracción, debe haber una colección cuantitativa de cada componente. Idealmente, la cantidad de materiales no deseados provenientes de la extracción debe mantenerse al mínimo y ser fácilmente desechables; los desechos no deben ser dañinos para el medio ambiente. Desafortunadamente, los métodos de extracción tradicionales a menudo no cumplen con estos requisitos. Al respecto, la SFE tiene varias ventajas en comparación con las técnicas tradicionales.
La velocidad de extracción depende de la viscosidad y difusividad de la fase móvil. Con una baja viscosidad y alta difusividad, el componente que se va a extraer puede pasar fácilmente a través de la fase móvil. La mayor difusividad y menor viscosidad de los fluidos supercríticos, en comparación con los líquidos de extracción regulares, ayudan a que los componentes se extraigan más rápido que otras técnicas. Así, un proceso de extracción puede tomar solo 10-60 minutos con SFE, mientras que tomaría horas o incluso días con métodos clásicos.
La eficiencia de disolución de un fluido supercrítico puede ser alterada por la temperatura y la presión. Por el contrario, los líquidos no se ven afectados tanto por los cambios de temperatura y presión. Por lo tanto, la SFE tiene el potencial de ser optimizada para proporcionar una mejor capacidad de disolución.
En los métodos clásicos, se requiere calentamiento para eliminar el líquido de extracción. Sin embargo, este paso hace que los materiales sensibles a la temperatura se descompongan. Para SFE, cuando se elimina la presión crítica, un fluido supercrítico se transforma en fase gaseosa. Debido a que los solventes fluidos supercríticos son químicamente inertes, inofensivos y económicos; pueden ser liberados a la atmósfera sin dejar ningún desperdicio. A través de esto, los componentes extraídos se pueden obtener con mucha más facilidad y se minimiza la pérdida de muestra.
Instrumentación de SFE
El aparato necesario para una configuración de SFE es simple. La figura\(\PageIndex{3}\) representa los elementos básicos de un instrumento SFE, el cual está compuesto por un depósito de fluido supercrítico, una unidad de inyección de sintonización de presión, dos bombas (para tomar los componentes en la fase móvil y enviarlos fuera de la celda de extracción) y una cámara de recolección.
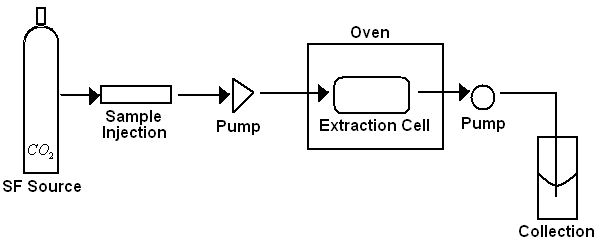
Hay dos modos principales para ejecutar el instrumento:
- Extracción estática.
- Extracción dinámica.
En la extracción dinámica, la segunda bomba que envía los materiales a la cámara de recolección siempre está abierta durante el proceso de extracción. Así, la fase móvil llega a la célula de extracción y extrae los componentes para sacarlos de manera consistente.
En el experimento de extracción estática, hay dos etapas distintas en el proceso:
- La fase móvil llena la celda de extracción e interactúa con la muestra.
- Se abre la segunda bomba y se extraen de inmediato las sustancias extraídas.
Para elegir la fase móvil para SFE, los parámetros tomados en consideración incluyen la polaridad y solubilidad de las muestras en la fase móvil. El dióxido de carbono es la fase móvil más común para SFE. Tiene capacidad para disolver materiales no polares como alcanos. Para compuestos semipolares (como hidrocarburos aromáticos policíclicos, aldehídos, ésteres, alcoholes, etc.) se puede utilizar dióxido de carbono como fase móvil de un solo componente. Sin embargo, para los compuestos que tienen características polares, el dióxido de carbono supercrítico debe modificarse mediante la adición de disolventes polares como el metanol (CH 3 OH). Estos solventes adicionales se pueden introducir en el sistema a través de una bomba de inyección separada.
Modos de extracción
Hay dos modos en términos de recolección y detección de los componentes:
- Extracción fuera de línea.
- Extracción en línea.
La extracción fuera de línea se realiza eliminando la fase móvil con los componentes extraídos y dirigiéndolos hacia la cámara de recolección. En este punto, la fase de fluido supercrítico se evapora y se libera a la atmósfera y los componentes se capturan en una solución o una superficie de adsorción conveniente. Después los fragmentos extraídos son procesados y preparados para un método de separación. Este paso de manipulación adicional entre el extractor y el instrumento de cromatografía puede causar errores. El método en línea es más sensible porque transfiere directamente todos los materiales extraídos a una unidad de separación, en su mayoría un instrumento de cromatografía, sin sacarlos de la fase móvil. En este tipo de extracción/detección, no hay preparación adicional de muestras después de la extracción para el proceso de separación. Esto minimiza los errores provenientes de los pasos de manipulación. Adicionalmente, no se produce pérdida de muestra y aumenta la sensibilidad.
Aplicaciones de SFE
SFE se puede aplicar a una amplia gama de materiales tales como polímeros, aceites y lípidos, carbonhidratos, pesticidas, contaminantes orgánicos, toxinas volátiles, hidrocarburos poliaromáticos, biomoléculas, alimentos, sabores, metabolitos farmacéuticos, explosivos y organometálicos, etc. la industria farmacéutica y bioquímica, la industria de polímeros, la síntesis y extracción industrial, la química de productos naturales y la industria alimentaria.
Ejemplos de materiales analizados en aplicaciones ambientales: aceites y grasas, pesticidas, alcanos, contaminantes orgánicos, toxinas volátiles, herbicidas, nicotina, fenantreno, ácidos grasos, surfactantes aromáticos en muestras de arcilla a desechos de petróleo, desde el suelo hasta los sedimentos de río. En los análisis de alimentos: cafeína, peróxidos, aceites, ácidos, colesterol, etc. se extraen de muestras como café, aceite de oliva, limón, cereales, trigo, papa y pienso para perros. A través de aplicaciones industriales, los materiales extraídos varían desde aditivos hasta diferentes oligómeros, y desde fracciones de petróleo hasta estabilizadores. Las muestras analizadas son plásticos, PVC, papel, madera etc. metabolitos de fármacos, enzimas, esteroides se extraen de plasma, orina, suero o tejidos animales en aplicaciones bioquímicas.
Resumen
La cromatografía de fluidos supercríticos y la extracción de fluidos supercríticos son técnicas que aprovechan las propiedades únicas de los fluidos supercríticos. Como tales, aportan ventajas sobre otros métodos relacionados tanto en cromatografía como en extracción. En ocasiones se utilizan como técnicas analíticas alternativas, mientras que otras veces se utilizan como socios complementarios para sistemas binarios. Tanto SFC como SFE demuestran su versatilidad a través de la amplia gama de aplicaciones en muchos dominios distintos de una manera ventajosa.


