7.6: XAFS
- Page ID
- 70973
La espectroscopía de estructura fina de absorción de rayos X (XAFS) incluye espectroscopias de estructura fina de absorción de rayos X (XANES) y de estructura fina de absorción de rayos X extendida (EXAFS). La diferencia entre ambas técnicas es el área a analizar, como se muestra en la Figura\(\PageIndex{1}\) y la información que proporciona cada técnica. El espectro XAFS completo se recoge en un rango de energía de alrededor de 200 eV antes del borde de absorción de interés y hasta 1000 eV después del mismo (Figura\(\PageIndex{2}\)). El borde de absorción se define como la energía de rayos X cuando el coeficiente de absorción tiene un aumento pronunciado. Esta energía es igual a la energía requerida para excitar un electrón a un orbital desocupado.

La estructura de absorción de rayos X cerca del borde (XANES) se utiliza para determinar el estado de valencia y la geometría de coordinación, mientras que la estructura fina de absorción extendida de rayos X (EXAFS) se utiliza para determinar la estructura molecular local de un elemento particular en una muestra.
Espectros de absorción de rayos X cerca de la estructura de borde (X
XANES es la parte del espectro de absorción más cerca de un borde de absorción. Cubre desde aproximadamente -50 eV hasta +200 eV con respecto a la energía del borde (Figura\(\PageIndex{2}\)).
Debido a que la forma del borde de absorción está relacionada con la densidad de estados disponibles para la excitación del fotoelectrón, la geometría de unión y el estado de oxidación del átomo afectan a la parte XANES del espectro de absorción.
Antes del borde de absorción, hay un área lineal y lisa. Entonces, el borde aparece como un escalón, que puede tener otras formas extra como picos aislados, hombros o una línea blanca, que es un pico fuerte sobre el borde. Esas formas dan alguna información sobre el átomo. Por ejemplo, la presencia de una línea blanca indica que después de la liberación del electrón, los estados atómicos del elemento quedan confinados por el potencial que siente. Este pico agudo se suavizaría si el átomo pudiera entrar a cualquier tipo de resonancia. Se da información importante debido a la posición del borde de absorción. Los átomos con mayor estado de oxidación tienen menos electrones que los protones, por lo que, los estados energéticos de los electrones restantes se reducen ligeramente, lo que provoca un desplazamiento de la energía del borde de absorción hasta varios eV a una mayor energía de rayos X.
Espectros de estructura fina de absorción de rayos X extendidos (EXAFS)
La parte EXAFS del espectro es la parte oscilatoria del coeficiente de absorción por encima de alrededor de 1000 eV del borde de absorción. Esta región se utiliza para determinar los ambientes de unión molecular de los elementos. EXAFS da información sobre los tipos y números de átomos en coordinación de un átomo específico y sus distancias interatómicas. Los átomos a la misma distancia radial de un átomo determinado forman una concha. El número de átomos en la cubierta es el número de coordinación (por ejemplo, Figura\(\PageIndex{2}\)).
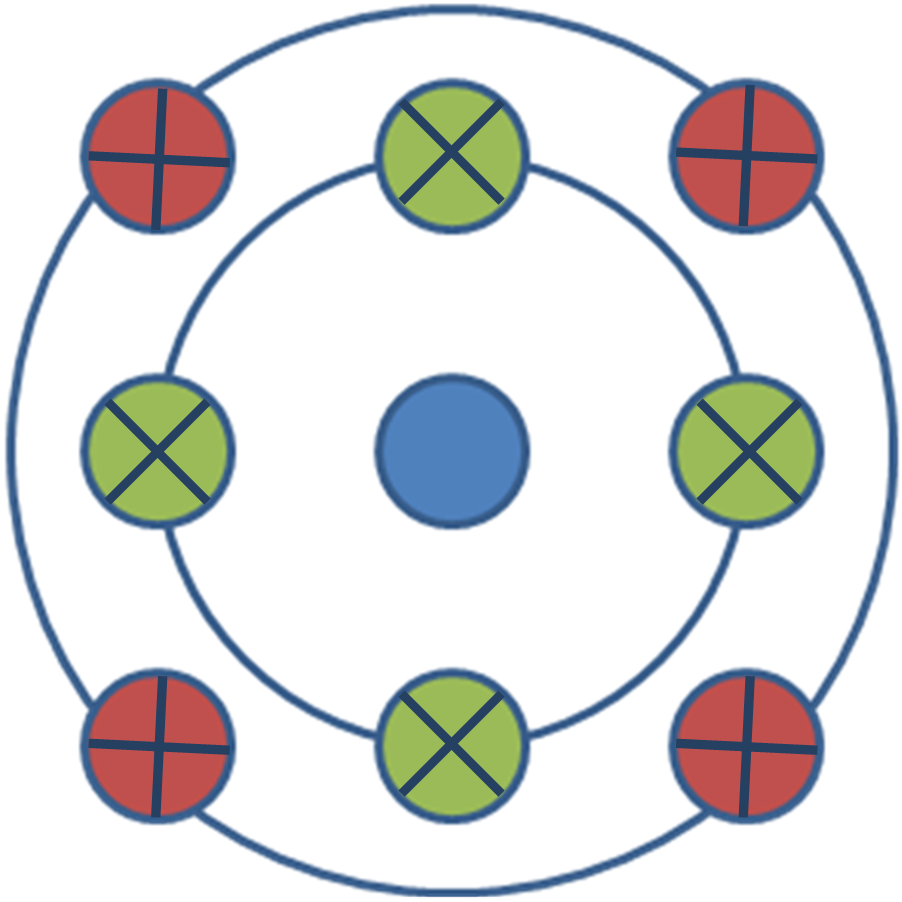
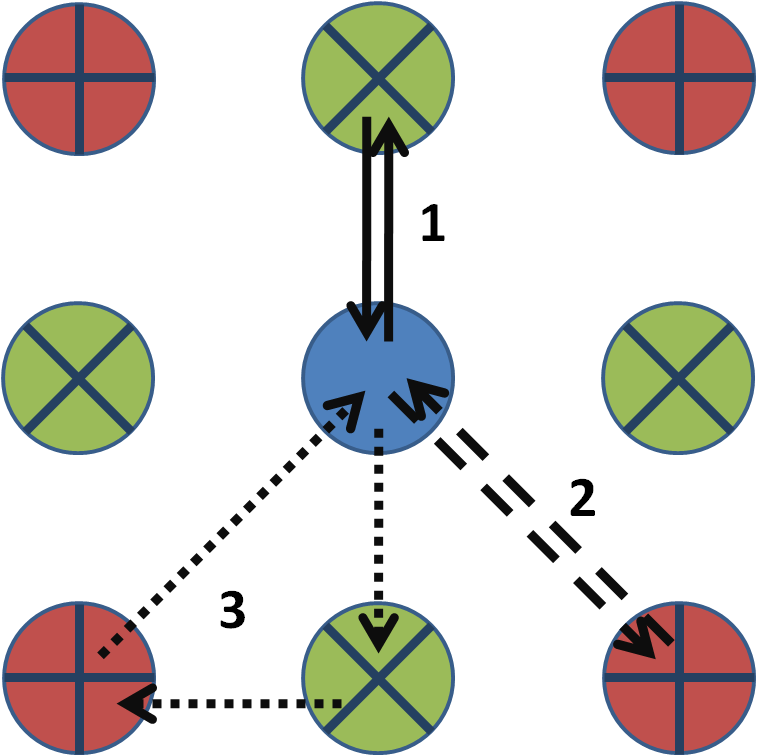
Una señal EXAFS viene dada por la dispersión de fotoelectrones generada para el átomo central. La fase de la señal está determinada por la distancia y la trayectoria que recorren los fotoelectrones. Un esquema simple de los diferentes caminos se muestra en la Figura\(\PageIndex{3}\). En el caso de dos conchas alrededor del átomo centrado, hay una degeneración de cuatro para el camino entre el átomo principal y la primera concha, una degeneración de cuatro para el camino entre el átomo principal y la segunda capa, y una degeneración de ocho para el camino entre el átomo principal a la primera capa, a la segunda y al átomo central.
El análisis de los espectros EXAFS se realiza mediante transformación de Fourier para ajustar los datos a la ecuación EXAFS. La ecuación EXAFS es una suma de la contribución de todas las rutas de dispersión de los fotoelectrones\ ref {1}, donde cada ruta viene dada por\ ref {2}.
\[ \chi (k)\ =\ \sum_{i} \chi _{i}(k) \label{1} \]
\[ \chi _{i} (k) \equiv \frac{(N_{i}S_{0}^{2})F_{eff_{i}}(k)}{kR^{2}_{i}} \sin[2kR_{i}\ +\ \phi _{i}(k)] e^{-2\sigma ^{2}_{i} k^{2}} e^{\frac{-2R_{i}}{\lambda (k)}} \label{2} \]
Los términos F eff i (k), φ i (k) y λ i (k) son la amplitud de dispersión efectiva del fotoelectrón, el desplazamiento de fase del fotoelectrón y la trayectoria libre media del fotoelectrón, respectivamente. El término R i es la longitud de medio camino del fotoelectrón (la distancia entre el átomo centrado y un átomo de coordinación para un evento de dispersión simple). Y el k 2 viene dado por\ ref {3}. Las variables restantes se determinan frecuentemente modelando el espectro EXAFS.
\[ k^{2}\ = \frac{2m_{e}(E-E_{0}\ +\ \Delta E_{0})}{\hbar} \label{3} \]
Análisis XAFS para adsorción de arsénico sobre óxidos de hierro
La absorción de especies de arsénico sobre óxido de hierro ofrece n ejemplo de la información que puede obtener EXAFS. Debido al enorme impacto que la presencia de arsénico en el agua puede producir en las sociedades hay mucha investigación en la adsorción de arsénico en varios tipos de materiales, en particular nano materiales. Algunos de los materiales más prometedores para este tipo de aplicaciones son los óxidos de hierro. La elucidación del mecanismo de coordinación del arsénico sobre las superficies de esos materiales ha sido estudiada últimamente mediante espectroscopía de absorción de rayos X.
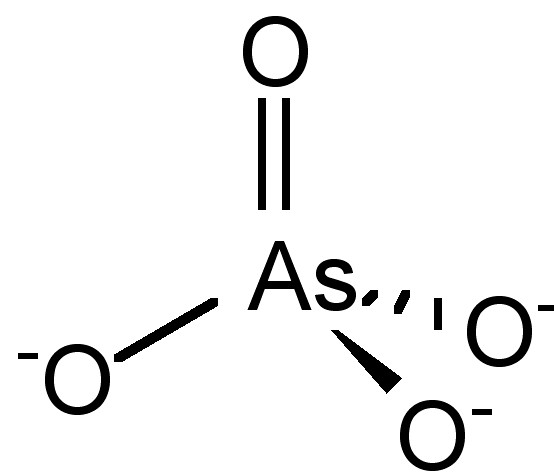
Hay varias formas de adsorber arseniato (AsO 4 3−, Figura\(\PageIndex{4}\)) sobre las superficies. La figura\(\PageIndex{5}\) muestra las tres formas en que Sherman propone que el arseniato puede adsorberse sobre la goetita (α-FeOOH): compartición de esquinas bidentado (2C), compartición de bordes bidentado (2E) y formas monodentadas de esquina compartidas (1V). La figura\(\PageIndex{6}\) muestra que el reparto de esquinas bidentado (2C) es la configuración que corresponde con los parámetros calculados no sólo para la goetita, sino para varios óxidos de hierro.

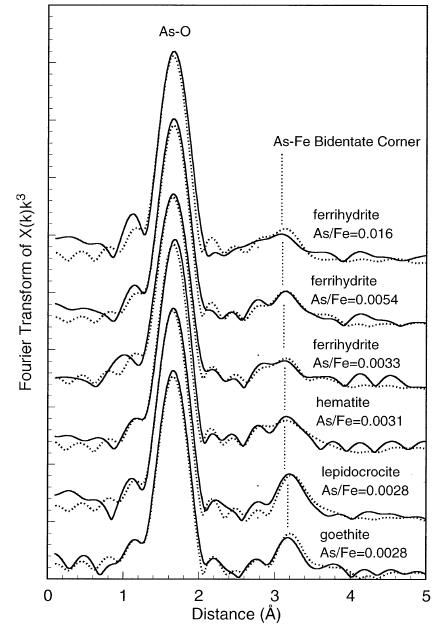
Diversos estudios han confirmado que el reparto de esquinas bidentado (2C) es el que está presente en la adsorción de arseniato pero también uno similar, un complejo tridentado de intercambio de esquinas (3C), para la adsorción de arsenito sobre la mayoría de los óxidos de hierro como muestra la Figura\(\PageIndex{7}\). En el cuadro se\(\PageIndex{1}\) muestran los números de coordinación y distancias reportados en la literatura para el As (III) y As (V) sobre la goetita.

| Como | CN As-O | R As-O (Å) | CN As Fe | R As Fe (Å) |
|---|---|---|---|---|
| III | 3.06±0.03 | 1.79±0.8 | 2.57±0.01 | 3.34±3 |
| 3.19 | 1.77±1 | 1.4 | 3.34±5 | |
| 3 | 1.78 | 2 | 3.55±5 | |
| V | 1.03 | 1.631 | 2 | 3.30 |
| 4.6 | 1.68 | — | 3.55±5 |


