4.8: Estadística de Velocidades Moleculares
- Page ID
- 74481
Los valores esperados para varias cantidades se pueden calcular a partir de la función de densidad de probabilidad Maxwell-Boltzmann. Las integrales definidas requeridas se tabulan en el Apéndice D.
La velocidad más probable,\(v_{mp}\), es la velocidad a la que la ecuación de Maxwell-Boltzmann adquiere su valor máximo. A esta velocidad, tenemos
\[ \begin{align*} 0&=\frac{d}{dv}\left(\frac{df\left(v\right)}{dv}\right)=\frac{d}{dv}\left[4\pi {\left(\frac{m}{2\pi kT}\right)}^{3/2}v^2\exp\left(\frac{-mv^2}{2kT}\right)\right] \\[4pt] &=\left[4\pi {\left(\frac{m}{2\pi kT}\right)}^{3/2}\exp\left(\frac{-mv^2}{2kT}\right)\right]\left[2v-\frac{mv^3}{kT}\right] \end{align*}\]
de la cual
\[v_{mp}=\sqrt{\frac{2kT}{m}}\approx 1.414\sqrt{\frac{kT}{m}}\]
La velocidad promedio,\(\overline{v}\) o\(\left\langle v\right\rangle\), es el valor esperado de la velocidad escalar (\(g\left(v\right)=v\)). ENCONTRAMOS
\[\overline{v}=\left\langle v\right\rangle =\int^{\infty }_0{4\pi {\left(\frac{m}{2\pi kT}\right)}^{3/2}v^3exp\left(\frac{-mv^2}{2kT}\right)}dv=\sqrt{\frac{8kT}{\pi m}}\approx 1.596\sqrt{\frac{kT}{m}}\]
La velocidad media cuadrada,\(\overline{v^2}\) o\(\left\langle v^2\right\rangle\), es el valor esperado de la velocidad al cuadrado (\(g\left(v\right)=v^2\)):
\[\overline{v^2}=\left\langle v^2\right\rangle =\int^{\infty }_0{4\pi {\left(\frac{m}{2\pi kT}\right)}^{3/2}v^4exp\left(\frac{-mv^2}{2kT}\right)}dv=\frac{3kT}{m}\]
y la velocidad media cuadrática raíz,\(v_{rms}\), es
\[v_{rms}=\sqrt{\left\langle v^2\right\rangle }=\sqrt{\frac{3kT}{m}}\approx 1.732\sqrt{\frac{kT}{m}}\]
Ejemplo\(\PageIndex{1}\)
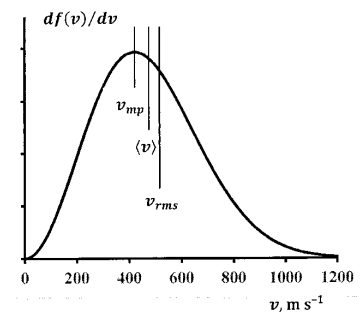
La Figura 6 muestra la distribución de velocidad 300 K para moléculas de nitrógeno a 300 K.
Solución
Finalmente, encontremos la varianza de la velocidad; es decir, el valor esperado de\(\left(v-\left\langle v\right\rangle \right)^2\):
\({\text { variance }(v)=\sigma_{v}^{2}} \)
\[\begin{align*} &=\int_{0}^{\infty}(v-\langle v\rangle)^{2}\left(\frac{d f(v)}{d v}\right) d v \\ &=\int_{0}^{\infty} v^{2}\left(\frac{d f}{d v}\right) d v-2\langle v\rangle \int_{0}^{\infty} v\left(\frac{d f}{d v}\right) d v+\langle v\rangle^{2} \int_{0}^{\infty}\left(\frac{d f}{d v}\right) \\ &=\left\langle v^{2}\right\rangle- 2\langle v\rangle\langle v\rangle+\langle v\rangle^{2} \\ &=\left\langle v^{2}\right\rangle-\langle v\rangle^{2} \end{align*}\]
Para\(N_2\) a\(300\) K, calculamos:
\[v_{mp}\ =422\ \mathrm{m\ }{\mathrm{s}}^{\mathrm{-1}} \nonumber\]
\[\left\langle v\right\rangle =\overline{v}=476\ \mathrm{m\ }{\mathrm{s}}^{\mathrm{-1}} \nonumber\]
\[v_{rms}=517\ \mathrm{m\ }{\mathrm{s}}^{\mathrm{-1}} \nonumber\]
\[ \text{Variance} \left(v\right)=\sigma^2_v=40.23\times {10}^{-3}\ \mathrm{m\ }{\mathrm{s}}^{\mathrm{-1}} \nonumber\]
\[\sigma_v=201\ \mathrm{m\ }{\mathrm{s}}^{\mathrm{-1}} \nonumber\]


