3.11: Capítulo 3 Problemas
- Page ID
- 78059
Un número de problema subrayado o una letra de parte del problema indica que la respuesta numérica aparece en el Apéndice I.
3.1 Supongamos que tiene un resorte metálico que obedece a la ley de Hooke:\(F=c\left(l-l_{0}\right)\), donde\(F\) esta la fuerza ejercida sobre el resorte de longitud\(l, l_{0}\) es la longitud del resorte no estresado, y\(c\) es la constante del resorte. Encuentre una expresión para el trabajo realizado en el resorte cuando lo comprime reversiblemente de longitud\(l_{0}\) a una longitud más corta\(l^{\prime}\).
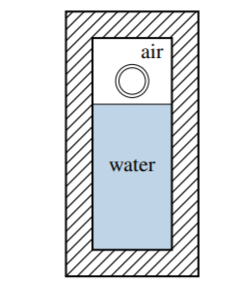
3.2 El aparato mostrado en la Fig. \(3.22\)consiste en cantidades fijas de agua y aire y una esfera de vidrio sólido incompresible (un mármol), todo encerrado en un recipiente rígido que descansa sobre una mesa de laboratorio. Supongamos que el mármol tiene una capa externa adiabática para que su temperatura no pueda cambiar, y que las paredes de la vasija también son adiabáticas.
Inicialmente el mármol se suspende sobre el agua. Cuando se libera, cae a través del aire al agua y llega a descansar en el fondo del recipiente, provocando que el agua y el aire (pero no el mármol) se vuelvan un poco más cálidos. El proceso se completa cuando el sistema vuelve a un estado de equilibrio. El cambio de energía del sistema durante este proceso depende del marco de referencia y de cómo se define el sistema. \(\Delta E_{\text {sys }}\)es el cambio de energía en un marco de laboratorio, y\(\Delta U\) es el cambio de energía en un marco local específico.
Para cada una de las siguientes definiciones del sistema, dé el signo (positivo, negativo o cero) de ambos\(\Delta E_{\text {sys }}\) y\(\Delta U\), y exponga su razonamiento. Tome el marco local de cada sistema para que sea un marco de centro de masa.
(a) El sistema es el mármol.
b) El sistema es la combinación de agua y aire.
(c) El sistema es la combinación de agua, aire y mármol.
3.3 La figura\(3.23\) muestra el estado inicial de un aparato que consiste en un gas ideal en una bombilla, una llave de paso, un tapón poroso y un cilindro que contiene un pistón sin fricción. Las paredes son diatérmicas, y los alrededores están a una temperatura constante de\(300.0 \mathrm{~K}\) y una presión constante de\(1.00 \mathrm{bar}\).
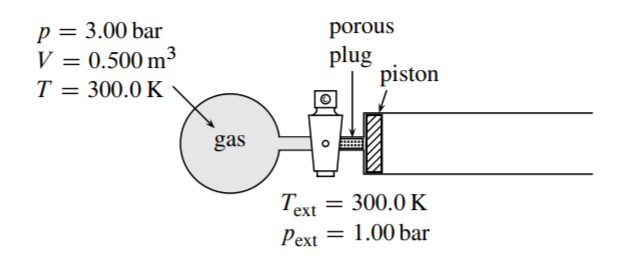
Cuando se abre la llave de paso, el gas se difunde lentamente a través del tapón poroso, y el pistón se mueve lentamente hacia la derecha. El proceso termina cuando se igualan las presiones y el pistón deja de moverse. El sistema es el gas. Supongamos que durante el proceso la temperatura en todo el sistema difiere solo infinitesimalmente de\(300.0 \mathrm{~K}\) y la presión en ambos lados del pistón difiere solo infinitesimalmente de\(1.00\) bar.
a) ¿Cuál de estos términos describe correctamente el proceso: isotérmico, isobárico, isocórico, reversible, irreversible?
(b) Calcular\(q\) y\(w\).
3.4 Considere un dispositivo horizontal de cilindro y pistón similar al que se muestra en la Fig. \(3.5\)en la página 72. El pistón tiene masa\(m\). La pared del cilindro es diatermal y está en contacto térmico con un depósito de calor de temperatura\(T_{\text {ext }}\). El sistema es una cantidad\(n\) de un gas ideal confinado en el cilindro por el pistón.
El estado inicial del sistema es un estado de equilibrio descrito por\(p_{1}\) y\(T=T_{\text {ext }}\). Hay una presión externa constante\(p_{\text {ext }}\), igual a dos veces\(p_{1}\), que suministra una fuerza externa constante sobre el pistón. Cuando se libera el pistón, comienza a moverse hacia la izquierda para comprimir el gas. Hacer los supuestos idealizados de que (1) el pistón se mueve con fricción insignificante; y (2) el gas permanece prácticamente uniforme (porque el pistón es masivo y su movimiento es lento) y tiene una temperatura prácticamente constante\(T=T_{\text {ext }}\) (porque el equilibrio de temperatura es rápido).
a) Describir el proceso resultante.
(b) Describa cómo podría calcular\(w\) y\(q\) durante el período necesario para que la velocidad del pistón vuelva a ser cero.
(c) Calcular\(w\) y\(q\) durante este periodo para\(0.500 \mathrm{~mol}\) gas en\(300 \mathrm{~K}\).
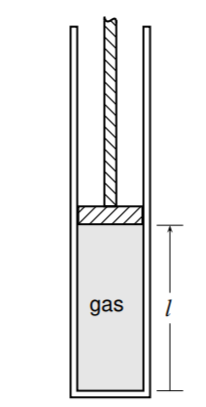
3.5 Este problema está diseñado para probar la afirmación en la página 60 que para procesos termodinámicos típicos en los que cambia la elevación del centro de masa, suele ser una buena aproximación para establecer\(w\) igual a\(w_{\text {lab. }}\). El cilindro mostrado en la Fig. \(3.24\)en la página anterior tiene una orientación vertical, por lo que la elevación del centro de masa del gas confinado por el pistón cambia a medida que el pistón se desliza hacia arriba o hacia abajo. El sistema es el gas. Supongamos que el gas es nitrógeno\(\left(M=28.0 \mathrm{~g} \mathrm{~mol}^{1}\right)\) en\(300 \mathrm{~K}\), e inicialmente la longitud vertical\(l\) de la columna de gas es de un metro. Trate el nitrógeno como un gas ideal, use un marco local de centro de masa y tome el centro de masa para que esté en el punto medio de la columna de gas. Encuentre la diferencia entre los valores de\(w\) y\(w_{\text {lab }}\), expresados como porcentaje de\(w\), cuando el gas se expande de manera reversible e isotérmica al doble de su volumen inicial.
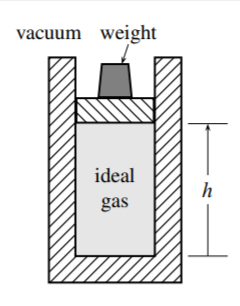
3.6 La figura\(3.25\) muestra un gas ideal confinado por un pistón sin fricción en un cilindro vertical. El sistema es el gas, y el límite es adiabático. La fuerza hacia abajo sobre el pistón se puede variar cambiando el peso en la parte superior del mismo.
(a) Demostrar que cuando el sistema se encuentra en estado de equilibrio, la presión del gas viene dada por\(p=\)\(m g h / V\) donde\(m\) está la masa combinada del pistón y el peso,\(g\) es la aceleración de caída libre, y\(h\) es la elevación del pistón que se muestra en la figura.
(b) Inicialmente la masa combinada del pistón y el peso es\(m_{1}\), el pistón está en altura\(h_{1}\), y el sistema se encuentra en un estado de equilibrio con condiciones\(p_{1}\) y\(V_{1}\). La temperatura inicial es\(T_{1}=p_{1} V_{1} / n R\). Supongamos que de repente se coloca un peso adicional sobre el pistón, de manera que eso\(m\) aumenta de\(m_{1}\) a\(m_{2}\), provocando que el pistón se hunda y que el gas se comprima adiabática y espontáneamente. Los gradientes de presión en el gas, una forma de fricción, eventualmente hacen que el pistón descanse en una posición final\(h_{2}\). Encuentra el volumen final,\(V_{2}\), en función de\(p_{1}, p_{2}, V_{1}\), y\(C_{V} .\) (Supongamos que la capacidad calorífica del gas,\(C_{V}\), es independiente de la temperatura.) Pista: La energía potencial del entorno cambia en\(m_{2} g \Delta h\); dado que la energía cinética del pistón y los pesos es cero al principio y al final del proceso, y el límite es adiabático, la energía interna del gas debe cambiar por\(-m_{2} g \Delta h=-m_{2} g \Delta V / A_{\mathrm{s}}=-p_{2} \Delta V\).
(c) Podría parecer que al hacer que el peso colocado sobre el pistón sea suficientemente grande,\(V_{2}\) podría hacerse lo más cercano a cero como se desee. En realidad, sin embargo, este no es el caso. Encuentre expresiones para\(V_{2}\) y\(T_{2}\) en el límite a medida que\(m_{2}\) se acerca al infinito, y evalúe\(V_{2} / V_{1}\) en este límite si la capacidad calorífica es\(C_{V}=(3 / 2) n R\) (el valor de un gas monatómico ideal a temperatura ambiente).
3.7 La curva sólida en la Fig. \(3.7\)muestra la trayectoria de una expansión adiabática reversible o compresión de una cantidad fija de un gas ideal. La información sobre el gas se da en la leyenda de la figura. Para la compresión a lo largo de este camino, comenzando en\(V=0.3000 \mathrm{dm}^{3}\)\(T=300.0 \mathrm{~K}\) y terminando en\(V=0.1000 \mathrm{dm}^{3}\), encontrar la temperatura final hasta\(0.1 \mathrm{~K}\) y el trabajo.
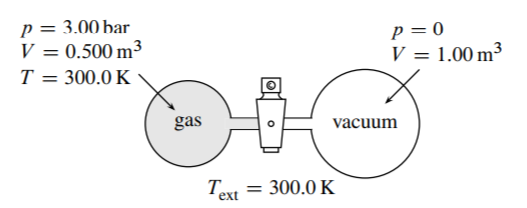
3.8 La figura\(3.26\) muestra el estado inicial de un aparato que contiene un gas ideal. Cuando se abre la llave de paso, el gas pasa al recipiente evacuado. El sistema es el gas. Encuentra\(q, w\), y\(\Delta U\) bajo las siguientes condiciones.
a) Los vasos tienen paredes adiabáticas.
b) Los recipientes tienen paredes diatérmicas en contacto térmico con un baño de agua mantenido a\(300 . \mathrm{K}\), y la temperatura final en ambos recipientes es\(T=300 . \mathrm{K}\).
3.9 Considerar un proceso reversible en el que el eje del sistema A en la Fig. \(3.11\)hace una revolución en la dirección de aumentar\(\vartheta\). Demostrar que el trabajo gravitacional del peso es el mismo que el trabajo de eje dado por\(w=m g r \Delta \vartheta\).
Cuadro 3.2 Datos para el Problema 3.10. Los valores son del papel 1850 de Joule\(^{a}\) y se han convertido a unidades SI.
\({ }^{a}\)Ref. [91], p. 67, experimento\(5 .\)
\({ }^{b}\) Calculado a partir de las masas y capacidades caloríficas específicas de los materiales.
3.10 Este problema le guía a través de un cálculo del equivalente mecánico del calor utilizando datos de uno de los experimentos de James Joule con un aparato de rueda de paletas (ver Sec. 3.7.2). Los datos experimentales se recogen en la Tabla 3.2.
En cada uno de sus experimentos, Joule permitió que los pesos del aparato se hundieran al suelo veinte veces desde una altura de aproximadamente\(1.6 \mathrm{~m}\), utilizando una manivela para elevar los pesos antes de cada descenso (ver Fig. \(3.14\)en la página 89). La rueda de paletas se enganchó a las pesas a través del rodillo y las cuerdas solo mientras las pesas descendían. Cada descenso tomó alrededor de 26 segundos, y todo el experimento duró 35 minutos. Joule midió la temperatura del agua con un termómetro sensible de mercurio en vidrio tanto al inicio como al final del experimento.
Para los efectos de los cálculos, defina el sistema como la combinación del recipiente, su contenido (incluyendo la rueda de paletas y el agua), y su tapa. Todas las energías se miden en un marco de laboratorio. Ignorar la pequeña cantidad de trabajo de expansión que se produce en el experimento. Ayuda conceptualmente pensar en la sala de bodega en la que Joule instaló su aparato como efectivamente aislado del resto del universo; entonces el único entorno que debes considerar para los cálculos es la parte de la habitación fuera del sistema.
(a) Calcular el cambio de la energía potencial gravitacional\(E_{\mathrm{p}}\) de los pesos de plomo durante cada uno de los descensos. Para la aceleración de la caída libre en Manchester, Inglaterra (donde Joule realizó el experimento) utilice el valor\(g=9.813 \mathrm{~m} \mathrm{~s}^{-2}\). Este cambio energético representa una disminución en la energía del entorno, y sería igual en magnitud y opuesto en señal al trabajo de agitación realizado en el sistema si no hubiera otros cambios en el entorno.
(b) Calcular la energía cinética\(E_{\mathrm{k}}\) de los pesos descendentes justo antes de llegar al piso. Esto representa un incremento en la energía del entorno. (Esta energía se disipó en energía térmica en los alrededores cuando los pesos llegaron a descansar en el piso).
(c) Joule encontró que durante cada descenso de los pesos, la fricción en las cuerdas y poleas disminuyó la cantidad de trabajo realizado en el sistema por\(2.87 \mathrm{~J}\). Esta cantidad representa un incremento en la energía térmica del entorno. Joule también consideró el ligero estiramiento de las cuerdas mientras las pesas se suspendieron de ellas: cuando las pesas llegaron a descansar en el suelo, se alivió la tensión y la energía potencial de las cuerdas cambió por\(-1.15 \mathrm{~J}\). Encuentra el cambio total en la energía del entorno durante todo el experimento a partir de todos los efectos descritos hasta este punto. Tenga en cuenta que los pesos descendieron 20 veces durante el experimento.
(d) Los datos en la Tabla\(3.2\) muestran que el cambio de la temperatura del sistema durante el experimento fue
\ [
\ Delta T =( 289.148-288.829)\ mathrm {K} =+0.319\ mathrm {~K}
\]
La embarcación con rueda de paletas no tenía aislamiento térmico, y la temperatura del aire fue más ligero más cálido, por lo que durante el experimento hubo una transferencia de algo de calor al sistema. A partir de un procedimiento de corrección descrito por Joule, se estima que es el cambio de temperatura que se habría producido si el recipiente hubiera sido aislado\(+0.317 \mathrm{~K}\).
Utilice esta información junto con sus resultados de la parte (c) para evaluar el trabajo necesario para aumentar la temperatura de un gramo de agua en un kelvin. Este es el “equivalente mecánico del calor” a la temperatura promedio del sistema durante el experimento. (Como se menciona en la p. 87, Joule obtuvo el valor\(4.165 \mathrm{~J}\) basado en los 40 experimentos.)
3.11 Refiérase al aparato representado en la Fig. \(3.1\)en la página 61. Supongamos que la masa del peso externo es\(m=1.50 \mathrm{~kg}\), la resistencia de la resistencia eléctrica es\(R_{\mathrm{el}}=5.50 \mathrm{k} \Omega\), y la aceleración de caída libre es\(g=9.81 \mathrm{~m} \mathrm{~s}^{-2}\). ¿Durante cuánto tiempo necesitará operar la celda externa, proporcionando una diferencia de potencial eléctrico\(|\Delta \phi|=1.30 \mathrm{~V}\), para provocar el mismo cambio en el estado del sistema que el cambio cuando el peso se hunde\(20.0 \mathrm{~cm}\) sin trabajo eléctrico? Supongamos que ambos procesos ocurren adiabáticamente.


