8.9: Los valores permitidos de J - el número cuántico de momento angular total
- Page ID
- 79653
- Compate dos esquemas de acoplamiento espín-órbita que acoplan el momento angular de espín total y el momento angular orbital total de un espectro multi-electrón
Necesitamos ser capaces de identificar los estados electrónicos que resultan de una configuración electrónica dada y determinar sus energías relativas. Un estado electrónico de un átomo se caracteriza por una energía específica, función de onda (incluyendo espín), configuración electrónica, momento angular total y la forma en que los momentos orbitales y angulares de espín de los diferentes electrones se acoplan entre sí. Hay dos descripciones para el acoplamiento del momento angular. Uno se llama acoplamiento j-j, y el otro se llama acoplamiento L-S. El esquema de acoplamiento j-j se utiliza para elementos pesados (z > 40) y el esquema de acoplamiento L-S para los elementos más ligeros. Solo el acoplamiento L-S se discute a continuación.
Acoplamiento L-S de Momenta Angular
El acoplamiento L-S también se llama acoplamiento R-S o Russell-Saunders. En el acoplamiento L-S, los momentos orbitales y angulares de espín de todos los electrones se combinan por separado
\[L = \sum _i l_i \label{8.11.3} \]
\[S = \sum _i s_i \label{8.11.4} \]
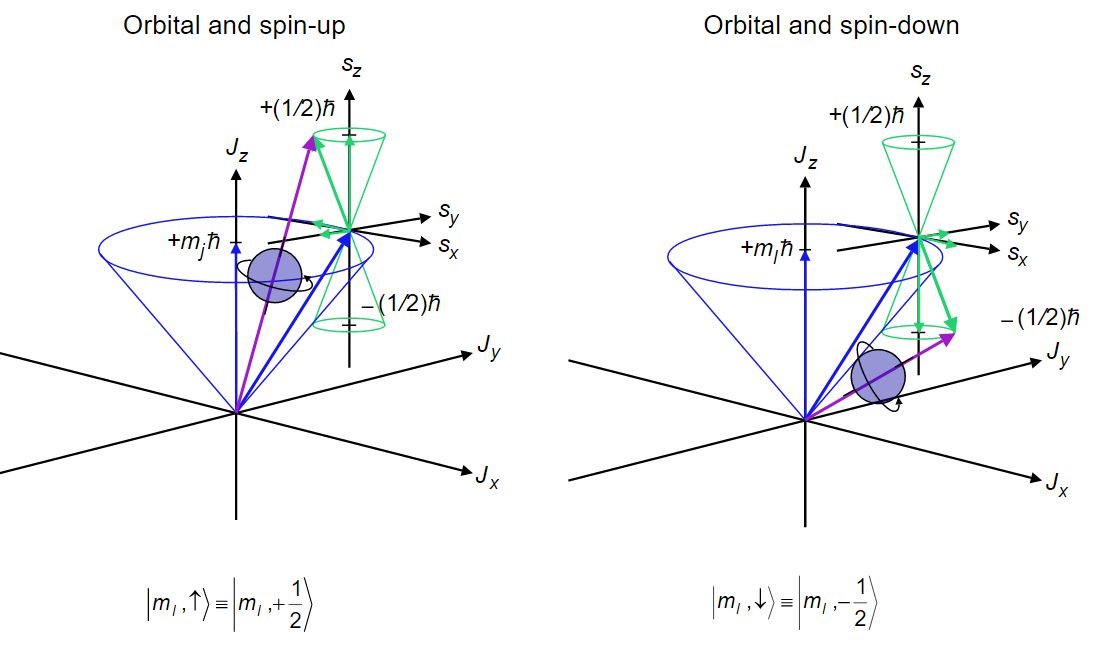
El vector de momento angular total es entonces la suma del vector de momento angular orbital total y el vector de momento angular de giro total.
\[J = L + S \label{8.11.5} \]
El número cuántico de momento angular total parametriza el momento angular total de una partícula dada, combinando su momento angular orbital y su momento angular intrínseco (es decir, su giro). Debido a la interacción espín-órbita en el átomo, el momento angular orbital ya no conmuta con el hamiltoniano, ni el giro.

Sin embargo el momento angular total\(J\) sí conmuta con el hamiltoniano y así es una constante de movimiento (no cambia en el tiempo). Las definiciones relevantes del momento angular son:
Momento angular orbital
\[|\vec{L}| = \hbar \sqrt{\ell(\ell+1)} \nonumber \]
con su proyección en el eje z\[L_z = m_\ell \hbar \nonumber \]
Momento angular de giro
\[ |\vec{S}| = \hbar \sqrt{s(s+1)} \nonumber \]
con su proyección en el eje z\[ S_z = m_s \hbar \nonumber \]
Momento Angular Total
\[ |\vec{J}| = \hbar \sqrt{j(j+1)} \nonumber \]
con su proyección en el eje z\[ J_z = m_j \hbar \nonumber \]
donde
- \(l\)es el número cuántico azimutal de un solo electrón,
- \(s\)es el número cuántico de espín intrínseco al electrón,
- \(j\)es el número cuántico de momento angular total del electrón,
Los números cuánticos toman los valores:
\[\begin{align} & m_\ell \in \{ -\ell, -(\ell-1) \cdots \ell-1, \ell \} , \quad \ell \in \{ 0,1 \cdots n-1 \} \\& m_s \in \{ -s, -(s-1) \cdots s-1, s \} , \\& m_j \in \{ -j, -(j-1) \cdots j-1, j \} , \\& m_j=m_\ell+m_s, \quad j=|\ell+s|\\\end{align} \nonumber \]
y las magnitudes son:
\[\begin{align} & |\textbf{J}| = \hbar\sqrt{j(j+1)} \\& |\textbf{J}_1| = \hbar\sqrt{j_1(j_1+1)} \\& |\textbf{J}_2| = \hbar\sqrt{j_2(j_2+1)} \\\end{align} \nonumber \]
en el que
\[ j \in \{ |j_1 - j_2|, |j_1 - j_2| - 1 \cdots j_1 + j_2 - 1, j_1 + j_2 \} \,\! \nonumber \]
Este proceso puede repetirse para un tercer electrón, luego el cuarto etc. hasta que se haya encontrado el momento angular total.
El resultado de estas sumas vectoriales se especifica en un código que se denomina símbolo de término Russell-Saunders, y cada símbolo de término identifica un nivel de energía del átomo. En consecuencia, los niveles de energía también se denominan términos. Un símbolo de término tiene la forma\(^{2s+1} L_J\) donde la letra de código que se utiliza para el número cuántico de momento angular orbital total L = 0, 1, 2, 3, 4, 5 es S, P, D, F, G, H, respectivamente. Observe cómo este código coincide con el utilizado para los orbitales atómicos. El superíndice\(2S+1\) da la multiplicidad de espín del estado, donde S es el número cuántico de momento angular de giro total. La multiplicidad de giro es el número de estados de giro asociados a un estado electrónico dado. Para no confundir la letra de código S para el momento angular orbital con el número cuántico de giro S, se debe examinar el contexto en el que se usa cuidadosamente. En el término símbolo, el subíndice J da el número cuántico de momento angular total. Debido al acoplamiento espín-órbita, solo\(J\) y\(M_j\) son números cuánticos válidos, pero debido a que el acoplamiento spin-órbita es débil\(L\),\(M_l\),\(S\), y\(m_s\) todavía sirven para identificar y caracterizar los estados para los elementos más ligeros.
Por ejemplo, el estado base, es decir, el estado de energía más baja, del átomo de hidrógeno corresponde a la configuración electrónica en la que el electrón ocupa el orbital espacial 1s y puede tener espín\(\alpha\) o espín\(\beta\). El término símbolo para el estado base es\(^2 S_{1/2}\), que se lee como “doblete S 1/2”. El número cuántico de espín es 1/2 por lo que el superíndice 2S+1 = 2, lo que da la multiplicidad de espín del estado, es decir, el número de estados de giro es igual a 2 correspondientes a\(\alpha\) y\(\beta\). El S en el término símbolo indica que el número cuántico de momento angular orbital total es 0 (Para el estado base del hidrógeno, solo hay un electrón y está en un s-orbital con\(l = 0\)). El subíndice ½ se refiere al número cuántico de momento angular total. El momento angular total es la suma del espín y los momentos angulares orbitales para los electrones en un átomo. En este caso, el número cuántico de momento angular total es solo el número cuántico de momento angular de giro, ½, ya que el momento angular orbital es cero. El estado base tiene una degeneración de dos debido a que el momento angular total puede tener una proyección del eje z de\(+\frac {1}{2} \hbar\) o\(-\frac {1}{2} \hbar\), correspondiente a\(m_J\) = +1/2 o -1/2 resultante de los dos estados de espín de electrones\(\alpha\) y\(\beta\). También podemos decir, de manera equivalente, que el término estado base o nivel de energía es doblemente degenerado.
Escriba el término símbolo para un estado que tenga 0 tanto para los números cuánticos de giro como de momento angular orbital.
Escriba el símbolo del término para un estado que tenga 0 para el giro y 1 para los números cuánticos de momento angular orbital
Colaboradores y Atribuciones
Adapted from "Quantum States of Atoms and Molecules" by David M. Hanson, Erica Harvey, Robert Sweeney, Theresa Julia Zielinski

