13.14: La teoría de grupos determina la actividad infrarroja
- Page ID
- 79834
Determinar si un modo normal es IR o Raman Activo
Una transición de\(v \rightarrow v'\) es IR activa si la integral del momento de transición contiene la representación irreducible totalmente simétrica del grupo puntual al que pertenece la molécula. La integral del momento de transición se deriva del oscilador armónico unidimensional. Usando la definición de momento dipolo eléctrico\(\mu\), la integral es:
\[ M(v \rightarrow v') = \langle \text{final wavefunction} | \vec{\mu} | \text{initial wavefunction } \rangle \nonumber \]
o en términos de ondas vibracionales para un modo normal específico\( | \phi (v) \rangle \)
\[ M(v \rightarrow v') = \langle \phi(v' \neq 0) | \vec{\mu} | \phi (v=0) \rangle \label{M1} \]
asumiendo la transición de la\(v=0\) función de\(v' \neq 0\) onda a la función de onda.
Ahora bien, consideremos el caso que\(\vec{μ}\), es una constante y por lo tanto independiente de la vibración (es decir, el momento dipolo eléctrico no cambia durante la vibración). Esto se podría tomar fuera de la integral en Ecuación\(\ref{M1}\) se convierte
\[ M(v \rightarrow v') = \vec{\mu} \langle \phi(v' \neq 0) | \phi (v=0) \rangle \label{M2} \]
Dado que\(|\phi(v=0) \rangle \) y\(|\phi(v =\neq0) \rangle \) son mutuamente ortogonales entre sí, la integral en Ecuación\(\ref{M1}\) será igual a cero y no se permitirá la transición (es decir, está prohibida). Para\(M\) que el sea distinto de cero,\(\vec{μ}\) debe cambiar durante una vibración. Esta regla de selección explica por qué las moléculas diatómicas homonucleares no producen un espectro IR. No hay cambio en el momento dipolar que resulte en un momento de transición integral de cero y una transición que está prohibida.
Para que una transición sea Raman activo, se aplican las mismas reglas. La integral del momento de transición debe contener la representación irreducible totalmente simétrica del grupo de puntos. La integral contiene el tensor de polarizabilidad\(\alpha\) (generalmente representado por una matriz cuadrada):
\[ M(v \rightarrow v') = \langle \phi(v' \neq 0) | \alpha | \phi (v=0) \rangle \label{M3} \]
Siguiendo un argumento similar al anterior,\(\alpha\) debe ser distinto de cero para que se permita la transición y exhiba dispersión Raman.
Tabla de caracteres
Para que una molécula sea IR activa el momento dipolar tiene que cambiar durante la vibración. Para que una molécula sea Raman activa la polarizabilidad de la molécula tiene que cambiar durante la vibración. La representación reducible γ vib también se puede encontrar determinando la representación reducible de los 3N grados de libertad de H 2 O, γ tot. Al aplicar la Teoría de Grupos es sencillo encontrar γ x , y, z así como UMA (número de átomos inmóvil). Nuevamente, usando agua como ejemplo con simetría C 2v donde 3N = 9, se puede determinar γ tot:
| C 2v | E | C 2 | σ (xz) | σ (yz) | |
|---|---|---|---|---|---|
| T5 x, y, z | 3 | -1 | 1 | 1 | |
| UMA | 3 | 1 | 1 | 3 | |
| γ tot | 9 | -1 | 1 | 3 | =3a 1 + a 2 + 2b 1 + 3b 2 |
| Tenga en cuenta que γ tot contiene nueve grados de libertad consistentes con 3N = 9. | |||||
γ tot contiene γ traslacional, γ rotacional así como γ vibracional. γ trans se puede obtener encontrando las representaciones irreducibles correspondientes a x, y y z en el lado derecho de la tabla de caracteres, γ rot encontrando las correspondientes a R x, R y y Rz. γ vib se puede obtener por γ tot - γ trans - γ rot.
\[Γ_{vib} (H_2O) = (3a_1 + a_2 + 2b_1+ 3b_2) - (a_1 + b_1 + b_2) - (a_2 + b_1 + b_2) = 2a_1 + b_2 \nonumber \]
Para determinar qué modos están activos IR, es necesaria una comprobación simple de la representación irreducible que corresponde a x, y y z y una comprobación cruzada con la representación reducible γ vib. Si contienen la misma representación irreducible, el modo es IR activo.
Para H 2 O, z se transforma como a 1, x como b 1 e y como b 2. Los modos a1 y b2 son IR activos ya que γvib contiene 2a 1 + b 2.
Para determinar qué modos están activos Raman, se utiliza la representación irreducible que corresponde a z 2, x 2 -y 2, xy, xz e yz y se vuelve a cruzar con γvib. Para H 2 O, z 2 y x 2 -y 2 transforman como a 1, xy como a 2, xz como b 1 e yz como b 2. Los modos a 1 y b 2 también están activos Raman ya que γ vib contiene ambos modos.
El espectro IR de H2O de hecho tiene tres bandas según lo predicho por la Teoría de Grupos. Los dos tramos simétricos v1 y v2 ocurren a 3756 y 3657 cm-1 mientras que el movimiento de flexión v3 ocurre a 1595 cm-1.
Para determinar qué modos normales son las vibraciones de estiramiento y cuáles son las vibraciones de flexión, se puede realizar un análisis de estiramiento. Entonces las vibraciones de estiramiento se pueden deducir de las vibraciones totales para obtener las vibraciones de flexión. Una flecha de doble punta se dibuja entre el átomo como se representa a continuación:
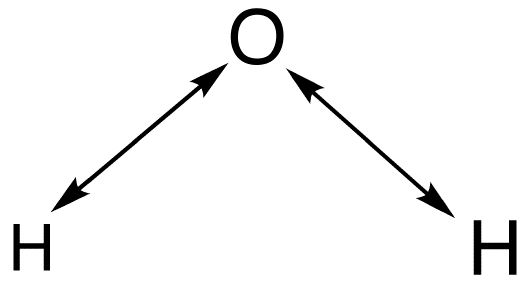
Luego, una determinación de cómo las flechas se transforman bajo cada operación de simetría en simetría C2v arrojará los siguientes resultados:
| C 2v | E | C 2 | σ (xz) | σ (yz) | |
|---|---|---|---|---|---|
| γ estiramiento | 2 | 0 | 0 | 2 | = a 1 + b 2 |
\[Γ_{bend} = Γ_{vib} - Γ_{stretch} = 2a_1 + b_2 -a_1 - b_2 = a_1 \nonumber \]
H 2 O tiene dos vibraciones de estiramiento así como una vibración de flexión. Este concepto puede expandirse a moléculas complejas como PtCl4 -. Se pueden dibujar cuatro flechas de doble punta entre los átomos de la molécula y determinar cómo éstas se transforman en simetría D 4h. Una vez que se ha elaborado la representación irreducible para γ stretch, γ bend puede ser determinada por γ bend = γ vib - γ stretch.
La mayoría de las moléculas están en su energía de punto cero a temperatura ambiente. Por lo tanto, la mayoría de las transiciones se originan a partir del estado v=0. Algunas moléculas sí tienen una población significativa del estado v=1 a temperatura ambiente y las transiciones de este estado térmicamente excitado se denominan bandas calientes.
Referencias
- Merlín, J.C., Cornard, J.P., J. Chem. Educ., 2006, 83 (9), p. 1383. DOI: 10.1021/ed083p1393
- McGuinn, C.J., J. Chem. Educ., 1982, 59 (10), pág. 813. DOI: 10.1021/ed059p813
- Harris, D.C., Bertolucci, M.D., Simetría y Espectroscopia: Una introducción a la Espectroscopia Vibracional y Electrónica. Dover Publocations, Inc., Nueva York, 1989.
- McQuarrie, D. A., Simon, J.D., Physical Chemistry: A Molecular Approach, University Science Books, Sausalito, California, 1997; 518-521.
- Housecroft, C.E., Sharpe, A.G., Química Inorgánica. Pearson Education Limited, Inglaterra, 2008, 107.
- Atkins, P., DeAula, J., Química Física, W.H. Freeman and Company, Nueva York, 2002, 520-523.
- Bishop, D.M., Teoría y Química de Grupos, Dover Publications, Inc, Nueva York, 1973, 166.

