4.9: Dibujos tridimensionales
- Page ID
- 80575
Nuestro propósito en este capítulo es poder representar la estructura de una molécula. Cuando dibujamos la estructura de Lewis para metano, es solo una representación bidimensional, pero realmente el compuesto tiene una forma tridimensional. El carbono central en el metano es tetraédrico, con los cuatro hidrógenos en las esquinas alternas de un cubo.
Podemos dibujar un tetraedro haciendo un vértice entre dos líneas, luego uniendo una línea acuñada y una línea rayada al exterior de la esquina. La línea negra, acuñada se lee como “este átomo está hacia nosotros”. La línea rayada se lee como “este átomo está más lejos de nosotros”. Aunque el dibujo es plano, las líneas rayadas y acuñadas son una notación abreviada para la tridimensionalidad.
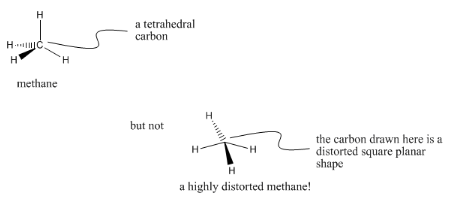
La representación de la forma tridimensional de una molécula se puede hacer en papel, pero solo si somos muy cuidadosos al dibujar convenciones como los dibujos de cuña y guiones.
Los carbonos que tienen enlaces a cuatro vecinos diferentes son siempre tetraédricos. Los vecinos dispuestos alrededor de un carbono tetraédrico están separados alrededor de 109°. En ocasiones, por razones en las que no vamos a entrar aquí, los carbonos tetraédricos se llaman carbonos sp3.
El pentano es un compuesto que contiene cuatro carbonos tetraédricos seguidos. Cada carbono tetraédrico podría mostrarse con proyecciones de cuña - guión.
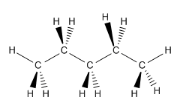
También es muy común usar programas de dibujo por computadora para mostrar las formas de las moléculas. Se puede ver la estructura tridimensional del pentano de muchas maneras diferentes. Aquí se muestran tres de las formas más comunes. Ball & Stick es una manera fácil de ver dónde están todos los átomos y cómo están conectados. Wireframe le permite ver conexiones sin tener su vista oscurecida por átomos. Los modelos de relleno de espacio están pensados para mostrarle más de cerca la forma de la molécula, aunque los átomos involucrados se oscurecen en esta vista.
Ir a Animación IM9.1. Un modelo tridimensional de pentano.
Los carbonos doblemente unidos a un vecino, y consecuentemente unidos a tres vecinos diferentes en general, son planos trigonales. Los vecinos están todos en el mismo plano y están a unos 120 ° de distancia. Los carbonos planos trigonales a veces se describen como carbonos sp2.
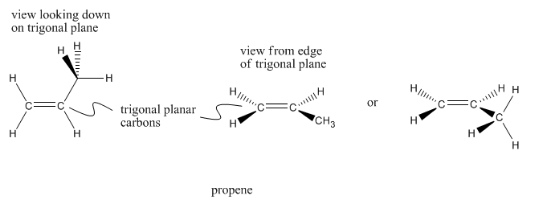
El propeno tiene dos carbonos planos trigonales, así como un carbono tetraédrico. Observe que un carbono plano trigonal es plano si se ve desde una dirección, pero no si se ve desde la otra. A veces verás los carbonos trigonales dibujados de manera diferente, si el cajón quiere que mires la molécula desde una dirección u otra.
Consulta si puedes encontrar ambos tipos de carbono en el modelo a continuación.
Ir a Animación IM9.2. Un modelo tridimensional de propeno.
Los carbonos que solo tienen dos vecinos diferentes son lineales; cada vecino está separado 180 ° del otro. Los carbonos lineales a veces se denominan carbonos sp.
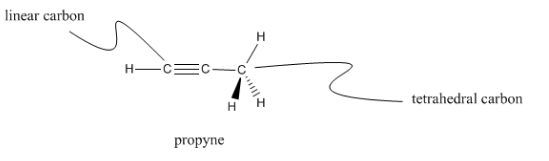
El propino tiene dos carbonos lineales así como un carbono tetraédrico. Consulta si puedes encontrar ambos tipos de carbono en el modelo a continuación.
Ir a Animación IM9.3. Un modelo tridimensional de propino.
Decir que un carbono es sp o sp2 solo está dando la forma de un átomo dentro de una molécula. La propia molécula puede tener una forma particular que está determinada por las geometrías de sus átomos constituyentes, pero que no puede describirse simplemente en palabras como “tetraédrica” o “lineal”.
El pentano es más o menos una forma de zig-zag. En un modelo de relleno de espacio, se asemeja a una oruga gorda avanzando lentamente. El propeno es casi en forma de bumerán. El propino tiene forma de dardo; tiene un extremo puntiagudo y un extremo emplumado.
Otras moléculas tienen formas más complicadas. La forma del ginkgolido B (un producto natural aislado del árbol ginkgo biloba medicinalmente interesante) es difícil de describir. Sin embargo, es claro que los carbonos individuales en el ginkgólido B son en su mayoría tetraédricos, con solo un par de carbonos planos trigonales.
Ir a Animación IM9.4. Un modelo tridimensional de ginkgolide B.
Comprender la forma general de una molécula es particularmente importante en diversos aspectos de la bioquímica. Por ejemplo, el efecto de cualquier fármaco en el cuerpo está fuertemente influenciado por la forma de la droga y cómo esa forma puede interactuar con receptores específicos.
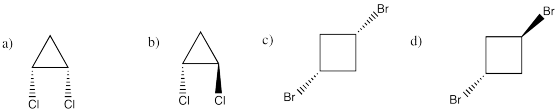
Los isómeros cíclicos cis y trans tienen dos sustituyentes unidos a un anillo. El isómero cis tiene ambos sustituyentes en la misma cara del anillo. El isómero trans tiene sustituyentes en caras opuestas del anillo. Utilice proyecciones de cuña y guiones para dibujar las formas de las siguientes moléculas:
- cis -1,2-diclorociclopropano, C 3 H 4 Cl 2 (los números significan que hay cloro en el primer carbono y una clorina en el segundo carbono)
- trans-1,2-diclorociclopropano, C 3 H 4 Cl 2 c) cis-1,3-dibromociclobutano, C 4 H 6 Br 2 d) trans-1,3-dibromociclobutano, C 4 H 6 Br 2
- cis -1,3-dibromociclobutano, C 4 H 6 Br 2
- trans -1,3-dibromociclobutano, C 4 H 6 Br 2
- Contestar
-
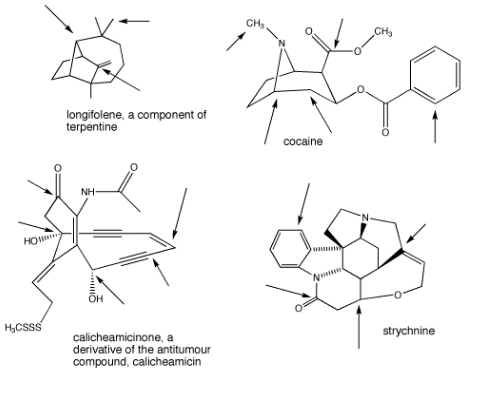
Identificar la geometría en los carbonos indicados en las siguientes moléculas:
- Contestar
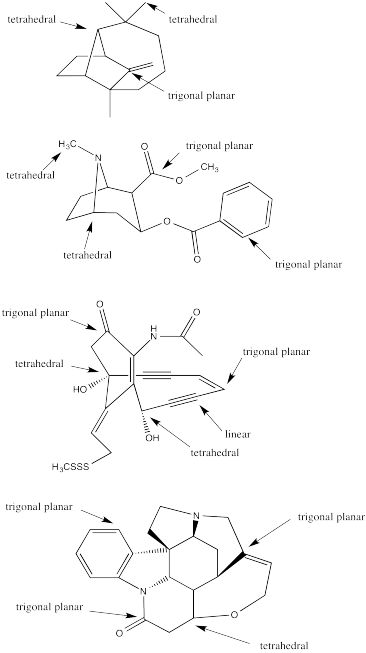
RespuestaEjercicio 4.9.2, que muestra fórmulas estructurales para longifoleno, cocaína, caliqueamicinona y estricnina.

