5.15: Otro tipo de estereoquímica- isómeros de alqueno
- Page ID
- 80573
Los isómeros relacionados por quiralidad no son el único tipo de isómeros geométricos. Otro ejemplo es el isomerismo cis-trans en alquenos; es decir, diferentes orientaciones alrededor de un doble enlace carbono-carbono (y otros dobles enlaces, en algunos casos).
En los isómeros cis, hay un grupo no hidrógeno en cada extremo del alqueno, y están en el mismo lado del eje del doble enlace.
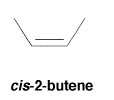
Figura\(\PageIndex{1}\): Un isómero cis de un alqueno.
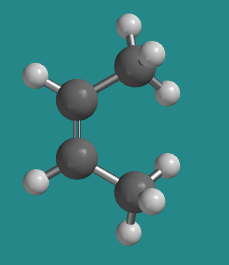
Ir a Animación SC12.1. Un modelo tridimensional de cis-2-buteno.
En los isómeros trans, hay un grupo no hidrógeno en cada extremo del alqueno, y están en los lados opuestos del eje del doble enlace.
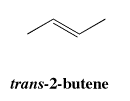
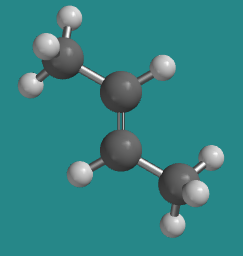
Ir a Animación SC12.1. Un modelo tridimensional de trans -2-buteno.
- En los isómeros cis, los grupos que no son hidrógeno en cada extremo de un alqueno están en el mismo lado.
- En los isómeros trans, los grupos que no son hidrógeno en cada extremo de un alqueno están en lados opuestos.
Este tipo de isomería es diferente a los cambios de forma que se observan en los hidrocarburos saturados como el butano; es decir, los compuestos que solo tienen enlaces simples, y no dobles enlaces, no tienen estos isómeros específicos. (Sin embargo, las estructuras de anillos saturados pueden tener isómeros cis y trans; en ese caso, los términos describen si dos grupos están en la misma cara de un anillo o caras opuestas). Hay rotación libre en butano, porque los enlaces simples que mantienen unidos los carbonos no son tan sensibles a la orientación de los carbonos tetraédricos en ninguno de los extremos del enlace. Por el contrario, girar el carbono plano trigonal en un extremo de un doble enlace interrumpiría el solapamiento orbital p que forma el enlace pi. Eso costaría mucha energía.
Los isómeros cis y trans desempeñan importantes papeles biológicos. Por ejemplo, una de las proteínas responsables de la visión es la rodopsina. La rodopsina le ha unido un compuesto orgánico llamado retinal (el oxígeno en la retina es reemplazado por un nitrógeno en una cadena lateral de aminoácidos en la proteína para formar rodopsina activa).
Uno de los enlaces en la forma activa de retinal tiene una configuración cis. Es posible que sepas por análisis conformacional que habría cierto hacinamiento entre los grupos que se mantienen muy unidos por un lado del doble vínculo. Ese hacinamiento, a veces llamado cepa estérica, provoca un aumento en la energía.
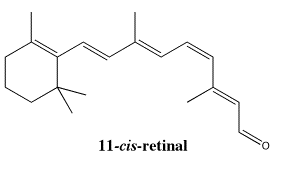
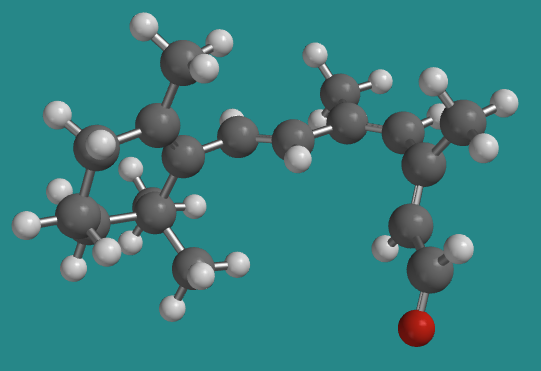
Ir a Animación SC12.1. Un modelo tridimensional de cis-retinal.
Sin embargo, si un fotón es absorbido por la molécula, un electrón puede ser excitado desde un nivel de estado básico a un nivel de estado excitado. Este electrón ocuparía entonces un orbital antienlace pi, debilitando la unión pi en el sistema. Eso facilita la rotación de la molécula, y lo hace.
Una vez libre para rotar, la molécula adopta más fácilmente una forma más ope n, menos plegada. Se convierte en el isómero all- trans.
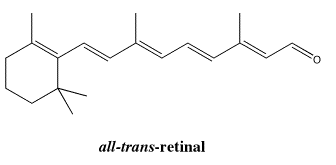
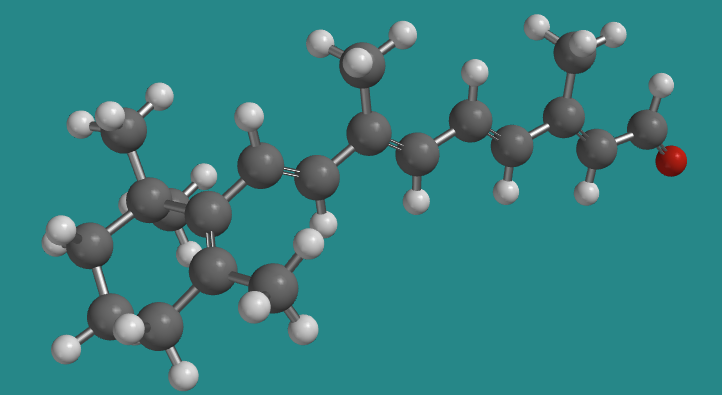
Ir a Animación SC12.1. Un modelo tridimensional de trans-retinal.
El cambio de forma en la retina es importante porque se une a la proteína rodopsina. La proteína se pliega alrededor de la retina, de modo que cuando la porción retiniana cambia de forma, la proteína tiene que sufrir un cambio conformacional para encajar alrededor de la retina. El cambio conformacional resultante de la proteína permite enviar una señal diciéndole al cerebro que se ha detectado luz en un lugar particular del ojo.
Ejercicio\(\PageIndex{1}\)
Determinar si las siguientes moléculas son cis, trans o ninguna.
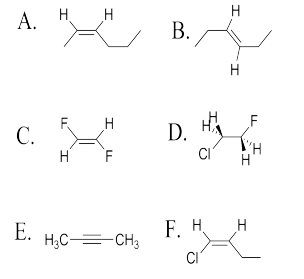
- Respuesta A.:
-
Cis
- Respuesta B.:
-
Trans
- Respuesta C.:
-
Trans
- Respuesta D.:
-
Ninguno (Hay rotación libre alrededor del enlace sencillo C-C).
- Respuesta E.:
-
Tampoco (los triples enlaces C-C tienen sustituyentes a 180 grados entre sí (lineales).)
- Respuesta F.:
-
Cis

