6.13: Más Práctica con Conformación
- Page ID
- 80688
Ejercicio\(\PageIndex{1}\)
Los enlaces de hidrógeno pueden tener una fuerte influencia en la forma molecular. Por ejemplo, es un factor clave para determinar la forma del ADN. En el ADN, los “pares de bases” en cadenas adyacentes de ADN se unen entre sí. Mostrar cómo la adenina y la timina, que se muestran en el siguiente dibujo, se unen hidrógeno entre sí.
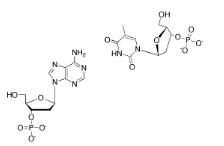
- Contestar
-
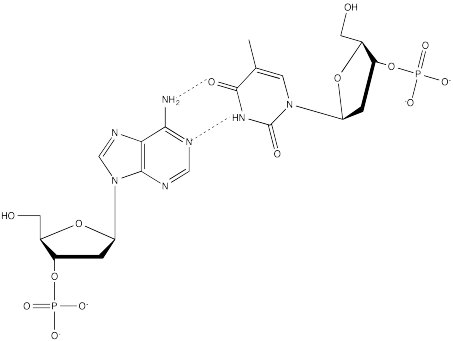
Ejercicio\(\PageIndex{2}\)
Mostrar cómo citosina y guanina, que se muestran en el siguiente dibujo, se unen hidrógeno entre sí.
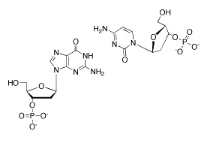
- Contestar
-
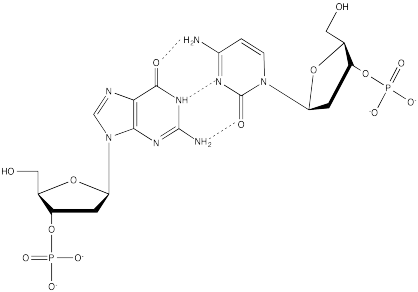
Ejercicio\(\PageIndex{3}\)
Mostrar por qué la timina no es adecuada para el enlace de hidrógeno con citosina y guanina.
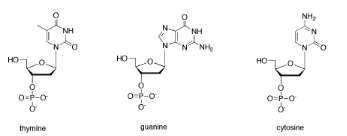
- Contestar
-
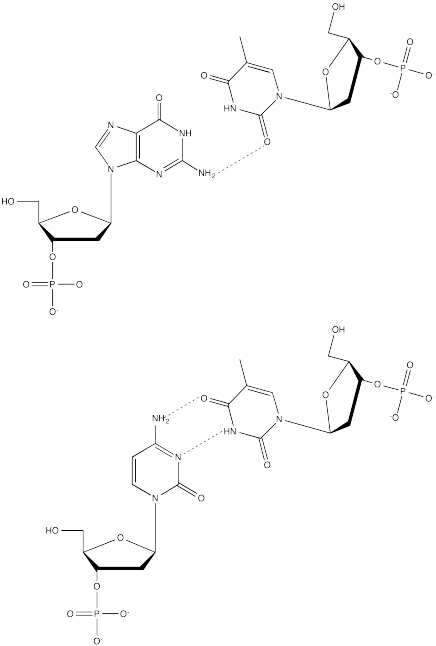
Ejercicio\(\PageIndex{4}\)
Eric Kool de la Universidad de Stanford ha utilizado “nucleótidos de diseño” para estudiar la ADN polimerasa y los mecanismos de reparación del ADN. Se ha interesado particularmente en cómo los esteros y los enlaces de hidrógeno afectan estas funciones. Se diseñó el siguiente conjunto de nucleótidos para imitar un nucleótido natural. Quizás sorprendentemente, estos nucleótidos son sustratos aceptables en lo que respecta a la ADN polimerasa, y pueden incorporarse en la posición “correcta” en el ADN.
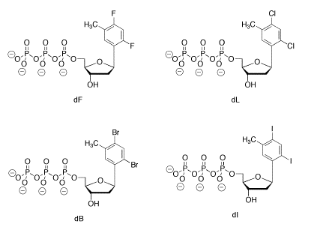
- ¿A qué nucleótido natural se asemejan más estas moléculas diseñadoras en forma?
- Mostrar cómo el nucleótido diseñador, dF, encajaría con el compañero de pares de bases correcto para ese nucleótido natural.
- Comparar y contrastar estos nucleótidos con el natural, en términos de su capacidad de enlace de hidrógeno con el “compañero de pares de bases” correcto.
- Comparar y contrastar estos nucleótidos con el natural, en términos de su capacidad para encajar con el “compañero de pares de bases” correcto en una molécula de ADN.
- Respuesta a:
-
5'-trifosfato de timina
- Respuesta b:
-
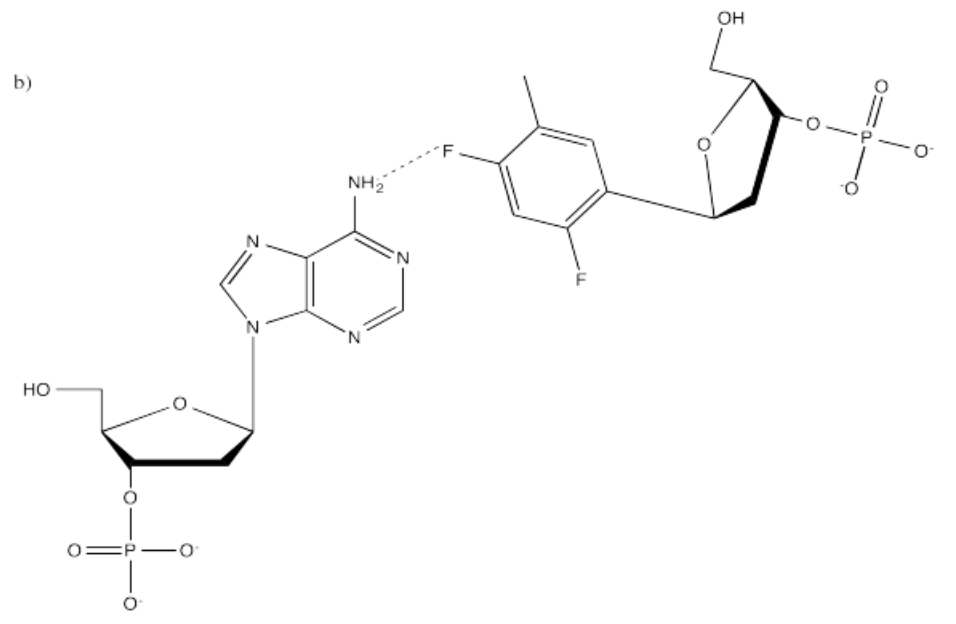
- Respuesta c:
-
dF solo es capaz de formar enlaces de hidrógeno con adinina en una posición, mientras que la timina puede hidrógeno en dos posiciones con la timina.
- Respuesta d:
-
dF es similar en tamaño y naturaleza electrónica a la timina. Los grupos flúor en dF son algo más pequeños que el oxígeno en la timina, pero presentan un grupo polar comprable que es capaz de actuar como aceptor de enlaces de hidrógeno. dF carece de la capacidad de donación de enlaces de hidrógeno como se ve en la timina.
Ejercicio\(\PageIndex{5}\)
A continuación se muestra otro de los “nucleótidos de diseño” de Kool.
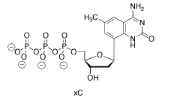
a) ¿Con qué nucleótido natural interactuaría xC más fuertemente? Mostrar la interacción.
b) Comparar y contrastar xC con su análogo natural, en términos de su capacidad de enlace de hidrógeno con el “compañero de pares de bases” correcto.
c) Comparar y contrastar xC con su análogo natural, en términos de su capacidad para encajar con el “compañero de pares de bases” correcto en una molécula de ADN.
- Respuesta a:
-
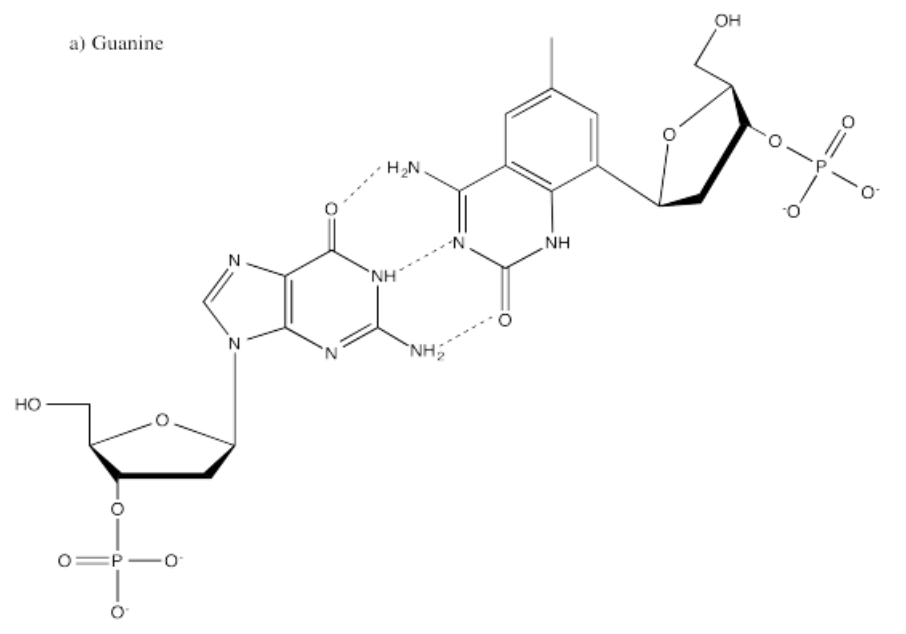
- Respuesta b:
-
xC es similar a la citosina. Ambas moléculas presentan donantes y aceptores de enlaces de hidrógeno en las mismas posiciones.
- Respuesta c:
-
Si bien xC es similar a la citosina en términos de colocación de donantes y aceptores de enlaces de hidrógeno, el anillo adicional crea problemas estéricos ya que los donantes y aceptores de enlaces de hidrógeno se colocan demasiado cerca del “compañero de pares de bases” correcto.

