7.1: Introducción a la Sustitución Aromática Electrofílica
- Page ID
- 78844
Los aromáticos, o arenos, son derivados del benceno u otros compuestos con sistemas de anillos aromáticos. Es decir, son cíclicos, planos, totalmente conjugados y tienen un número impar de pares π-electrón. Al igual que los alquenos, los aromáticos tienen electrones π que se sujetan sin apretar y son fácilmente atraídos por los electrófilos. Sin embargo, los aromáticos no experimentan las reacciones típicas de los alquenos.
Por ejemplo, el bromo no se agregará a través del doble enlace del benceno.
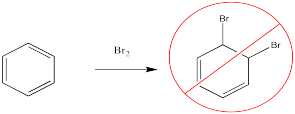
En cambio, un átomo de bromo reemplaza a uno de los átomos de hidrógeno en el benceno. Esta reacción se acelera enormemente en presencia de ácidos de Lewis, como el cloruro férrico.
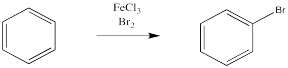
Una reacción similar ocurre con el cloro. Si se trata con gas cloro y un catalizador metálico, un átomo de cloro del gas cloro puede reemplazar un átomo de hidrógeno sobre el benceno. Sin embargo, lo mismo no funciona tan suavemente con los otros halógenos, yodo y flúor.
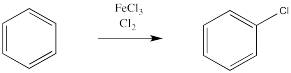
Las reacciones de cloro y bromo con benceno y otros aromáticos pueden ser catalizadas por una variedad de catalizadores metálicos ácidos de Lewis. También lo pueden hacer las reacciones de haluros de alquilo y haluros de acilo, que normalmente no pensamos como electrófilos para la adición de alquenos.
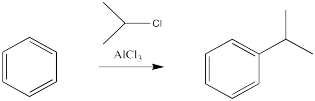
Hay algunas limitaciones sobre qué tipo de grupos se pueden agregar de esta manera. El carbono unido al haluro debe ser tetraédrico. Por lo general, es mucho más fácil agregar alquilos secundarios o terciarios que los primarios. Es decir, el carbono unido al halógeno tenía mejor estar unido también a otros dos o tres carbonos. Los metilos son muy, muy difíciles de agregar de esta manera.
Hay una excepción. El carbono unido al halógeno no necesita ser tetraédrico, siempre que sea un carbono carbonilo. Esa reacción se llama acilación.
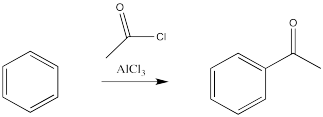
En estos casos, es el alquilo o acilo, más que el halógeno, el que reemplaza un átomo de hidrógeno en el benceno. Recuerde, lo más probable es que el benceno esté actuando como nucleófilo en esta reacción, a pesar de que está siguiendo una vía diferente a la que lo haría un alqueno. Está reaccionando con la parte más electrófila del haluro de alquilo o haluro de acilo.
Los aromáticos tienen un repertorio limitado de electrófilos con los que comúnmente experimentan reacción. Además de estas reacciones catalizadas por ácido de Lewis, también hay reacciones de medios ácidos fuertes, como una mezcla de ácido nítrico y sulfúrico.
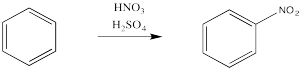
Otro medio ácido, denominado “ácido sulfúrico fumando”, es realmente una mezcla de ácido sulfúrico y trióxido de azufre.
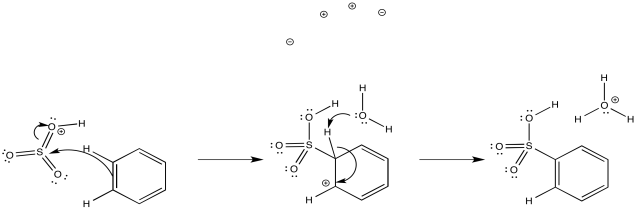
Al igual que con las reacciones catalizadas por ácido, el grupo nitro y el grupo sulfonato simplemente reemplazan un átomo de hidrógeno en el anillo de benceno. La reacción global implica la formación de enlaces entre un carbono de benceno y el electrófilo, y la escisión del enlace entre el mismo carbono y un protón.
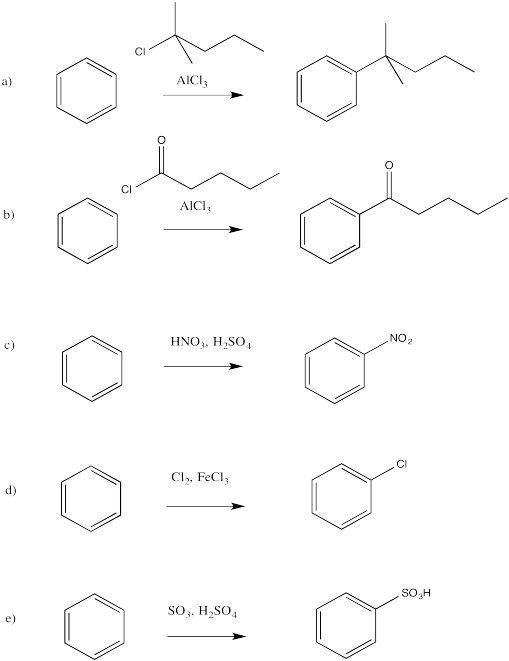
Rellene los reactivos faltantes en las siguientes reacciones.
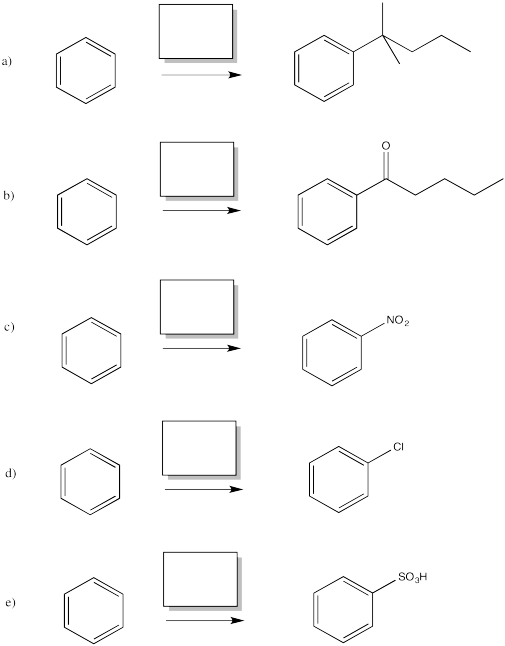
- Responder
-