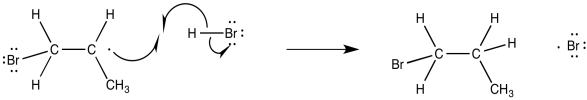6.8: Adición de radicales
- Page ID
- 79200
La adición radical a los alquenos es otro ejemplo clásico de una reacción radical. Al igual que la sustitución radical, ilustra algunos elementos importantes de la reactividad radical.
El ejemplo más común de adición radical a alquenos visto en los libros de texto universitarios de química es la adición radical de bromuro de hidrógeno, HBr. Eso es porque complementa la adición habitual de HBr a un alqueno.
En la adición habitual, HBr agrega de manera Markovnikov para colocar el bromo en el extremo más sustituido del alqueno y el hidrógeno en el extremo menos sustituido (recuerden el adagio, “los ricos se hacen más ricos y los pobres se vuelven más pobres”).
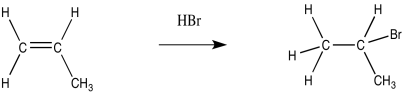
En contraste, la adición de HBr en condiciones radicales conduce a que el bromo se adhiera en la posición menos sustituida, mientras que los enlaces de hidrógeno a la posición más sustituida. Esta es una reacción de Robin Hood.
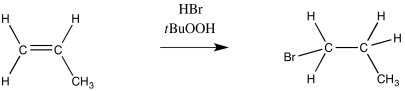
¿Cómo se produce esa inversión en regioquímica? Considerar el mecanismo de la reacción.
La adición radical de HBr casi siempre se realiza en presencia de peróxidos. El peróxido actúa como iniciador de la reacción. El enlace O-O puede romper la simple acción de la energía térmica (tal vez incluso a temperatura ambiente).
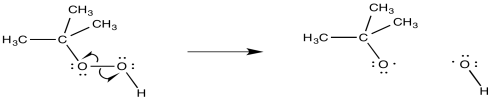
Los radicales alcoxi o hidroxi que resultan de esta etapa de iniciación se dejan inducir la propagación de radicales. Ciertamente, uno de los objetivos más fáciles disponibles es el enlace H-Br relativamente débil. La abstracción de un átomo de hidrógeno de HBr produce un radical bromo.
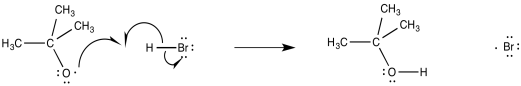
Una de las cosas que podría hacer el radical bromo es agregar al doble enlace de un alqueno. Cuando lo haga, se unirá a un extremo u otro del doble enlace anterior. ¿A qué fin irá?
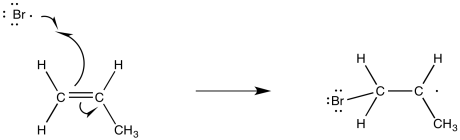
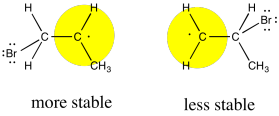
Al igual que los cationes, los radicales se consideran algo deficientes en electrones. Se estabilizan por factores donadores de electrones. Eso significa que, como un catión, el radical será más favorable sobre el carbono más sustituido del doble enlace formal.
Observe que este paso en realidad se rige por casi el mismo factor exacto que gobierna la adición polar de HBr. La regioquímica se rige por la estabilidad del intermedio. Una vez que ese evento ha ocurrido, se fija la regioquímica del producto. Solo queda para el radical alquilo arrancar un átomo de hidrógeno de otra molécula HBr, formando el producto final y generando otro radical bromo.