8.24: Polímeros de adición
- Page ID
- 75786
Los polímeros de adición se hacen usualmente a partir de un monómero que contiene un doble enlace. Podemos pensar en el doble enlace como “apertura” para participar en dos nuevos bonos simples de la siguiente manera:
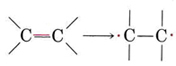
Así, si el eteno se calienta a temperatura y presión moderadas en presencia de un catalizador apropiado, polimeriza:
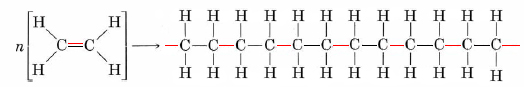
| Monómero | Nombre no sistemático | Polímero | Algunos usos típicos |
|---|---|---|---|
| Etileno | Polietileno | Película para empaques y bolsas, juguetes, botellas, recubrimientos | |
| Propileno | Polipropileno | Cartones de leche, cuerda, alfombras para exteriores | |
| Estireno | Poliestireno | Contenedores transparentes, vasos de plástico, refrigeradores, espuma de poliestireno | |
| Cloruro de vinilo | Cloruro de polivinilo, PVC | Tuberías y tubos, impermeables, cortinas, discos fonográficos, equipaje, baldosas | |
| Acrilonitrilo | Poliacrilonitrilo (Orlon, Acrilan) | Textiles, ruga | |
| Tetrafluoroetileno | Teflón | Recubrimientos antiadherentes para sartén, rodamientos, juntas |
El resultado es el familiar plástico ceroso llamado polietileno, que a nivel molecular consiste en una colección de moléculas de alcano de cadena larga, la mayoría de las cuales contienen decenas de miles de átomos de carbono. Sólo hay una cadena de ramificación corta ocasional.
El polietileno se fabrica actualmente a muy gran escala, más grande que cualquier otro polímero, y se utiliza para hacer bolsas de plástico, botellas baratas, juguetes, etc. muchas de sus propiedades son las que esperaríamos de su composición molecular. El hecho de que sea una mezcla de moléculas cada una de longitud de cadena ligeramente diferente (y por lo tanto un punto de fusión ligeramente diferente) explica por qué se ablanda en un rango de temperaturas en lugar de tener un solo punto de fusión. Debido a que las moléculas solo se mantienen unidas por las fuerzas londinenses, este derretimiento y ablandamiento ocurre a una temperatura bastante baja. (Algunas de las variedades más baratas de polietileno con cadenas más cortas y más cadenas ramificadas incluso se ablandarán en agua hirviendo). Las mismas fuerzas débiles de Londres explican por qué el polietileno es suave y fácil de rayar y por qué no es muy 'fuerte mecánicamente. '
La tabla anterior enumera algunos otros polímeros de adición conocidos y también algunos de sus usos. Probablemente puedas encontrar al menos un ejemplo de cada uno de ellos en tu hogar. Excepto el teflón, todos estos polímeros derivan de un monómero de la forma
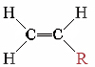
El polímero resultante tiene así la forma general
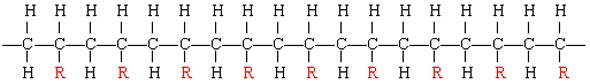
Variando la naturaleza del grupo R, las propiedades físicas del polímero se pueden controlar con bastante precisión.


