9.2: Propiedad de los Gases
- Page ID
- 75284
¿Por qué la persona promedio suele pasar por alto la presencia de gases? Probablemente porque las propiedades de los gases son tan discretas. Todos los gases son transparentes, y la mayoría son incoloros. Las principales excepciones a la segunda mitad de esta regla son flúor, F 2, y cloro, Cl 2, que son de color amarillo-verde pálido; bromo, Br 2, y dióxido de nitrógeno, NO 2, que son de color marrón rojizo; y yodo, I 2, que es violeta.
Créditos de imagen del cloro Imagen: Por W. Oelen (Home Science [woelen.homescience.net]) [CC BY-SA 3.0 (Creative Commons [creativecommons.org])], vía Wikimedia Commons
Otra propiedad importante de todos los gases es su movilidad. Cada gas se dispersará para llenar todo el espacio, a menos que se lo impida una barrera sólida o líquida o una fuerza. (La fuerza de la gravedad terrestre, por ejemplo, impide que el aire escape de nuestro planeta).
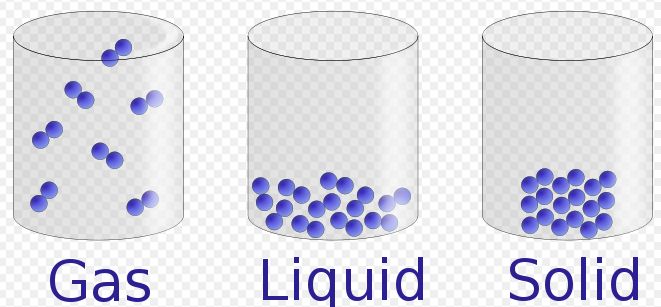
Fuente de la imagen: Por Yelod - Wikimedia Commons * Yelod - Wikipedia (En) [CC BY-SA 3.0 (Creative Commons [creativecommons.org])], vía Wikimedia Commons
Además, los gases son capaces de escapar a través de pequeños agujeros (poros) en barreras como yeso de parís o un globo, aunque el ojo humano ve tales materiales como continuos e impenetrables. La movilidad de los gases también se demuestra por la mínima resistencia que presentan a los objetos que se mueven a través de ellos. Puedes mover tu mano a través del aire mucho más fácilmente que a través de cualquier líquido.
Una tercera característica general de los gases es su amplia variación en la densidad bajo diversas condiciones. Las densidades de sólidos y líquidos cambian solo en un pequeño porcentaje cuando la temperatura o presión se duplica o reduce a la mitad. Cambios similares en las condiciones de un gas pueden alterar su densidad por un factor de 2. Esto ocurre porque el volumen de cualquier gas aumenta mucho con un aumento de la temperatura o con una reducción de la presión.
Esta tercera característica está relacionada con las capacidades de los gases para comprimirse y expandirse. La densidad variable de los gases es posible por su capacidad de cambiar de volumen. Esta propiedad de los gases los hace muy versátiles, permitiendo que los gases sean comprimidos para su almacenamiento o calentados y expandidos para impulsar un pistón (como en un motor).




