Mezcla de Orbitales para Hacer MoS
- Page ID
- 74757
Habilidades para Desarrollar
- Describir e ilustrar MO en una molécula
Los orbitales moleculares o MO son orbitales en una molécula. Recuerde que los orbitales atómicos (OA) son “nubes de probabilidad de electrones”. No podemos saber exactamente dónde está un electrón o qué camino sigue, debido al Principio de Incertidumbre, pero podemos encontrar una función matemática que nos dice cuán probables tenemos de encontrar el electrón en cada posición alrededor de un átomo. Si pensamos en electrones que se comportan como ondas, lo que hacen, la función de onda ψ nos dice la amplitud de la “onda electrónica” en cada punto alrededor del átomo. ψ 2 nos dice la probabilidad de encontrar allí el electrón. Cuando combinamos átomos para hacer moléculas, hay interferencia de ondas entre las ondas de electrones en diferentes átomos. Los electrones en una molécula ocupan orbitales moleculares, o MO, que son combinaciones de los orbitales atómicos hechos usando las reglas básicas de interferencia de ondas.
Los MO tienen las mismas propiedades básicas que tienen los orbitales atómicos. Cada MO puede contener 2 electrones con giros opuestos. ψ 2 todavía representa la probabilidad de encontrar el electrón. Cada MO tiene una energía específica, y eliminar un electrón de ese MO requiere tanta energía. Sin embargo, los MO pueden tener formas muy diferentes en comparación con los MO, y pueden extenderse sobre muchos átomos en una molécula.
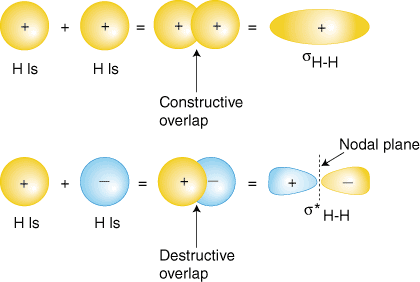
Hacemos MO de una manera similar a como hicimos orbitales híbridos. Si combinamos 2 AO (los llamamos φ A y φ B) en diferentes átomos, haremos 2 nuevos MO (llamarlos ψ 1 y ψ 2).
\[\Psi_{1} = C \left(\varphi_{A} + \varphi_{B}\right)\]
\[\Psi_{2} = C \left(\varphi_{A} - \varphi_{B}\right)\]
Haremos un MO sumando los OA y el otro restando los OA. C es una constante que “normaliza” la función de onda para que la probabilidad total de encontrar el electrón sobre todo el átomo sea 1.
Colaboradores y Atribuciones
Emily V Eames (City College of San Francisco)

