8.16.1: Biología- Cetosis
- Page ID
- 75756
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Las biomoléculas prevalentes procesadas por el cuerpo humano todos los días son carbohidratos, ácidos grasos y aminoácidos, y la ingestión de etanol en bebidas alcohólicas es, con moderación, algo inofensiva. Estos compuestos aparentemente perfectamente comestibles sufren cambios químicos en el cuerpo que producen moléculas que no son tan biológicamente amigables especialmente en grandes cantidades. La eliminación de un grupo amina de un aminoácido ayuda a la descomposición de los ácidos grasos en acetona, ácido acetoacético y ácido beta-hidroxibutírico [1]. La acetona (y las otras dos moléculas en menor medida) son miembros de la familia de las cetonas.
El etanol se oxida fácilmente a acetaldehído, uno de los aldehídos más importantes. Las cetonas y aldehídos son familias numerosas de compuestos orgánicos que tienen el grupo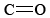 funcional, llamado grupo carbonilo.
funcional, llamado grupo carbonilo.
|
De izquierda a derecha: etanol, acetaldehído y acetona. |
Gire las estructuras jmol para ver las similitudes y diferencias entre cada modelo. Así como el etanol se oxida a acetaldehído, el metanol se oxida a formaldehído. La pérdida del átomo de hidrógeno conectado al átomo de oxígeno del metanol lo obliga a doble enlace con el átomo de carbono adyacente, creando el grupo carbonilo. Una cetona como la acetona comparte esta característica, excepto que el grupo carbonilo está unido a dos carbonos.
Ejemplo
Examina qué tipo de alcohol es el metanol y cómo se oxida a formaldehído. Usando esta información, ¿qué tipo de alcohol crees que se oxidaría para formar una cetona?
Contestar
El metanol es un alcohol primario, con su grupo hidroxilo al final de una cadena carbonada. Debido a que el grupo carbonilo de una cetona está unido a un átomo de carbono conectado a otros dos átomos de carbono, debemos deducir que los alcoholes secundarios se oxidan para producir cetonas.
Ejemplo
Utilizando lo que sabes sobre los enlaces de hidrógeno, compara cualitativamente los puntos de fusión y ebullición de aldehídos y cetonas con sus derivados de alcohol.
Contestar
Se produce un fuerte enlace de hidrógeno entre los alcoholes debido a sus grupos hidroxilo (OH). Cuando estos alcoholes se oxidan, el átomo de hidrógeno unido al átomo de oxígeno se pierde para formar el doble enlace y el grupo carbonilo. Por lo tanto, los aldehídos y cetonas tienen fuerzas intermoleculares más débiles y, por lo tanto, menores puntos de fusión y ebullición en comparación con alcoholes de tamaño similar. El grupo carbonilo es bastante polar, sin embargo, ya que la diferencia entre las electronegatividades del carbono (2.5) y el oxígeno (3.5) es bastante grande, y generalmente no hay otros dipolos en una molécula de aldehído o cetona para cancelar el efecto de C==O.
Por lo tanto, los puntos de ebullición de aldehídos y cetonas son intermedios entre los de alcanos o éteres por un lado y los alcoholes por otro. El acetaldehído, CH 3 CH 2 CHO, hierve a 20.8°C a medio camino entre propano (—42°C) y etanol (78.5°C). Los puntos de ebullición del propanal y la acetona se comparan con otros compuestos orgánicos en la tabla de los puntos de ebullición de compuestos orgánicos comparables lo que muestra la misma tendencia.
Nomenclatura y Estructura
Las terminaciones al y uno significan al dehído y ket uno, respectivamente. Los compuestos con pesos moleculares más bajos tienen nombres comunes, como el formaldehído, pero también se puede aplicar la nomenclatura estándar de la IUPAC.
Los aldehídos se nombran así como los alcoholes a partir de los cuales se oxidan, simplemente reemplazando el “ol” por “al”. Por ejemplo, el alcohol primario butanol se oxidaría a butanal. Los nombres de las cetonas dependen de dónde se encuentre el grupo carbonilo en la cadena. Al contar los átomos de carbono en la cadena principal de carbono más larga, el número del carbono incluido en el grupo carbonilo se inserta entre el nombre de la base y el sufijo “uno”. Una molécula orgánica con cinco átomos de carbono con el grupo carbonilo constituido por un átomo de oxígeno doble enlazado al tercer carbono se denominaría pentan-3-ona. Alternativamente, el dígito se puede colocar al frente, dando 3-pentanona.
La fórmula general para un aldehído es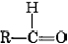 , mientras que para una cetona lo es
, mientras que para una cetona lo es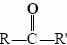 . Tenga en cuenta que cada cetona es isomérica con al menos un aldehído. La acetona, por ejemplo, tiene la misma fórmula molecular (C 3 H 6 O) que el propanal.
. Tenga en cuenta que cada cetona es isomérica con al menos un aldehído. La acetona, por ejemplo, tiene la misma fórmula molecular (C 3 H 6 O) que el propanal.
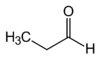
EJEMPLO Nombra las moléculas orgánicas mostradas a continuación.
a)
b)
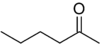
Contestar
a) Propanal
b) 2-Hexanona o Hexan-2-ona
Detección de aldehídos y cetonas
Se pueden realizar pruebas químicas para determinar la presencia de un grupo carbonilo. Inmunoquímicamente, se puede encontrar añadiendo 2,4-dinitrofenilhidrazina a tubos de ensayo que contienen 2-propanol, un alcohol, 2-propanona (acetona), una cetona; y ácido propiónico, un ácido carboxílico. La 2,4-dinitrofenilhidrazina solo reacciona con el grupo carbonilo de la 2-propanona, formando un precipitado naranja.
La reacción que se produce es:
Otra prueba puede distinguir entre aldehídos y cetonas, utilizando reactivo Tollens, que es una solución acuosa de nitrato de plata, hidróxido de sodio y un poco de amoníaco. Si se agrega un aldehído, en este caso, glucosa, a la solución, el Ag + se reduce por el aldehído, y el aldehído se oxida en un ácido carboxílico. Esto produce metal plateado, que recubre el matraz y crea el espejo. Las cetonas no se oxidan tan fácilmente, por lo que solo los aldehídos producen el espejo de plata.
La ecuación para la reacción en el video es:
Impactos Biológicos
Los aldehídos y cetonas más simples son los más importantes desde el punto de vista comercial. El formaldehído, el aldehído más simple, es uno de los conservantes biológicos más utilizados; probablemente hayas visto un frasco que contiene un órgano animal aleatorio. Mata a la mayoría de las bacterias y hongos, pero su verdadero valor radica en su tamaño. Se eligen muchos conservantes porque reaccionan con los enlaces covalentes en el tejido químico, endureciéndolo. Debido a que el formaldehído es más pequeño en comparación con otros conservantes comunes, puede penetrar la capa externa del tejido orgánico y reaccionar más fácilmente.
La velocidad de esta reacción es especialmente importante cuando el tejido se encuentra en un ambiente en el que el propio formaldehído es producido por una reacción química que no es especialmente favorecida por el producto. Por ejemplo, cuando el formaldehído está en una reacción de equilibrio con metanodiol o aminas, la constante de equilibrio no se ve favorecida hacia el formaldehído. Sin embargo, a medida que el aldehído reacciona con la materia orgánica, el equilibrio se desplaza, creando más formaldehído para reponer parcialmente el producto usado [2]. Esto es consistente con el Principio de Le Chatelier.
La acetona, la cetona más simple, es muy miscible con el agua y es común en el cuerpo. Como se mencionó anteriormente, las cetonas grandes se producen naturalmente en el hígado a través de la descomposición de los ácidos grasos. Estas moléculas perderán la mayor parte de sus grupos carbonilo en un proceso llamado descarboxilación, donde el carbonilo se separa para producir dióxido de carbono. La acetona es el producto final y se excreta a través de la respiración y la orina. Cuando el metabolismo es incapaz de eliminar rápidamente las cetonas, el cuerpo entra en un estado de cetosis. Esto suele ocurrir cuando no hay suficientes carbohidratos disponibles en el torrente sanguíneo.
¿Esta privación de carbohidratos suena familar? Cuando se induce la cetosis, el cuerpo depende más de las reservas de grasa para obtener energía. Exclusión forzada de carbohidratos de la dieta para perder - sí, esta es la dieta Atkins, químicamente dependiente de la cetosis. Si bien este proceso es normal, la exclusión de carbohidratos puede conducir a estados prolongados de cetosis que inducen la deshidratación y estresan el hígado. En casos diabéticos o alcohólicos extremos, la producción incontrolada de cetonas, especialmente ácido acetoacético y ácido beta-hidroxibutírico, conduce a la cetoacidosis. En este estado, el pH del torrente sanguíneo de una persona cae por debajo de 7.2, y en algunos casos puede ser fatal [3]. La cetoacidosis se puede identificar por la respiración de una persona; los altos niveles de acetona exhalada se pueden detectar como que tienen un aroma ligeramente afrutado, aunque algunos dicen que el olor es más como quitaesmalte.
Referencias
- ↑ Cuerpos cetónicos: una revisión de fisiología, fisiopatología y aplicación del monitoreo a la diabetes [www.ncbi.nlm.nih.gov]
- ↑ Goldstein Fixation Time Handout SFAI Fall Lecture [www.appliedimmuno.org]
- ↑ Cetoacidosis alcohólica [www.nlm.nih.gov]


