8.4: Teoría Orbital Molecular
- Page ID
- 75198
- Describir el enfoque cuántico-mecánico básico para derivar orbitales moleculares a partir de orbitales atómicos
- Describir los rasgos de orbitales moleculares ligantes y antiligantes
- Calcular órdenes de enlace basadas en configuraciones de electrones moleculares
- Escribir configuraciones de electrones moleculares para moléculas diatómicas de primera y segunda fila
- Relacionar estas configuraciones de electrones con las estabilidades y propiedades magnéticas de las moléculas
Para casi todas las moléculas covalentes que existen, ahora podemos dibujar la estructura de Lewis, predecir la geometría de pares de electrones, predecir la geometría molecular y acercarnos a predecir los ángulos de enlace. Sin embargo, una de las moléculas más importantes que conocemos, la molécula de oxígeno O 2, presenta un problema con respecto a su estructura de Lewis. Escribiríamos la siguiente estructura de Lewis para O 2:
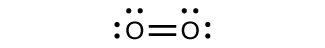
Esta estructura electrónica se adhiere a todas las reglas que rigen la teoría de Lewis. Hay un doble enlace O=O, y cada átomo de oxígeno tiene ocho electrones a su alrededor. Sin embargo, esta imagen está en desacuerdo con el comportamiento magnético del oxígeno. Por sí mismo, O 2 no es magnético, sino que se siente atraído por los campos magnéticos. Así, cuando vertimos oxígeno líquido más allá de un imán fuerte, éste se acumula entre los polos del imán y desafía la gravedad. Tal atracción hacia un campo magnético se llama paramagnetismo, y surge en moléculas que tienen electrones desapareados. Y sin embargo, la estructura Lewis de O 2 indica que todos los electrones están emparejados. ¿Cómo damos cuenta de esta discrepancia?
La susceptibilidad magnética mide la fuerza que experimenta una sustancia en un campo magnético. Cuando comparamos el peso de una muestra con el peso medido en un campo magnético (Figura\(\PageIndex{1}\)), las muestras paramagnéticas que son atraídas por el imán aparecerán más pesadas debido a la fuerza ejercida por el campo magnético. Podemos calcular el número de electrones desapareados con base en el aumento de peso.
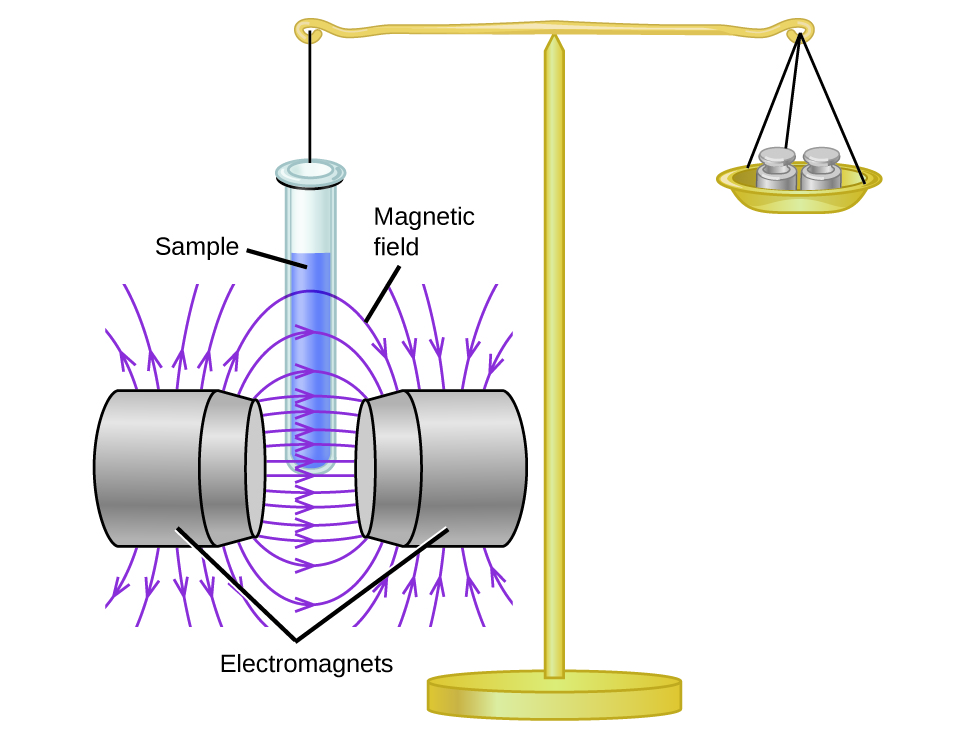
Los experimentos muestran que cada molécula de O 2 tiene dos electrones desapareados. El modelo de estructura de Lewis no predice la presencia de estos dos electrones desapareados. A diferencia del oxígeno, el peso aparente de la mayoría de las moléculas disminuye ligeramente en presencia de un campo magnético no homogéneo. Los materiales en los que todos los electrones están emparejados son diamagnéticos y repelen débilmente un campo magnético. Los materiales paramagnéticos y diamagnéticos no actúan como imanes permanentes. Sólo en presencia de un campo magnético aplicado demuestran atracción o repulsión.
La teoría orbital molecular (teoría MO) proporciona una explicación de la unión química que explica el paramagnetismo de la molécula de oxígeno. También explica la unión en una serie de otras moléculas, como violaciones de la regla del octeto y más moléculas con unión más complicada (más allá del alcance de este texto) que son difíciles de describir con estructuras de Lewis. Adicionalmente, proporciona un modelo para describir las energías de los electrones en una molécula y la probable ubicación de estos electrones. A diferencia de la teoría de los enlaces de valencia, que utiliza orbitales híbridos que se asignan a un átomo específico, la teoría MO utiliza la combinación de orbitales atómicos para producir orbitales moleculares que se deslocalizan sobre toda la molécula en lugar de localizarse en sus átomos constituyentes. La teoría MO también nos ayuda a entender por qué algunas sustancias son conductores eléctricos, otras son semiconductores y otras son aislantes. La tabla\(\PageIndex{1}\) resume los puntos principales de las dos teorías de vinculación complementaria. Ambas teorías proporcionan formas diferentes y útiles de describir la estructura molecular.
| Teoría de los bonos de valencia | Teoría Orbital Molecular |
|---|---|
| considera los enlaces localizados entre un par de átomos | considera electrones deslocalizados en toda la molécula |
| crea enlaces a partir del solapamiento de orbitales atómicos (s, p, d...) y orbitales híbridos (sp, sp 2, sp 3...) | combina orbitales atómicos para formar orbitales moleculares (σ, σ*, π, π*) |
| forma enlaces σ o π | crea interacciones ligantes y antiadherentes basadas en las cuales se llenan los orbitales |
| predice la forma molecular basada en el número de regiones de densidad electrónica | predice la disposición de los electrones en las moléculas |
| necesita múltiples estructuras para describir la resonancia |
La teoría orbital molecular describe la distribución de electrones en moléculas de la misma manera que se describe la distribución de electrones en átomos usando orbitales atómicos. Utilizando la mecánica cuántica, el comportamiento de un electrón en una molécula todavía se describe mediante una función de onda, ψ, análoga al comportamiento en un átomo. Al igual que los electrones alrededor de átomos aislados, los electrones alrededor de los átomos en las moléculas se limitan a energías discretas (cuantificadas). La región del espacio en la que es probable que se encuentre un electrón de valencia en una molécula se denomina orbital molecular (ψ 2). Al igual que un orbital atómico, un orbital molecular está lleno cuando contiene dos electrones con espín opuesto.
Consideraremos los orbitales moleculares en moléculas compuestas por dos átomos idénticos (H 2 o Cl 2, por ejemplo). Tales moléculas se llaman moléculas diatómicas homonucleares. En estas moléculas diatómicas, ocurren varios tipos de orbitales moleculares.
El proceso matemático de combinar orbitales atómicos para generar orbitales moleculares se denomina combinación lineal de orbitales atómicos (LCAO). La función de onda describe las propiedades onduladas de un electrón. Los orbitales moleculares son combinaciones de funciones de ondas orbitales atómicas. La combinación de ondas puede conducir a interferencia constructiva, en la que los picos se alinean con picos, o interferencia destructiva, en la que los picos se alinean con valles (Figura\(\PageIndex{2}\)). En los orbitales, las ondas son tridimensionales, y se combinan con ondas en fase produciendo regiones con una mayor probabilidad de densidad electrónica y ondas fuera de fase que producen nodos, o regiones sin densidad electrónica.

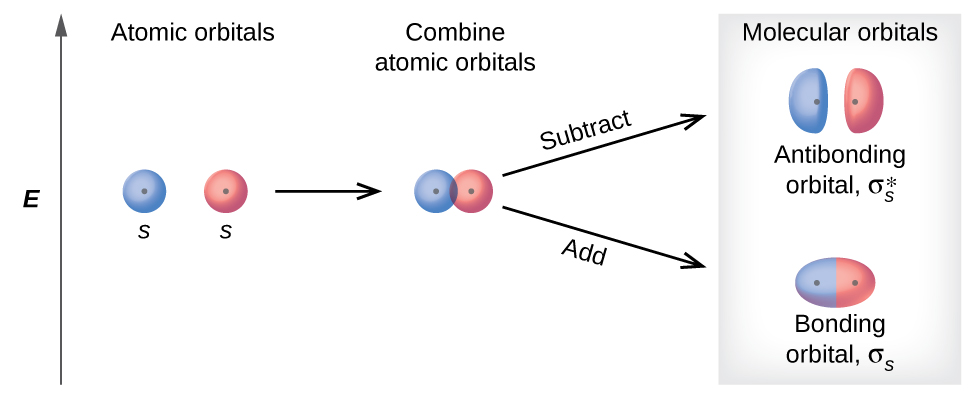
Hay dos tipos de orbitales moleculares que se pueden formar a partir de la superposición de dos orbitales atómicos en átomos adyacentes. Los dos tipos se ilustran en la Figura\(\PageIndex{3}\). La combinación en fase produce un orbital molecular σ s de menor energía (leído como “sigma-s”) en el que la mayor parte de la densidad de electrones se encuentra directamente entre los núcleos. La adición fuera de fase (que también se puede considerar como restando las funciones de onda) produce un orbital molecular de mayor energía\(σ^∗_s\) m olecular (leído como “sigma-s-estrella”) orbital molecular en el que hay un nodo entre los núcleos. El asterisco significa que el orbital es un orbital antiadherentes. Los electrones en un orbital σ s son atraídos por ambos núcleos al mismo tiempo y son más estables (de menor energía) de lo que serían en los átomos aislados. Agregar electrones a estos orbitales crea una fuerza que mantiene unidos los dos núcleos, por lo que llamamos a estos orbitales que unen orbitales. Los electrones en los\(σ^∗_s\) orbitales se encuentran muy lejos de la región entre los dos núcleos. La fuerza de atracción entre los núcleos y estos electrones separa los dos núcleos. De ahí que estos orbitales se llamen orbitales antiadherentes. Los electrones llenan el orbital de enlace de menor energía antes que el orbital antienlace de mayor energía, así como llenan orbitales atómicos de menor energía antes de llenar orbitales atómicos de mayor energía.
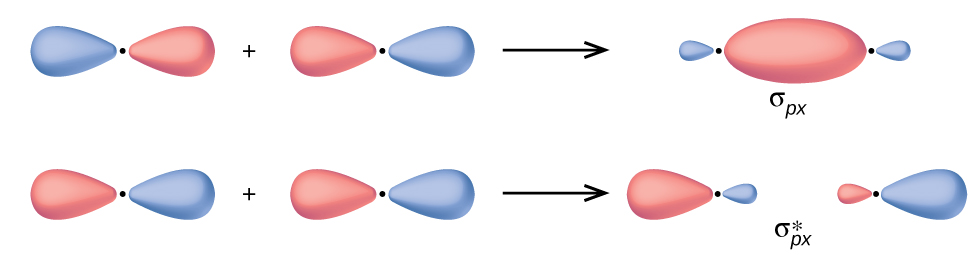
En los orbitales p, la función de onda da lugar a dos lóbulos con fases opuestas, análogas a como una onda bidimensional tiene ambas partes por encima y por debajo del promedio. Indicamos las fases sombreando los lóbulos orbitales de diferentes colores. Cuando los lóbulos orbitales de la misma fase se superponen, la interferencia de ondas constructivas aumenta la densidad de electrones. Cuando las regiones de fase opuesta se superponen, la interferencia de onda destructiva disminuye la densidad de electrones y crea nodos. Cuando los orbitales p se superponen de extremo a extremo, crean orbitales σ y σ* (Figura\(\PageIndex{4}\)). Si dos átomos están ubicados a lo largo del eje x en un sistema de coordenadas cartesianas, los dos orbitales p x se superponen de extremo a extremo y forman σ px\(σ^∗_{px}\) (enlace) y (antienlace) (leer como “sigma-p-x” y “estrella sigma-p-x”, respectivamente). Al igual que con el solapamiento s-orbital, el asterisco indica el orbital con un nodo entre los núcleos, que es un orbital antienlace de mayor energía.
The side-by-side overlap of two p orbitals gives rise to a pi (\(π\)) bonding molecular orbital and a \(π^*\) antibonding molecular orbital, as shown in Figure \(\PageIndex{5}\). In valence bond theory, we describe π bonds as containing a nodal plane containing the internuclear axis and perpendicular to the lobes of the p orbitals, with electron density on either side of the node. In molecular orbital theory, we describe the π orbital by this same shape, and a π bond exists when this orbital contains electrons. Electrons in this orbital interact with both nuclei and help hold the two atoms together, making it a bonding orbital. For the out-of-phase combination, there are two nodal planes created, one along the internuclear axis and a perpendicular one between the nuclei.
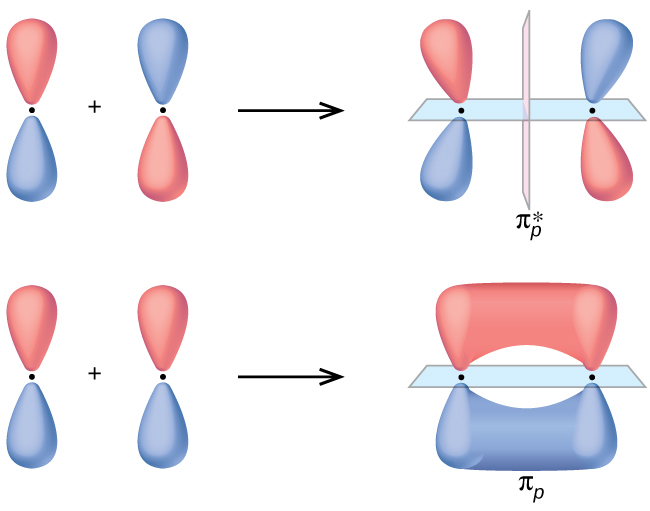
In the molecular orbitals of diatomic molecules, each atom also has two sets of p orbitals oriented side by side (py and pz), so these four atomic orbitals combine pairwise to create two π orbitals and two \(π^*\) orbitals. The \(π_{py}\) and \(π^∗_{py}\) orbitals are oriented at right angles to the \(π_{pz}\) and \(π^∗_{pz}\) orbitals. Except for their orientation, the πpy and πpz orbitals are identical and have the same energy; they are degenerate orbitals. The \(π^∗_{py}\) and \(π^∗_{pz}\) antibonding orbitals are also degenerate and identical except for their orientation. A total of six molecular orbitals results from the combination of the six atomic p orbitals in two atoms: \(σ_{px}\) and \(σ^∗_{px}\), \(π_{py}\) and \(π^∗_{py}\), \(π_{pz}\) and \(π^∗_{pz}\).
Predict what type (if any) of molecular orbital would result from adding the wave functions so each pair of orbitals shown overlap. The orbitals are all similar in energy.
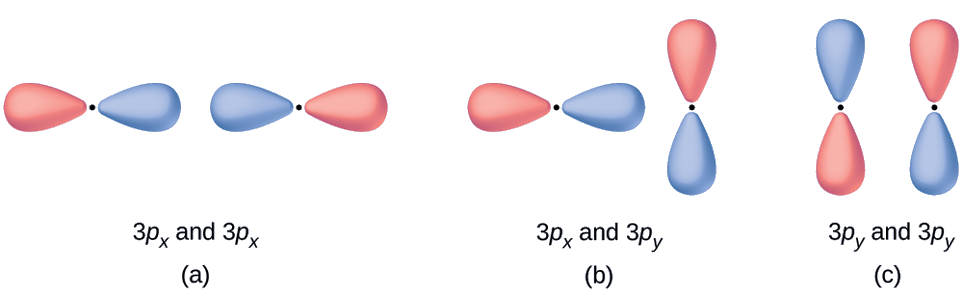
Solución
- Esta es una combinación en fase, dando como resultado un orbital σ 3 p
- Esto no dará como resultado un nuevo orbital porque el componente en fase (inferior) y el componente fuera de fase (arriba) se cancelan. Solo se pueden combinar orbitales con la alineación correcta.
- Esta es una combinación fuera de fase, resultando en un\(π^∗_{3p}\) orbital.
Marcar el orbital molecular que se muestra como\(σ\) o\(π\), enlace o antiunión e indique dónde ocurre el nodo.

- Contestar
-
El orbital se ubica a lo largo del eje internuclear, por lo que es un\(σ\) orbital. Hay un nodo que bisecciona el eje internuclear, por lo que es un orbital antiadherentes.
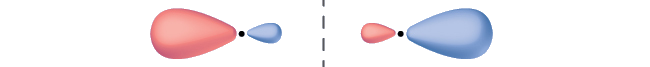
Se muestran dos orbitales acostados de extremo a extremo. Cada uno tiene uno agrandado y un lado pequeño. Los lados pequeños están enfrentados entre sí y están separados por una línea punteada vertical.
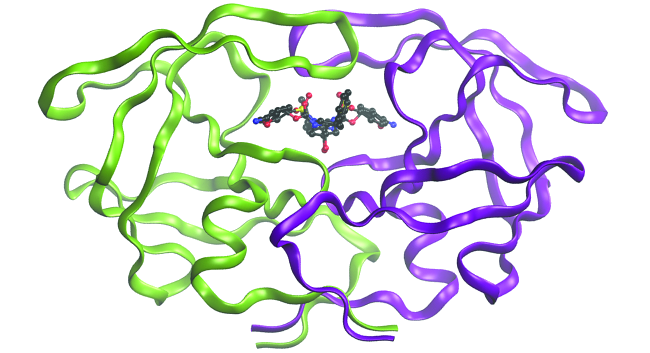
Si bien las descripciones de vinculación descritas en este capítulo involucran muchos conceptos teóricos, también tienen muchas aplicaciones prácticas en el mundo real. Por ejemplo, el diseño de medicamentos es un campo importante que utiliza nuestra comprensión de la unión química para desarrollar productos farmacéuticos. Esta área de estudio interdisciplinar utiliza la biología (entender las enfermedades y cómo operan) para identificar dianas específicas, como un sitio de unión que está involucrado en una vía de la enfermedad. Al modelar las estructuras del sitio de unión y los fármacos potenciales, los químicos computacionales pueden predecir qué estructuras pueden encajar entre sí y con qué eficacia se unirán (Figura\(\PageIndex{6}\)). Miles de candidatos potenciales pueden reducirse a algunos de los candidatos más prometedores. Estas moléculas candidatas se prueban cuidadosamente para determinar los efectos secundarios, la eficacia con la que pueden transportarse a través del cuerpo y otros factores. Decenas de importantes nuevos productos farmacéuticos han sido descubiertos con la ayuda de la química computacional, y se están llevando a cabo nuevos proyectos de investigación.
Diagramas de energía orbital molecular
Los niveles de energía relativa de los orbitales atómicos y moleculares se muestran típicamente en un diagrama orbital molecular (Figura\(\PageIndex{7}\)). Para una molécula diatómica, los orbitales atómicos de un átomo se muestran a la izquierda, y los del otro átomo se muestran a la derecha. Cada línea horizontal representa un orbital que puede contener dos electrones. Los orbitales moleculares formados por la combinación de los orbitales atómicos se muestran en el centro. Las líneas discontinuas muestran cuál de los orbitales atómicos se combinan para formar los orbitales moleculares. Por cada par de orbitales atómicos que se combinan, un orbital molecular de menor energía (enlace) y un orbital de mayor energía (antienlace) resultan orbitales. Así podemos ver que la combinación de los seis orbitales atómicos de 2 p da como resultado tres orbitales de unión (uno σ y dos π) y tres orbitales antiadherentes (uno σ* y dos π*).
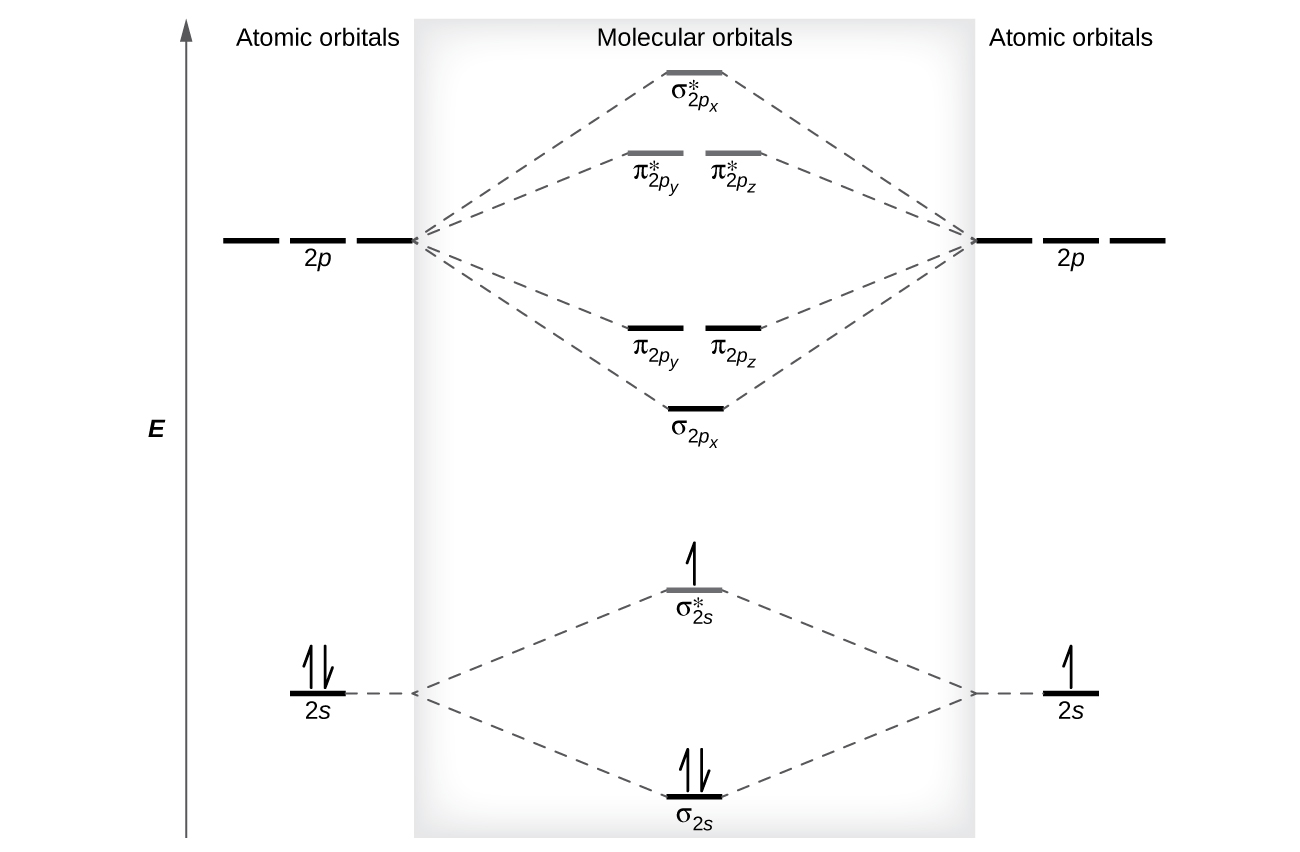
Predecimos la distribución de electrones en estos orbitales moleculares llenando los orbitales de la misma manera que llenamos los orbitales atómicos, por el principio Aufbau. Los orbitales de menor energía se llenan primero, los electrones se extienden entre orbitales degenerados antes del emparejamiento, y cada orbital puede contener un máximo de dos electrones con espines opuestos (Figura\(\PageIndex{7}\)). Así como escribimos configuraciones de electrones para átomos, podemos escribir la configuración electrónica molecular enumerando los orbitales con superíndices que indican el número de electrones presentes. Para mayor claridad, colocamos paréntesis alrededor de orbitales moleculares con la misma energía. En este caso, cada orbital está a una energía diferente, por lo que los paréntesis separan cada orbital. Por lo tanto, esperaríamos que una molécula diatómica o ion que contenga siete electrones (como\(\ce{Be2+}\)) tendría la configuración de electrones moleculares\((σ_{1s})^2(σ^∗_{1s})^2(σ_{2s})^2(σ^∗_{2s})^1\). Es común omitir los electrones centrales de diagramas y configuraciones orbitales moleculares e incluir solo los electrones de valencia.
Orden de Bonos
El diagrama orbital molecular relleno muestra el número de electrones tanto en orbitales moleculares enlazantes como antiadherentes. La contribución neta de los electrones a la fuerza de enlace de una molécula se identifica determinando el orden de enlace que resulta del llenado de los orbitales moleculares por electrones.
Al usar estructuras de Lewis para describir la distribución de electrones en moléculas, definimos el orden de enlace como el número de pares de enlaces de electrones entre dos átomos. Así, un enlace sencillo tiene un orden de enlace de 1, un doble enlace tiene un orden de enlace de 2 y un triple enlace tiene un orden de enlace de 3. Definimos el orden de enlace de manera diferente cuando usamos la descripción orbital molecular de la distribución de electrones, pero el orden de enlace resultante suele ser el mismo. La técnica MO es más precisa y puede manejar casos en los que falla el método de la estructura de Lewis, pero ambos métodos describen el mismo fenómeno.
En el modelo orbital molecular, un electrón contribuye a una interacción de enlace si ocupa un orbital de enlace y contribuye a una interacción antiunión si ocupa un orbital antienlace. El orden de los enlaces se calcula restando los electrones desestabilizantes (antiadherentes) de los electrones estabilizadores (enlaces). Dado que un enlace consiste en dos electrones, dividimos por dos para obtener el orden de enlace. Podemos determinar el orden de los bonos con la siguiente ecuación:
\[\textrm{bond order}=\dfrac{(\textrm{number of bonding electrons})−(\textrm{number of antibonding electrons})}{2} \nonumber \]
El orden de un enlace covalente es una guía para su fuerza; un enlace entre dos átomos dados se vuelve más fuerte a medida que aumenta el orden de enlace. Si la distribución de electrones en los orbitales moleculares entre dos átomos es tal que el enlace resultante tendría un orden de enlace de cero, no se forma un enlace estable. A continuación analizamos algunos ejemplos específicos de diagramas MO y órdenes de bonos.
Unión en Moléculas Diatómicas
Una molécula de dihidrógeno (H 2) se forma a partir de dos átomos de hidrógeno. Cuando los orbitales atómicos de los dos átomos se combinan, los electrones ocupan el orbital molecular de menor energía, el orbital de unión σ 1 s. Una molécula de dihidrógeno, H 2, se forma fácilmente porque la energía de una molécula H 2 es menor que la de dos átomos de H. El orbital σ 1 s que contiene ambos electrones es menor en energía que cualquiera de los dos orbitales atómicos de 1 s.
Un orbital molecular puede contener dos electrones, por lo que ambos electrones en la molécula H 2 están en el orbital de unión σ 1 s; la configuración electrónica es\((σ_{1s})^2\). Representamos esta configuración mediante un diagrama de energía orbital molecular (Figura\(\PageIndex{8}\)) en el que una sola flecha hacia arriba indica un electrón en un orbital, y dos flechas (hacia arriba y hacia abajo) indican dos electrones de espín opuesto.
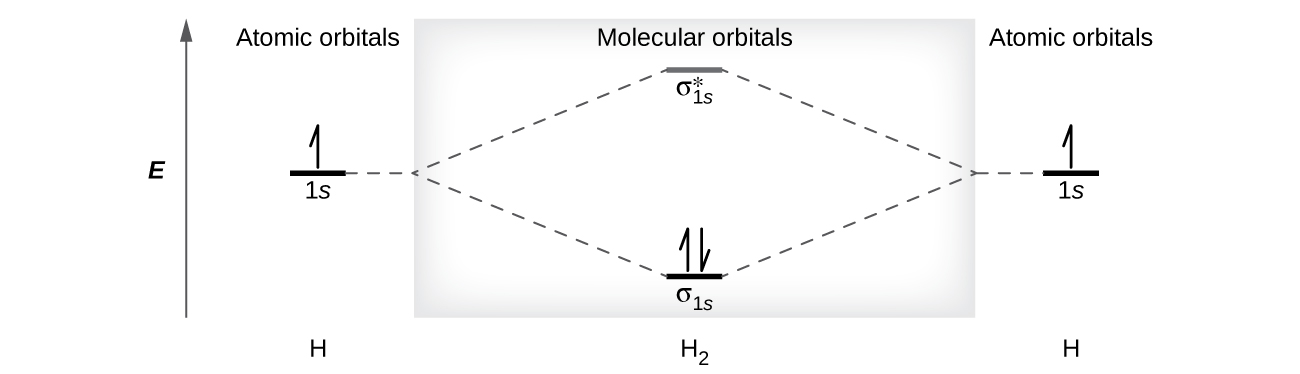
Una molécula de dihidrógeno contiene dos electrones de enlace y no hay electrones antienlace, por lo que tenemos
\[\ce{bond\: order\: in\: H2}=\dfrac{(2−0)}{2}=1 \nonumber \]
Debido a que el orden de enlace para el enlace H—H es igual a 1, el enlace es un enlace sencillo.
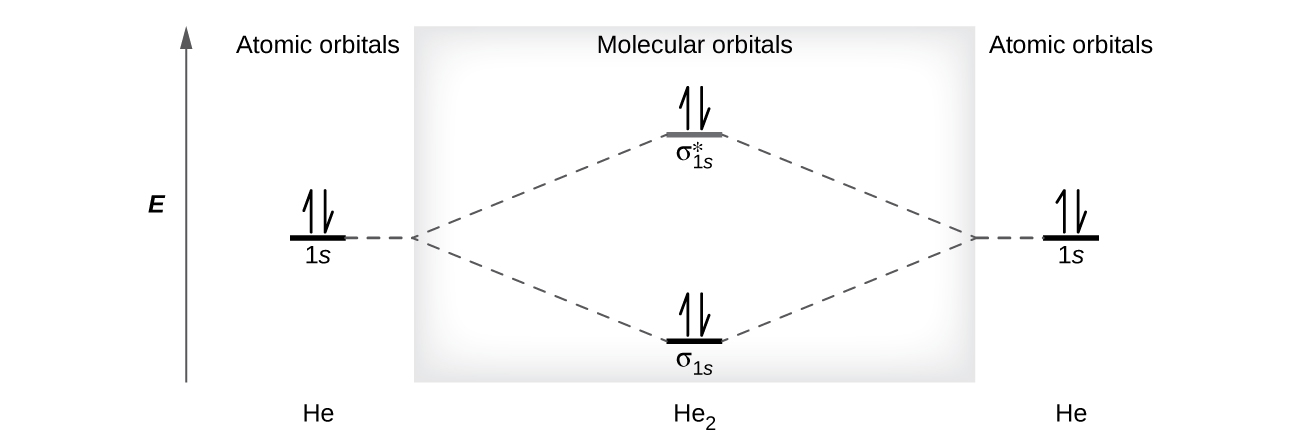
Un átomo de helio tiene dos electrones, ambos de los cuales están en su orbital de 1 s. Dos átomos de helio no se combinan para formar una molécula de dihelio, He 2, con cuatro electrones, debido a que el efecto estabilizador de los dos electrones en el orbital de enlace de menor energía sería compensado por el efecto desestabilizador de los dos electrones en el orbital molecular antienlace de mayor energía. Escribiríamos la hipotética configuración electrónica de He 2\((σ_{1s})^2(σ^∗_{1s})^2\) como en la Figura\(\PageIndex{9}\). El cambio neto de energía sería cero, por lo que no hay fuerza impulsora para que los átomos de helio formen la molécula diatómica. De hecho, el helio existe como átomos discretos más que como moléculas diatómicas. El orden de enlace en una molécula hipotética de dihelio sería cero.
\[\ce{bond\: order\: in\: He2}=\dfrac{(2−2)}{2}=0 \nonumber \]
Un orden de enlace de cero indica que no se forma ningún enlace entre dos átomos.
Las moléculas diatómicas del segundo periodo
Ocho posibles moléculas diatómicas homonucleares podrían estar formadas por los átomos del segundo periodo de la tabla periódica: Li 2, Be 2, B 2, C 2, N 2, O 2, F 2 y Ne 2. Sin embargo, podemos predecir que la molécula Be 2 y la molécula Ne 2 no serían estables. Esto lo podemos ver por una consideración de las configuraciones de electrones moleculares (Cuadro\(\PageIndex{1}\)).
| Molécula | Configuración de electrones | Orden de Bonos |
|---|---|---|
| Li 2 | \((σ_{2s})^2\) | 1 |
| Ser 2 (inestable) | \((σ_{2s})^2(σ^∗_{2s})^2\) | 0 |
| B 2 | \((σ_{2s})^2(σ^∗_{2s})^2(π_{2py},\:π_{2pz})^2\) | 1 |
| C 2 | \((σ_{2s})^2(σ^∗_{2s})^2(π_{2py},\:π_{2pz})^4\) | 2 |
| N 2 | \((σ_{2s})^2(σ^∗_{2s})^2(π_{2py},\:π_{2pz})^4(σ_{2px})^2\) | 3 |
| O 2 | \((σ_{2s})^2(σ^∗_{2s})^2(σ_{2px})^2(π_{2py},\:π_{2pz})^4(π^∗_{2py},π^∗_{2pz})^2\) | 2 |
| F 2 | \((σ_{2s})^2(σ^∗_{2s})^2(σ_{2px})^2(π_{2py},\:π_{2pz})^4(π^∗_{2py},\:π^∗_{2pz})^4\) | 1 |
| Ne 2 (inestable) | \((σ_{2s})^2(σ^∗_{2s})^2(σ_{2px})^2(π_{2py},\:π_{2pz})^4(π^∗_{2py},π^∗_{2pz})^4(σ^∗_{2px})^2\) | 0 |
Predecimos configuraciones de electrones orbitales moleculares de valencia del mismo modo que predecimos configuraciones de electrones de átomos. Los electrones de valencia se asignan a orbitales moleculares de valencia con las energías más bajas posibles. Consistente con la regla de Hund, siempre que haya dos o más orbitales moleculares degenerados, los electrones llenan cada orbital de ese tipo individualmente antes de que se produzca cualquier emparejamiento de electrones.
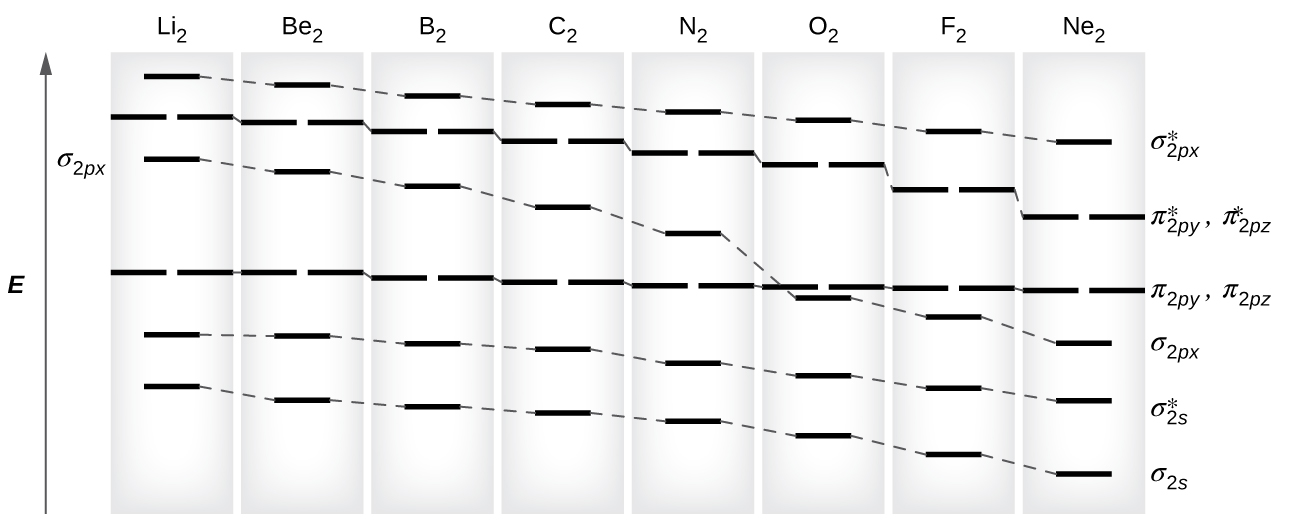
Como vimos en la teoría de los enlaces de valencia, los enlaces σ son generalmente más estables que los enlaces π formados a partir de orbitales atómicos degenerados. De manera similar, en la teoría de orbitales moleculares, los orbitales σ suelen ser más estables que los orbitales π. No obstante, no siempre es así. Los MO para los orbitales de valencia del segundo periodo se muestran en la Figura\(\PageIndex{10}\). Al observar los orbitales moleculares de Ne 2, vemos que el orden es consistente con el diagrama genérico mostrado en la sección anterior. Sin embargo, para los átomos con tres o menos electrones en los orbitales p (Li a N) observamos un patrón diferente, en el que el orbital σ p es mayor en energía que el conjunto π p. Obtener el diagrama orbital molecular para un ion diatómico homonuclear sumando o restando electrones del diagrama para la molécula neutra.
Este cambio en el orden orbital ocurre debido a un fenómeno llamado mezcla s-p. La mezcla s-p no crea nuevos orbitales; simplemente influye en las energías de los orbitales moleculares existentes. La función de onda σ s se combina matemáticamente con la función de onda σ p, con el resultado de que el orbital σ s se vuelve más estable y el orbital σ p se vuelve menos estable (Figura\(\PageIndex{11}\)). De manera similar, los orbitales antiadhesión también experimentan mezcla s-p, con los σ s * volviéndose más estables y los σ p * volviéndose menos estables.
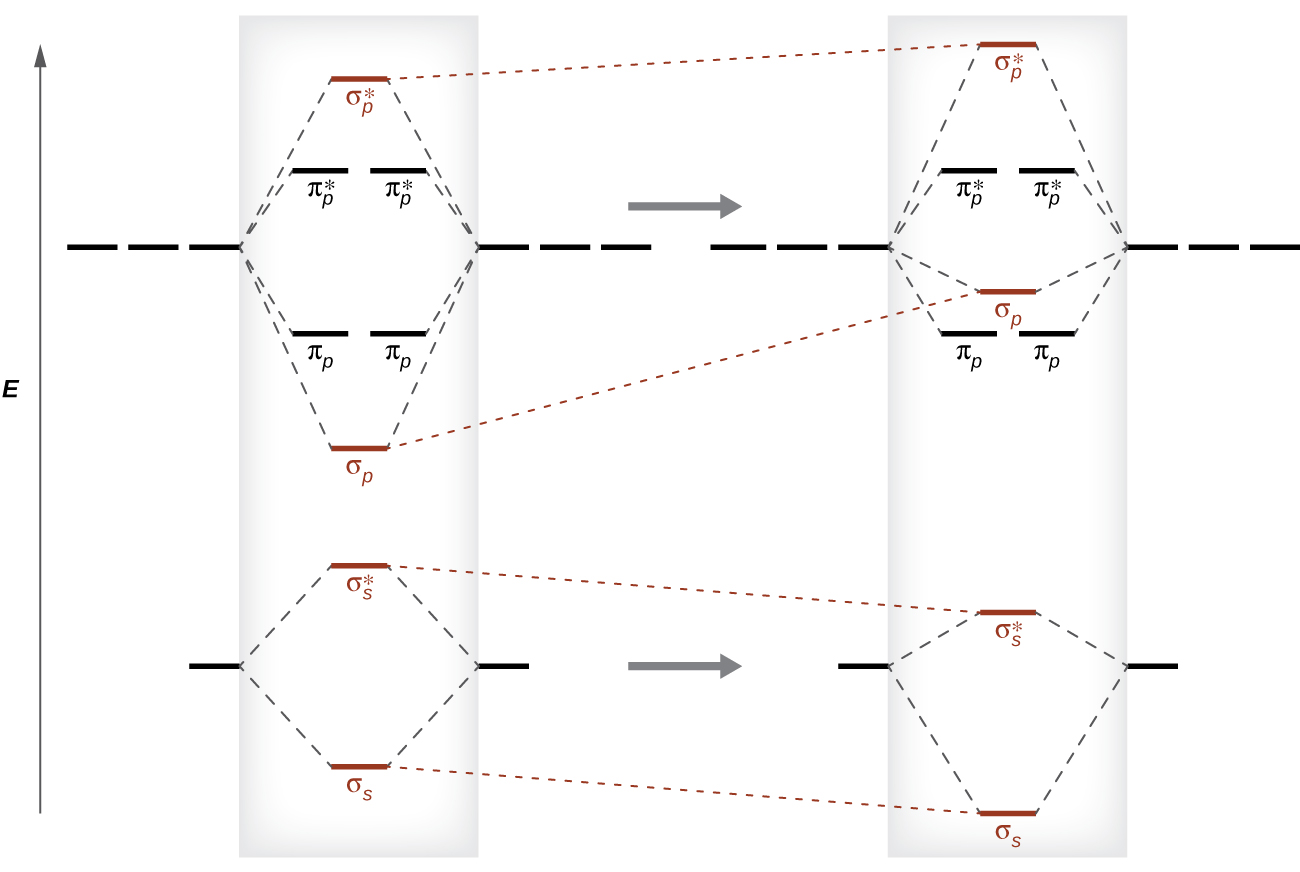
La mezcla de s-p ocurre cuando los orbitales s y p tienen energías similares. La diferencia de energía entre los orbitales de 2 s y 2 p en O, F y Ne es mayor que la de Li, Be, B, C y N. Debido a esto, O 2, F 2 y Ne presentan una mezcla s-p insignificante (no suficiente para cambiar el orden de energía), y sus diagramas MO siguen los patrón normal, como se muestra en la Figura\(\PageIndex{7}\). Todas las demás moléculas diatómicas del período 2 sí tienen mezcla s-p, lo que lleva al patrón donde el orbital σ p se eleva por encima del conjunto π p.
Usando los diagramas MO mostrados en la Figura\(\PageIndex{11}\), podemos agregar los electrones y determinar la configuración de electrones moleculares y el orden de enlace para cada una de las moléculas diatómicas. Como se muestra en la Tabla\(\PageIndex{1}\), las moléculas Be 2 y Ne 2 tendrían un orden de enlace de 0, y estas moléculas no existen.
La combinación de dos átomos de litio para formar una molécula de litio, Li 2, es análoga a la formación de H 2, pero los orbitales atómicos involucrados son los orbitales de valencia 2 s. Cada uno de los dos átomos de litio tiene un electrón de valencia. Por lo tanto, tenemos dos electrones de valencia disponibles para el orbital molecular de enlace σ 2 s. Debido a que ambos electrones de valencia estarían en un orbital de unión, predeciríamos que la molécula Li 2 sería estable. La molécula está, de hecho, presente en una concentración apreciable en vapor de litio a temperaturas cercanas al punto de ebullición del elemento. También se conocen todas las demás moléculas de la Tabla\(\PageIndex{1}\) con un orden de enlace mayor a cero.
La molécula O 2 tiene suficientes electrones para llenar a la mitad el\((π^∗_{2py},\:π^∗_{2pz})\) nivel. Esperamos que los dos electrones que ocupan estos dos orbitales degenerados estén desapareados, y esta configuración electrónica molecular para O 2 está de acuerdo con el hecho de que la molécula de oxígeno tiene dos electrones desapareados (Figura\(\PageIndex{10}\)). La presencia de dos electrones desapareados ha demostrado ser difícil de explicar usando estructuras de Lewis, pero la teoría orbital molecular lo explica bastante bien. De hecho, los electrones desapareados de la molécula de oxígeno proporcionan una fuerte pieza de apoyo para la teoría orbital molecular.
Cuando se combinan dos orbitales atómicos idénticos en diferentes átomos, resultan dos orbitales moleculares (por ejemplo,\(H_2\) en la Figura\(\PageIndex{8}\)). El orbital de enlace es menor en energía que los orbitales atómicos originales porque los orbitales atómicos están en fase en el orbital molecular. El orbital antiadhesión es mayor en energía que los orbitales atómicos originales porque los orbitales atómicos están desfasados.
En un sólido, suceden cosas similares, pero a una escala mucho mayor. Recuerde que incluso en una pequeña muestra hay una gran cantidad de átomos (típicamente > 10 23 átomos), y por lo tanto una gran cantidad de orbitales atómicos que pueden combinarse en orbitales moleculares. Cuando se combinan N orbitales atómicos de valencia, todos de la misma energía y cada uno conteniendo un (1) electrón, resultarán orbitales de unión N /2 (rellenos) y orbitales antiunión N /2 (vacíos). Cada orbital de unión mostrará una disminución de energía ya que los orbitales atómicos están en su mayoría en fase, pero cada uno de los orbitales de unión será un poco diferente y tendrá energías ligeramente diferentes. Los orbitales antiadhesión mostrarán un incremento en la energía ya que los orbitales atómicos están en su mayoría fuera de fase, pero cada uno de los orbitales antiadhesión también será un poco diferente y tendrá energías ligeramente diferentes. Los niveles de energía permitidos para todos los orbitales de unión son tan cercanos entre sí que forman una banda, llamada banda de valencia. De igual manera, todos los orbitales antiadherentes están muy unidos entre sí y forman una banda, llamada banda de conducción. Figura\(\PageIndex{12}\)) muestra las bandas para tres clases importantes de materiales: aisladores, semiconductores y conductores.
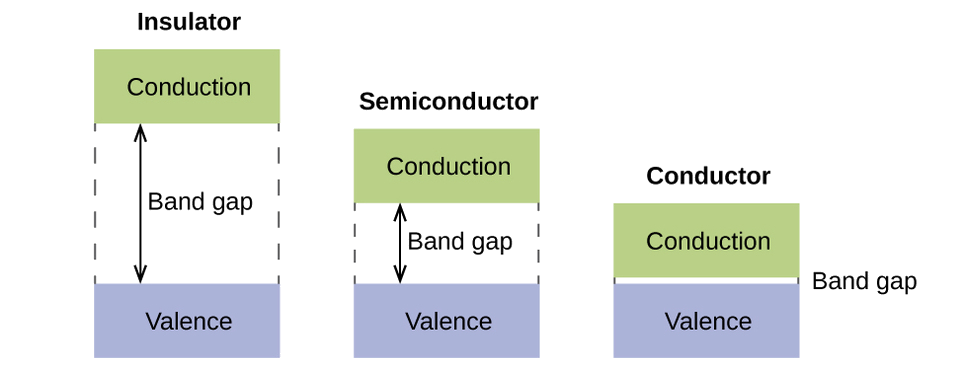
Para conducir la electricidad, los electrones deben moverse de la banda de valencia llena a la banda de conducción vacía donde pueden moverse por todo el sólido. El tamaño de la banda prohibida, o la diferencia de energía entre la parte superior de la banda de valencia y la parte inferior de la banda de conducción, determina lo fácil que es mover electrones entre las bandas. Solo se requiere una pequeña cantidad de energía en un conductor porque el espacio de banda es muy pequeño. Esta pequeña diferencia energética es “fácil” de superar, por lo que son buenos conductores de electricidad. En un aislador, la banda prohibida es tan “grande” que muy pocos electrones se mueven hacia la banda de conducción; como resultado, los aisladores son conductores pobres de la electricidad. Los semiconductores conducen electricidad cuando se proporcionan cantidades “moderadas” de energía para mover electrones fuera de la banda de valencia y entrar en la banda de conducción. Los semiconductores, como el silicio, se encuentran en muchos componentes electrónicos.
Los semiconductores se utilizan en dispositivos como computadoras, teléfonos inteligentes y células solares. Las células solares producen electricidad cuando la luz proporciona la energía para mover los electrones fuera de la banda de valencia. La electricidad que se genera puede entonces ser utilizada para alimentar una luz o herramienta, o puede almacenarse para su uso posterior cargando una batería. A diciembre de 2014, hasta 46% de la energía de la luz solar podría convertirse en electricidad utilizando células solares.
Dibujar el diagrama orbital molecular para la molécula de oxígeno, O 2. A partir de este diagrama, calcule el orden de fianza para O 2. ¿Cómo explica este diagrama el paramagnetismo de O 2?
Solución
Dibujamos un diagrama de energía orbital molecular similar al que se muestra en la Figura\(\PageIndex{7}\). Cada átomo de oxígeno aporta seis electrones, por lo que el diagrama aparece como se muestra en la Figura\(\PageIndex{7}\).
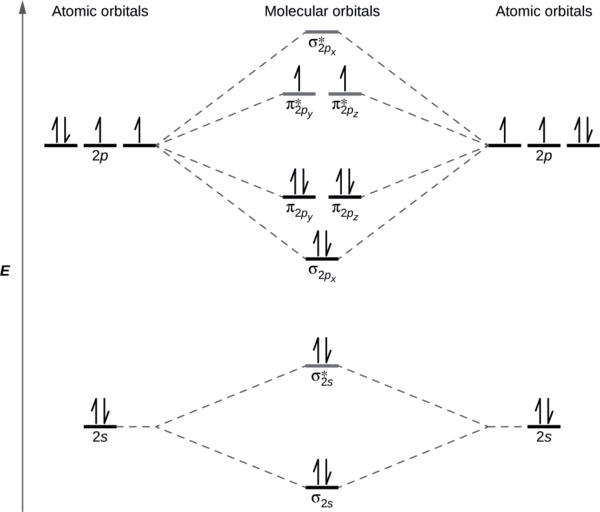
Calculamos la orden de fianza como
\[\ce{O2}=\dfrac{(8−4)}{2}=2 \nonumber \]
El paramagnetismo del oxígeno se explica por la presencia de dos electrones desapareados en los orbitales moleculares (π 2 py, π 2 pz) *.
El componente principal del aire es N 2. A partir del diagrama orbital molecular de N 2, predecir su orden de enlace y si es diamagnético o paramagnético.
- Contestar
-
N 2 tiene un orden de enlace de 3 y es diamagnético.
Dar la configuración orbital molecular para los electrones de valencia en\(\ce{C2^2-}\). ¿Estará estable este ion?
Solución
Al observar el diagrama MO apropiado, vemos que los orbitales π son más bajos en energía que el orbital σ p. La configuración de electrones de valencia para C 2 es
\((σ_{2s})^2(σ^∗_{2s})^2(π_{2py},\:π_{2pz})^4\).
Agregar dos electrones más para generar el\(\ce{C2^2-}\) anión dará una configuración de electrones de valencia de
\((σ_{2s})^2(σ^∗_{2s})^2(π_{2py},\:π_{2pz})^4(σ_{2px})^2\)
Dado que esto tiene seis electrones de unión más que antiadherentes, el orden de enlace será 3, y el ion debe ser estable.
¿Cuántos electrones desapareados estarían presentes en un\(\ce{Be2^2-}\) ion? ¿Sería paramagnético o diamagnético?
- Contestar
-
dos, paramagnético
Conceptos clave y resumen
La teoría orbital molecular (MO) describe el comportamiento de los electrones en una molécula en términos de combinaciones de las funciones de onda atómica. Los orbitales moleculares resultantes pueden extenderse sobre todos los átomos de la molécula. Los orbitales moleculares de unión están formados por combinaciones en fase de funciones de ondas atómicas, y los electrones en estos orbitales estabilizan una molécula. Los orbitales moleculares antiadherentes resultan de combinaciones desfasadas de funciones de onda atómica y electrones en estos orbitales hacen que una molécula sea menos estable. Los orbitales moleculares ubicados a lo largo de un eje internuclear se denominan σ MO. Se pueden formar a partir de orbitales s o de orbitales p orientados de extremo a extremo. Los orbitales moleculares formados a partir de orbitales p orientados lado a lado tienen densidad de electrones en lados opuestos del eje internuclear y se denominan orbitales π.
Podemos describir la estructura electrónica de las moléculas diatómicas aplicando la teoría orbital molecular a los electrones de valencia de los átomos. Los electrones llenan orbitales moleculares siguiendo las mismas reglas que se aplican al llenado de orbitales atómicos; la regla de Hund y el principio de Aufbau nos dicen que los orbitales de menor energía se llenarán primero, los electrones se extenderán antes de que se emparejen, y cada orbital puede contener un máximo de dos electrones con espines opuestos. Los materiales con electrones desapareados son paramagnéticos y atraídos por un campo magnético, mientras que aquellos con electrones totalmente emparejados son diamagnéticos y repelidos por un campo magnético. La predicción correcta de las propiedades magnéticas de las moléculas es una ventaja de la teoría orbital molecular sobre las estructuras de Lewis y la teoría de enlaces de valencia.


