6.10: Fragmentación - Cationes Estables
- Page ID
- 79129
Cuando las moléculas pasan por un espectrómetro de masas, algunas de ellas llegan intactas al detector, pero muchas de ellas se rompen en pedazos de diversas maneras diferentes. Para establecer una carga en una molécula, se tuvo que eliminar un electrón; la eliminación de ese electrón se efectúa a través de una colisión, generalmente con un electrón de alta energía. Durante esa colisión, la energía se transfiere del electrón de alta energía a la molécula, y esa energía tiene que ir a alguna parte. Parte de ella se divide en varias vibraciones de unión, por lo que las uniones comienzan a vibrar bastante, hasta que algunas de ellas se rompen por completo. El ion molecular se rompe y forma un ion fragmento.
Algunos iones fragmentos son muy comunes en la espectrometría de masas. Estos iones se ven frecuentemente por cualquiera de dos razones:
- no hay una vía disponible para descomponer el ion.
- el ion es relativamente estable, por lo que se forma fácilmente.
Las fragmentaciones ocurren a través de vías o mecanismos bien definidos. Un mecanismo es una serie paso a paso de eventos que ocurren en una reacción. Es importante entender cómo ocurren las reacciones, pero veremos las fragmentaciones cuando estudiemos las reacciones radicales.
Sin embargo, es útil saber qué factores hacen que los cationes sean estables.
Algunos iones comunes
Hay una serie de iones comúnmente vistos en la espectrometría de masas que te dicen un poco sobre la estructura. Al igual que con los aniones, hay un par de factores comunes que influyen en la estabilidad catiónica:
- La electronegatividad juega un papel. Los átomos más electronegativos tienen menos probabilidades de ser cationes.
- La polarizabilidad también juega un papel importante. Los átomos más polarizables tienen más probabilidades de ser cationes.
Sin embargo, en la mayoría de los casos, estaremos viendo el carbono con una carga positiva, y hay factores adicionales para distinguirlos
- La deslocalización estabiliza un catión extendiendo la carga en dos o más átomos diferentes.
- En términos de estructura de Lewis, la forma más fácil de deslocalizar la carga es vía resonancia.
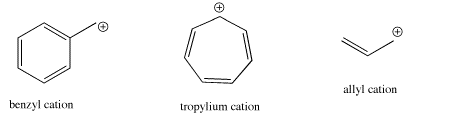
- La resonancia puede involucrar otros carbonos, como en los cationes alilo y bencilo.
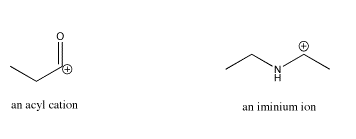
- La resonancia también puede involucrar otros átomos, como en los cationes acilio o iminio.
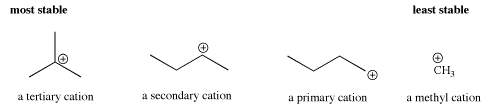
- La deslocalización también se puede lograr a través de efectos inductivos. La tendencia en los carbocationes es que cuantos más sustituyentes tengan los carbocationes, mayor será la estabilidad.
- Los cationes terciarios, con tres sustituyentes en el carbocatión, son más estables que los cationes secundarios, con dos sustituyentes en el carbocatión. Los cationes secundarios son más estables que los primarios. Los cationes primarios son más estables que los cationes metilo.
Los cálculos orbitales moleculares sugieren que el catión se estabiliza a través de la interacción con enlaces C-H vecinos en los grupos alquilo. Específicamente, un orbital de unión sigma C-H tiene simetría similar a la orbital p vacía sobre el carbono positivo. Los lóbulos de los dos orbitales pueden superponerse de tal manera que están en fase, y eso permite que los electrones sean donados del enlace C-H al carbono central deficiente en electrones. Formalmente, existe una interacción de vinculación y una interacción antiadhesión entre estos dos orbitales. Dado que uno de estos orbitales está vacío, la combinación antiadhesión permanece desocupada. La combinación de unión está poblada, sin embargo, y dado que es menor en energía que el enlace orbital p o el enlace sigma C-H (todas las combinaciones de unión son menores en energía que los orbitales que se combinan para formarlos), hay una disminución neta de energía.
Dibuja tantas estructuras de resonancia como puedas que ayuden a explicar la estabilidad de los siguientes cationes:
- catión alilo
- catión bencílico
- catión tropilio
- un ion acilio
- un ión iminio
- Responder
-
Agrega textos aquí. No elimine primero este texto.

