6.6: Principio de Aufbau, Relleno de Electrones, Notación de Caja y Espectroscopia de Fotoelectrones
- Page ID
- 79863
Principio de Aufbau
Los números cuánticos son una manera práctica de dar cuenta de los electrones que llenan las conchas atómicas, pero puede ser complicado hacer un seguimiento de ellos. En cambio, a menudo utilizamos taquigrafía para etiquetar los números cuánticos:
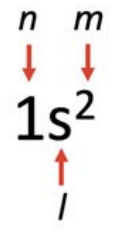
El principio de Aufbau es un truco para hacer un seguimiento del orden en que se rellena cada subshell:
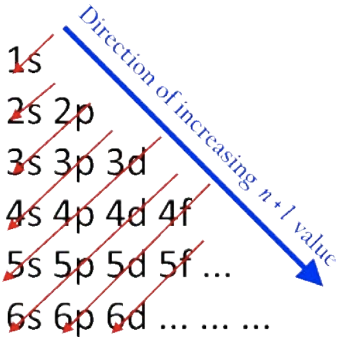
El superíndice después de cada subcapa indica el número de electrones en la subcapa: cada uno debe estar lleno excepto el caparazón más exterior, que se llena en función del número de electrones de valencia.
Ejemplo: Anote tanto la configuración electrónica completa como la notación de gas noble de\(\mathrm{Br}\).
\(\mathrm{Br}\)tiene 35 electrones de valencia, por lo que podemos llenar todo el camino hasta el Argón. La configuración completa, que sigue principalmente a Aufbau, es
\(1 \mathrm{~s}^2 2 \mathrm{~s}^2 2 \mathrm{p}^6 3 \mathrm{~s}^2 3 \mathrm{p}^6 3 \mathrm{~d}^{10} 4 \mathrm{~s}^2 4 \mathrm{p}^5\)
Tenga en cuenta aquí que el\(3 \mathrm{~d}^{10}\) y\(4 \mathrm{~s}^2\) ocurren en un orden inesperado: hay algunas excepciones al principio de Aufbau. No esperamos que memorice estas excepciones para\(3.091\), ¡pero sepa que están anotadas en la tabla periódica! La configuración del gas noble solo muestra los electrones más allá de la última capa completa:
\([\mathrm{Ar}] 3 \mathrm{~d}^{10} 4 \mathrm{~s}^2 4 \mathrm{p}^5\)
Relleno de electrones y notación de caja
Podemos observar la configuración y orientación de los electrones visualmente usando notación de caja. Por lo general, es más fácil usar el principio Aufbau (¡o la tabla periódica!) para anotar la configuración electrónica y luego traducirla a notación de caja. Es importante recordar la regla de Hund: cada órbita en una subconcha debe estar ocupada individualmente antes de que cualquier orbital esté doblemente ocupada.
Ejemplo: Dibujar la configuración electrónica de\(\mathrm{Br}\) y\(\mathrm{C}\) en notación de caja.
- Contestar
-
Escribimos la configuración de gas noble arriba, así que podemos simplemente dar la notación de caja de los electrones de valencia aquí:
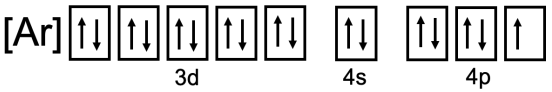
Para el carbono, la configuración electrónica es\(1 \mathrm{~s}^2 2 \mathrm{~s}^2 2 \mathrm{p}^2\). En notación de caja, llenamos\(2 \mathrm{~s}\) los estados\(1 \mathrm{~s}\) y, y poblamos el\(2 \mathrm{p}\) según la regla de Hund:
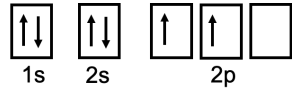
Espectroscopia fotoelectrónica (PES)
La espectroscopia fotoelectrónica (PES) es un método experimental utilizado para determinar la estructura electrónica. Primero, una muestra es bombardeada con fotones de alta energía para ionizar los átomos. Entonces, se mide la energía cinética de los electrones que se emiten. La energía de unión se puede determinar usando
\(E_{b i n d i n g}=h \nu-K E_{e-}\)
Al trazar los recuentos relativos de electrones emitidos con diversas energías de unión, la composición elemental de una muestra se puede determinar usando PES!
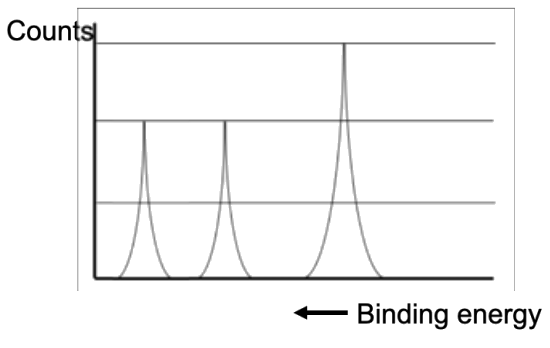
Ejemplo: Determine qué elemento corresponde al siguiente espectro PES:
- Contestar
-
En esta trama, la energía de unión aumenta hacia la izquierda. Los electrones más cercanos al núcleo deben tener la energía de unión más alta, por lo que el pico más a la izquierda debe corresponder a\(1 \mathrm{~s}\) los electrones. La altura relativa del pico corresponde a la frecuencia relativa a la que se emiten los electrones: dado que hay dos electrones 1s, la altura del pico más a la izquierda debe corresponder a dos electrones. El pico medio debe corresponder a dos\(2 \mathrm{~s}\) electrones. Entonces, dado que el pico más a la derecha es\(1.5\) veces más alto, debe representar 3 electrones en la\(2 \mathrm{p}\) subcapa. La configuración electrónica para el elemento en este diagrama PES debe ser\(1 \mathrm{~s}^2 2 \mathrm{~s}^2 2 \mathrm{p}^3\), que corresponde al nitrógeno.

