5.1: Compuestos organometálicos de Zinc y Cadmio
- Page ID
- 69126
Objetivos de aprendizaje
En esta sección aprenderás lo siguiente
- Compuestos organometálicos de zinc y cadmio.
- Características estructurales de los compuestos de organozinc
Compuestos organometálicos de zinc y cadmio
Los compuestos dialquilo de Zn, Cd y Hg no se asocian a través de puentes alquílicos.
Los compuestos de dialquilzinc son solo ácidos de Lewis débiles, los compuestos de organocadmio son aún más débiles y los compuestos organoméricos no actúan como ácidos de Lewis excepto en circunstancias especiales.
Los metales del Grupo 12 forman compuestos moleculares lineales, como ZnMe 2, CdMe 2 y HgMe 2, que no están asociados en estado sólido, líquido o gaseoso o en solución hidrocarbonada.
Forman enlaces 2c, 2e. A diferencia de los análogos Be y Mg, no completan sus conchas de valencia por asociación a través de puentes alquílicos. Los enlaces en estas moléculas son similares a los metales d 10 como Cu I, Ag I y Au I con geometría lineal ([N=C-M-C=N] -, M = Ag o Au). Esta tendencia a veces se racionaliza invocando hibridación pd en el ion M +, lo que conduce a orbitales que favorecen la unión lineal de ligandos (similar a la hibridación spd).
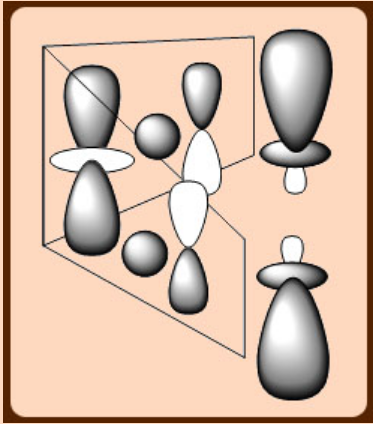
La preferencia por la coordinación lineal puede deberse a la similitud en energía de los orbitales externos n s, n p y (n-1) d, lo que permite la formación de híbridos colineales spd.
La hibridación de s, p z y d z 2 con la elección de fases aquí mostradas produce un par de orbitales colineales que pueden ser utilizados para formar enlaces σfuertes.
Compuestos organozincados y organocadmios
La vía conveniente es la metátesis con compuestos de alquilaluminio o alquillitio.
Con los compuestos de alquillitio es la electronegatividad la que es decisiva, mientras que entre Al y Zn es que las consideraciones de dureza predicen correctamente la formación de pares ZnCh 3 más blandos y AlCl más duros.
\[\ce{ZnCl2 + Al2Me6 -> ZnMe2 + Al2Cl2Me4}\]
Los compuestos de alquilzinc son pirofóricos y fácilmente hidrolizados, mientras que los compuestos de alquilcadmio reaccionan más lentamente con el aire. Debido a la leve acidez de Lewis, los compuestos de dialquilzinc y dialquilcadimum forman complejos estables con aminas, especialmente con aminas quelantes.
El Zn-C tiene mayor carácter carbaniónico que el enlace Cd-C.
Por ejemplo, la adición de compuestos de alquilzinc a través del grupo carbonilo de una cetona:
\[\ce{ZnMe2 + (CH3)2C=O -> (CH3)2C-O-ZnCH3}\]
Esta reacción no procede con los compuestos de alquilcadmio o alquilmercurio menos polares, pero los compuestos de organolitio, organomagnesio y organoaluminio pueden promover esta reacción fácilmente ya que todos los cuales contienen metales con menor electronegatividad que el zinc.
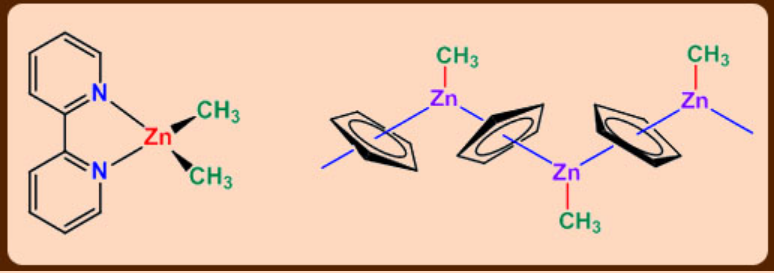
Curiosamente, los compuestos de ciclodipentadienilo son estructuralmente inusuales. El CpZnMe es monomérico en fase gaseosa con un grupo pentahapto Cp.
En estado sólido se asocia en una cadena en zig-zag, siendo cada grupo Cp pentahapto con respecto a dos átomos de Zn.
Problemas:
1. ¿Crees que procede la siguiente reacción? Si es así, ¿por qué y cómo?
\[\ce{ZnCl2 + Al2Me6 -> ZnMe2 + Al2Cl2Me4}\]
Solución
Al 2 Me 6, siendo una molécula deficiente en electrones, intercambia fácilmente dos grupos metilo con zinc por dos iones cloruro. Dado que los iones cloruro tienen suficiente electrón en su capa de valencia actúan como donadores de cuatro electrones a través del modo de coordinación puente. Al 2 Cl 2 Me 4 ya no es una molécula deficiente en electrones.


