9.1: Complejos de Alquenos Metálicos
- Page ID
- 69207
Objetivos de aprendizaje
En esta conferencia aprenderás lo siguiente
- Los complejos de alquenos metálicos.
- Las interacciones de enlace metal-olefina.
- La síntesis y reactividades de los complejos metal-olefina.
- Las reactividades umpolung de olefinas en los complejos de alquenos metálicos.
Aunque el primer complejo de olefinas metálicas se remonta a principios del siglo XIX, su formulación se estableció solo un siglo después en la década de 1950. Mientras reaccionaba\(\ce{K2PtCl4}\) con EtOH en 1827, el químico danés Zeise sintetizó la famosa sal de Zeise\(\ce{K[PtCl3(C2H4)]•H2O}\) que contenía un resto etileno unido a Pt y que, por cierto, representaba el primer complejo metal-olefina (Figura\(\PageIndex{1}\)).
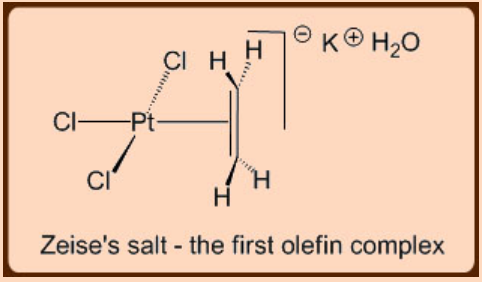
La interacción de unión metal-olefina se explica mejor por el modelo Dewar−Chatt, que tiene en cuenta dos donaciones de electrones mutuamente opuestas que implican la donación de σ−donación de los electrones olefínicos C=C π−−electrones a un orbital de metal d π vacío seguido de una donación de π−back de un relleno metal d π orbital en el orbital desocupado C=C π*. Muy comprensiblemente, para los sistemas d 0, no se observan las formaciones de complejos de metal-olefina. La extensión de la donación p directa C=C al metal y la posterior donación π−back desde el orbital d π relleno al orbital olefínico C=C π* tienen una relación directa en el enlace C=C del resto olefínico unido a metal en forma de provocar un cambio en la hibridación así como en la distancia de unión C−C (Figura\(\PageIndex{2}\)).
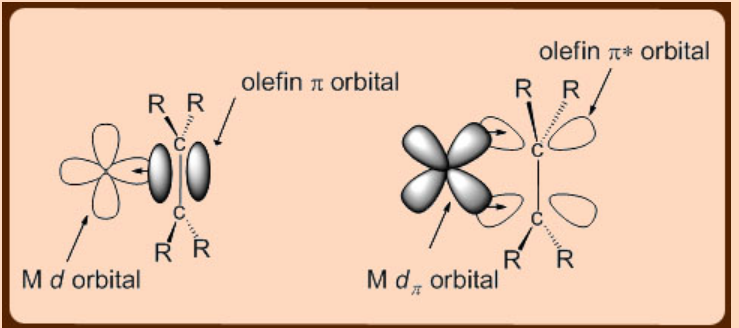
Si el componente de donación de metal a ligando n-back es más pequeño que el ligando a metal σ-donación, entonces se observa el alargamiento del enlace C-C en el resto de olefina unida a metal. Esto sucede principalmente por el hecho de que la donación de alqueno a metal σ−elimina los electrones C=C del enlace C−C del resto olefínico y hacia el centro metálico, disminuyendo así su orden de enlace y aumentando la longitud del enlace C−C. Además, a medida que aumenta la donación de metal a ligando π−back, se mejora la donación de electrones del metal cargado d π orbital en el orbital π* del resto de olefina unido a metal. Esto da como resultado un aumento en la longitud del enlace C-C. El alargamiento del enlace C-C en el complejo de olefina unida a metal puede correlacionarse con la basicidad p del metal. Por ejemplo, para un metal p básico débil, se anticipa que el alargamiento del enlace C-C sea pequeño, mientras que para un metal p básico fuerte, el alargamiento C-C sería significativo.
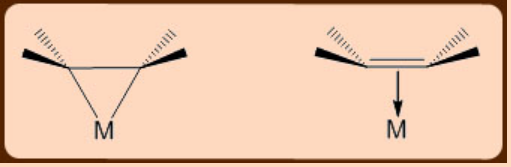
Otra implicación de la donación de ligando-metal π-back está en el cambio observado de hibridación en los átomos de C olefínicos de sp 2 puro, en complejos sin metal a ligando n-back donación, a sp 3, en complejos con metal significativo a ligando n-back donación, se observa. El cambio en la hibridación de los centros sp 2 a sp 3 del carbono olefínico se acompaña de que los sustituyentes están ligeramente doblados lejos del centro metálico en la forma final de metalaciclopropano (Figura\(\PageIndex{3}\)). Este cambio en la hibridación puede detectarse convenientemente mediante espectroscopía de RMN 1H y 13C. Por ejemplo, en el caso de los sistemas de metalaciclopropano, que tienen una fuerte donación de metal a ligando π−back, los protones vinílicos aparecen 5 ppm (en la RMN 1H) y 100 ppm (en la RMN de 13 C) de campo alto con respecto a la posición respectiva de los ligandos libres.
Una interesante caída del enlace de metal a ligando π−back es la unión más apretada de las olefinas deformadas al centro metálico como se observa en el caso del ciclopropeno y el norborneno. La fuerte unión de estos grupos de ciclopropeno y norborneno al centro metálico surge del alivio de la tensión del anillo tras la unión al metal. Por último, en los complejos de metal-olefina que tienen muy poco componente de enlace p, las reactividades químicas de la olefina unida a metal aparecen opuestas a las de una olefina libre. Por ejemplo, una olefina libre se considera rica en electrones en virtud de la presencia de electrones π−en su orbital de valencia más externa y por lo tanto sufre un ataque electrófila. Sin embargo, los complejos de olefinas unidas a metal que tienen predominantemente la donación de σ−electrones olefínicos y la donación insignificante de metal a ligando π−back, la C olefínica se carga positivamente y por lo tanto sufre un ataque nuclofílico. Esta naturaleza de inversión de la reactividad de las olefinas se llama carácter umpolung.
Síntesis
Los complejos de alqueno metálico se sintetizan mediante los siguientes métodos.
i. Sustitución en metales de baja valencia
\[\ce{AgOSO2CF3 + C2H4 -> (C2H4)AgOSO2CF3}\]
ii. Reducción del metal de alta valencia en presencia de un alqueno
\[\ce{(cod)PtCl2 + C2H4 -> [PtCl3(C2H4)]- + Cl-}\]
iii. De alquilos y especies afines
\[\ce{Cp2TaCl3 + n-BuMgX -> {Cp2TaBu3}}\]
\[\ce{{Cp2TaBu3} ->[\Beta -elimination][reductive \: elimination] Cp2TaH(1-Butene) + Butene + Butane}\]
Reacción de alquenos
Los complejos de alquenos metálicos muestran las siguientes reactividades.
i. Reacción de inserción
Estas reacciones son comúnmente mostradas por alquenos a medida que se insertan en enlaces Metal-X que producen alquilos metálicos. La reacción ocurre fácilmente a temperatura ambiente para X = H, mientras que para otros elementos (X = otros átomos), tales inserciones se vuelven raras. Además, los alquenos y alquinos tensos experimentan dicha inserción fácilmente.
\[\ce{PtHCl(PEt3)2 + C2H4 <=> PtElCl(PEt3)2}\]
ii. Reacciones de
Umpolung Las reacciones de Umpolung se observan solo para aquellos complejos metal-alqueno para los que el centro metálico es una base p pobre y como resultado de lo cual la olefina sufre un ataque nuclofílico.
iii. Adición oxidativa
Los alquenos que contienen hidrógenos alílicos experimentan adición oxidativa para dar un complejo de hidruro de alilo.
Problemas
1. Predecir el producto de la reacción.
\[\ce{AuMe(PPh3) + CF2=CF2 -> A -> B}\]
Respuesta: A = {(CF 2 =CF 2) AUMe (PPh 3)} y B = Au (CF 2 -CF 2 Me) (PPh 3)
2. Especificar si el alargamiento/acortamiento de la distancia de enlace C-C en el resto de olefina unida a metal se observa como resultado de la donación de metal a ligando π−back?
Ans: Alargamiento.
3. Dibujar la estructura de la sal de Zeise.
Ans:
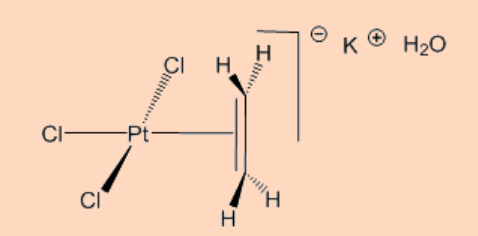
4. El cambio en la hibridación en la C olefínica de sp 2 a sp 3 surge principalmente debido a?
Ans: Donación de π-back de ligando metálico.
Prueba de autoevaluación
1. Predecir el producto de la reacción.
\[\ce{PtCl2- + C2H4 ->}\]
Respuesta: [PtCl 3 (C 2 H 4)] - y Cl -
2. Especificar si el alargamiento/acortamiento de la distancia de enlace C−C en el resto de olefina unida a metal se observa como resultado de la donación de ligando a metal σ−?
Ans: Alargamiento.
3. El intermedio de metalaciclopropano en un complejo de olefina unida a metal se forma principalmente debido a qué tipo de interacción?
Ans: Metal-ligando π−back donativo
4. El estado de oxidación del Pt en la sal de Zeise es?
Respuesta: Pt II
Resumen
Los alquenos son una clase importante de ligandos insaturados que se unen a un metal donando sus electrones C=C π−y también aceptan electrones del metal en su orbital π* de enlace C=C. Estos simbióticos σ−donativos y π−back donativos en complejos de olefinas ligadas a metales tienen un impacto significativo en su estructura y propiedades de reactividad. De manera muy importante, las manifestaciones estructurales que surgen de estas donaciones directas de σ−donación y π−back pueden caracterizarse utilizando métodos espectroscópicos de 1H, 13C RMN e IR.


