9.2: Complejos metálicos de alilo y dieno
- Page ID
- 69193
Objetivos de aprendizaje
En esta conferencia aprenderás lo siguiente
- Los complejos metal-alilo.
- Los complejos de metal−dieno.
- Los complejos metal-ciclobutadieno.
- Las respectivas interacciones metal-ligando.
“El ligando alilo a menudo se conoce como un ligando “" actor "” en lugar de un ligando “" espectador "”.” Se une a los metales de dos maneras es decir, en una forma η 1 (monohapto) y una forma η 3 (trihapto) (Figura\(\PageIndex{1}\)). i). En su forma monohapto (η 1), se comporta como un tipo X aniónico 1e-donador de un ligando análogo al de un resto metilo mientras que (ii) en forma trihapto (η 3), actúa como un tipo LX aniónico 3e-donador de un ligando.
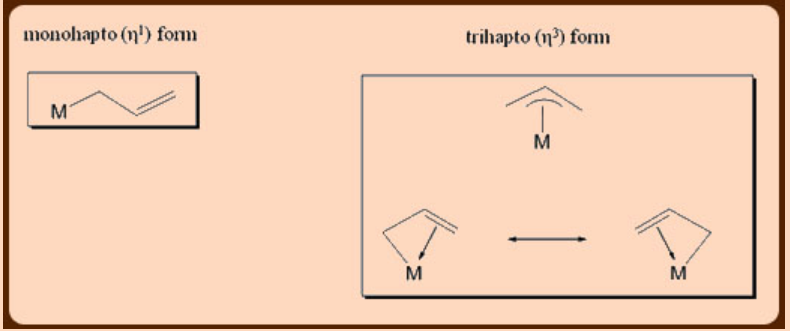
Interacción metal-alilo
De particular interés son los orbitales moleculares, a saber, ψ 1, ψ 2 y ψ 3 del ligando alilo que interactúan con el metal en un complejo de alilo metálico. La energía de estos orbitales moleculares aumenta con el incremento en el número de nodos. De los tres, los orbitales ψ 1 y ψ 2 generalmente se involucran en la donación de ligando a metal σ−donación, con ψ 1 involucrando en un enlace dativo tipo L y ψ 2 participando en un enlace covalente de tipo X con los orbitales de metal d (Figura\(\PageIndex{2}\)).
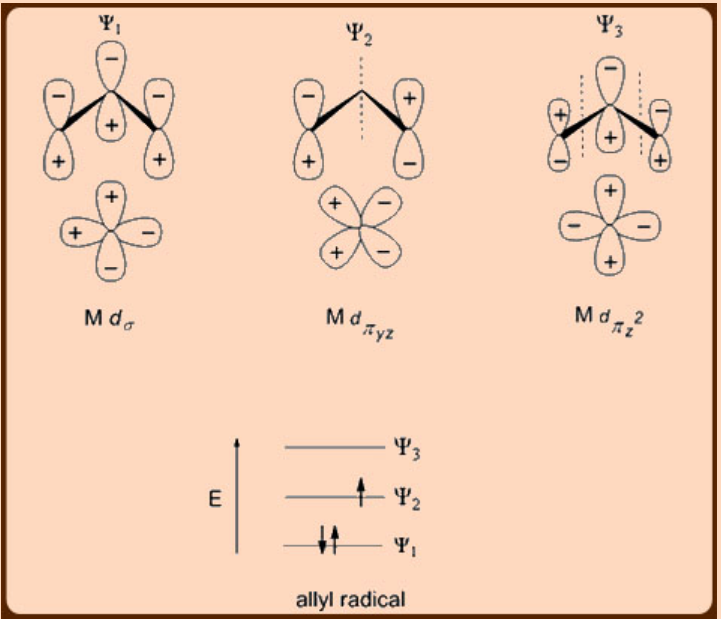
Síntesis de los complejos de alilo metálico
Los complejos de alilo metálico se sintetizan por los siguientes métodos.
i. De un complejo alqueno como se muestra a continuación.
\[\ce{Mo(dpe)2(η2 -propene) <=> Mo(dpe)2( η3-allyl)H}\]
ii. Por un ataque nucleofílico de un compuesto alílico como se muestra a continuación.
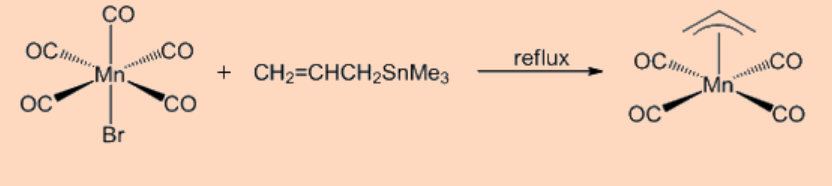
iii. Por un ataque electrófilo de un compuesto alílico como se muestra a continuación.
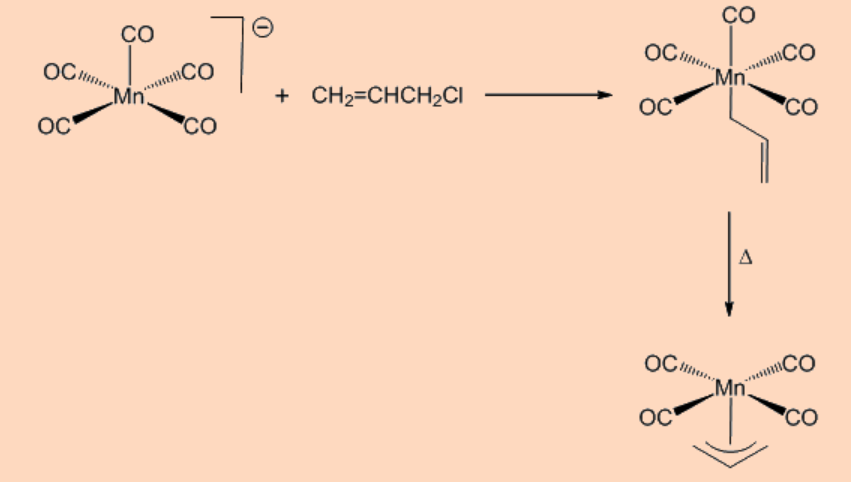
iv. De un complejo diénico como se muestra a continuación.
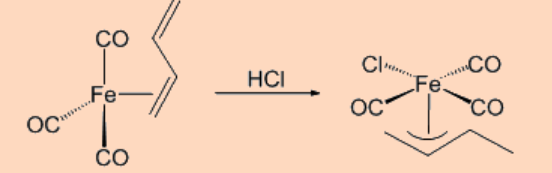
Reacciones de complejos de alilo metálico
Las reactividades de los complejos de alilo metálico hacia diversas especies se ilustran a continuación.
i. Reacción con nucleófilos
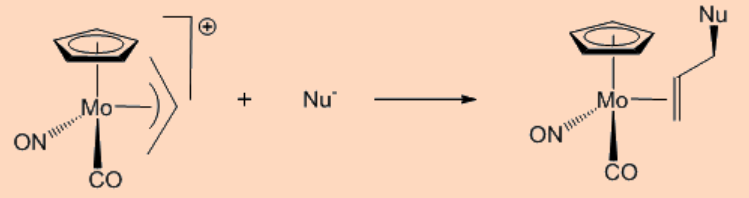
ii. Reacción con electrófilos
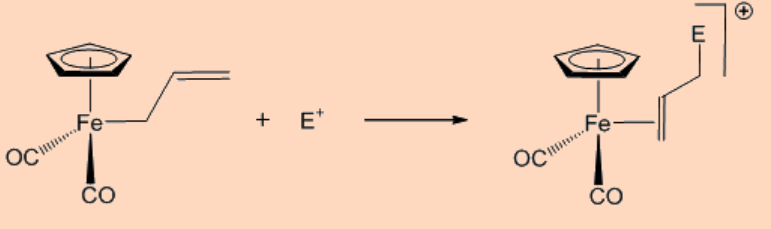
iii. Reacción de inserción
iv. Eliminación reductiva
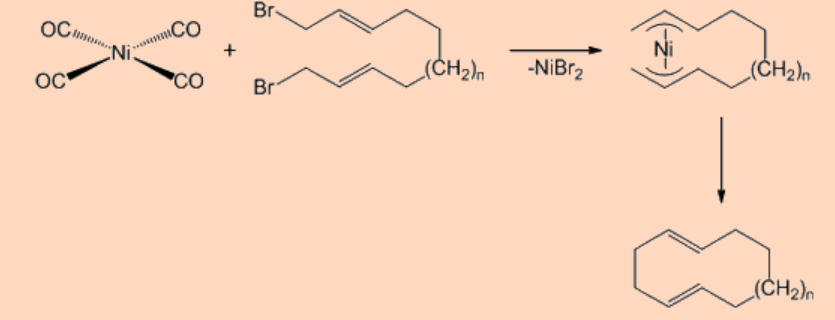
Complejos diénicos
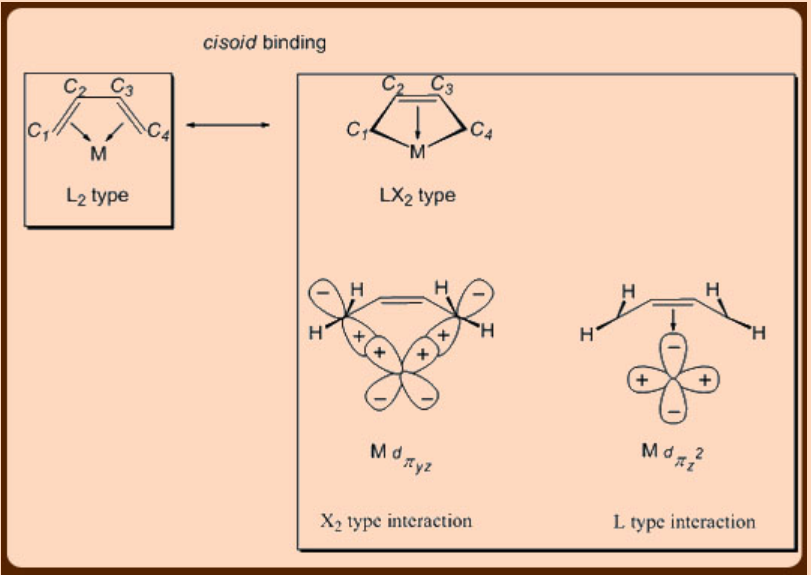
El 1,3-butadieno es un ligando 4e-donador que se une a un metal en una conformación cisoide. El modelo Dewar−Chatt, cuando se aplica a 1,3−butadieno, predice que el ligando puede unirse al metal ya sea como un tipo donante L 2 (π 2), similar al de un alqueno, o como un tipo donante LX 2 (σ 2 π), similar a la de una forma de metalaciclopropano. La unión L 2 de 1,3-butadieno es rara, por ejemplo asin (butadieno) Fe (CO) 3, mientras que la unión de tipo LX 2 es más común, por ejemplo, como en Hf (PMe 3) 2 Cl 2. Una implicación de la unión de tipo LX 2 está en el acortamiento observado de la distancia C2-C 3 (1.40 Å) junto con el alargamiento de las distancias C1-C2 (1.46 Å) y C3-C4 (1.46 Å) (Figura\(\PageIndex{3}\)).
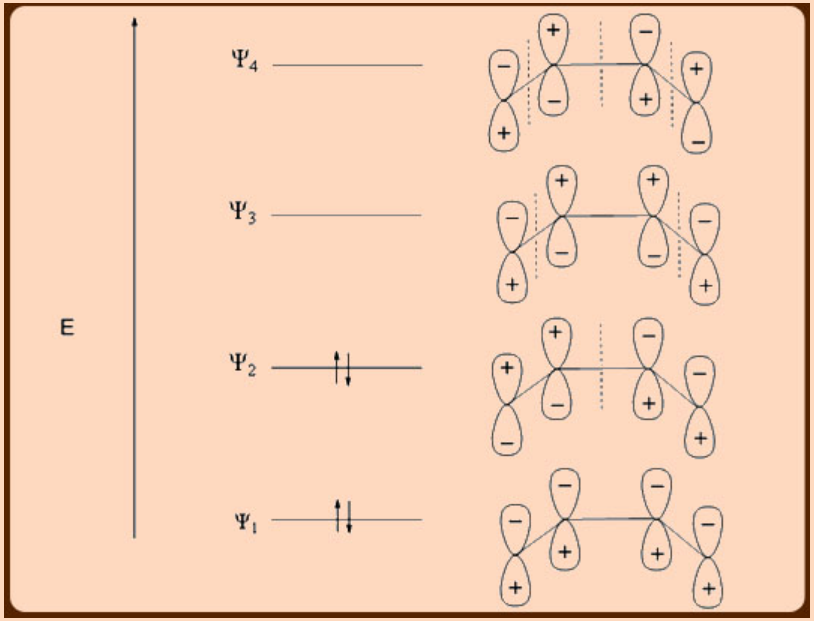
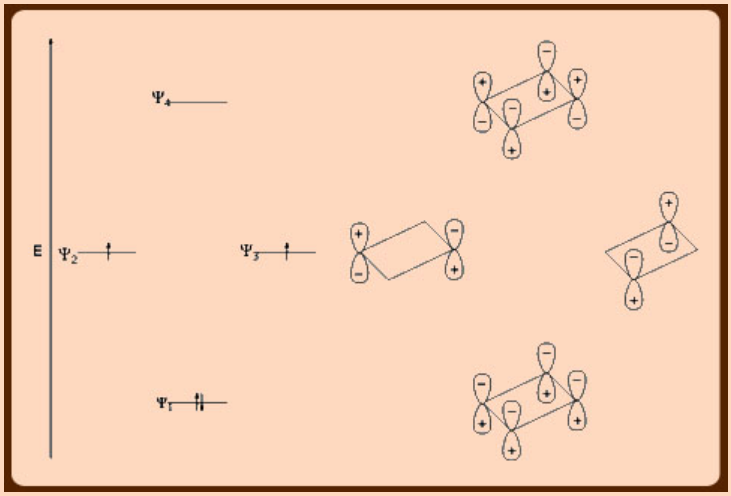
Los orbitales moleculares del ligando 1,3−butadieno comprenden dos orbitales llenos ψ 1 (HOMO−1) y ψ 2 (HOMO) y dos orbitales vacíos ψ 3 (LUMO) y ψ 4 (LUMO+1). En una interacción metal-butadieno, la donación de ligando a metal σ−se produce desde el orbital ψ 2 lleno del ligando 1,3-butadieno, mientras que la donación de metal a ligando n-back ocurre en el orbital ψ 3 vacío del ligando de 1,3-butadieno (Figura\(\PageIndex{4}\)).
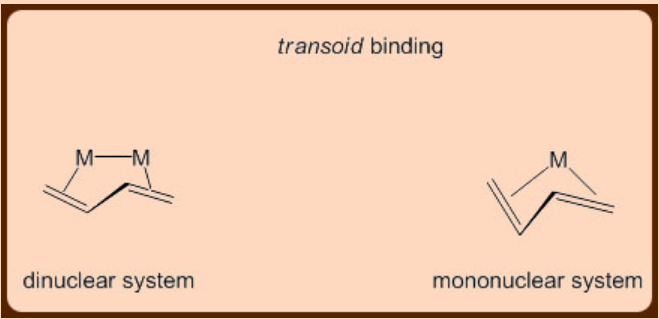
Aunque la unión cisoide se observa a menudo en complejos de metal butadieno, se observan algunos casos de unión transoide en dinucleares, por ejemplo, como en Os 3 (CO) 10 (C 4H 6), y en complejos mononucleares, por ejemplo, como en Cp 2 Zr (C 4 H 6) (Figura\(\PageIndex{5}\)).
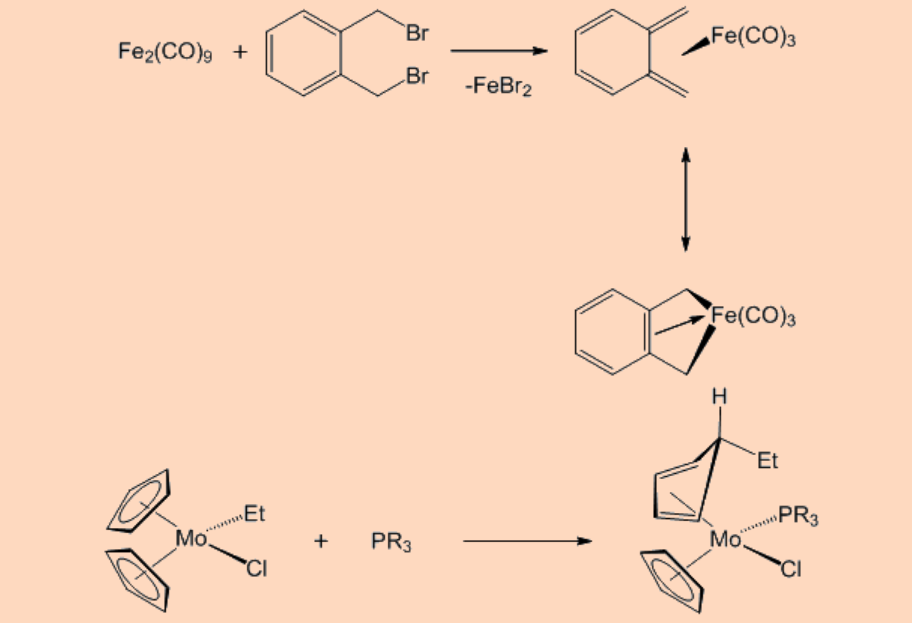
Síntesis de complejo de butadieno metálico
Los complejos de metal butadieno generalmente se preparan por los mismos métodos utilizados para sintetizar complejos de alquenos metálicos. A continuación se muestran dos rutas sintéticas notables.
Complejos metálicos de ciclobutadieno
El ciclobutadieno es un ligando interesante por el hecho de que su forma neutra, al ser anti−aromática (4π −electrones), es inestable como molécula libre (Figura\(\PageIndex{6}\)), pero su forma dianiónica es estable por ser aromática (6π −electrones). En consecuencia, el ligando de ciclobutadieno se estabiliza mediante una donación significativa de metal a ligando π-back a los orbitales de ligando vacantes.
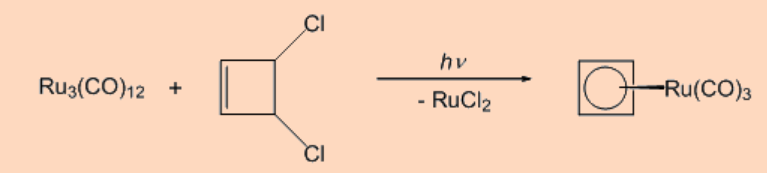
A continuación se muestra una ruta sintética al complejo de ciclobutadieno metálico.
Problemas
1. Las hapticidades mostradas por un resto alilo en la unión a metales son?
Ans: 1 y 3.
2. Identificar qué orbitales moleculares de un resto alilo participan en la interacción σ−con un orbital d adecuado de un metal en un complejo alilo η 3-metal?
Ans: ψ 1 y ψ 2.
3. Predecir el producto de la reacción.
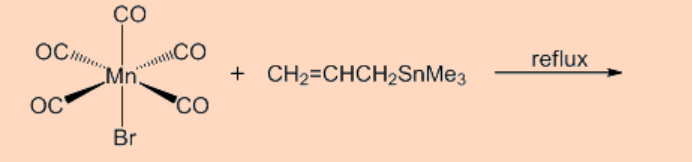
Ans:
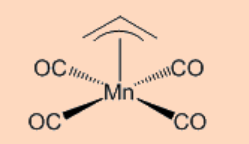
4. Identificar qué orbitales moleculares de un resto butadieno participan en la interacción σ−con un orbital d adecuado de un metal en un complejo de η 4-metal butadieno?
Ans: ψ 2.
Prueba de autoevaluación
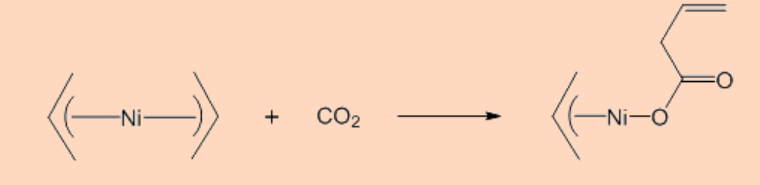
1. Predecir el producto de la reacción.
\[\ce{<(--Ni--)> + CO2 -> }\]
Ans:
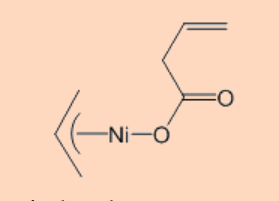
2. Identificar qué orbitales moleculares de un resto butadieno participan en la interacción π−con un orbital d adecuado de un metal en un complejo de alilo η 4-metal?
Ans: ψ 3.
3. Mencionar el tipo de orientaciones que muestran los ligandos de butadieno para la unión al metal.
Ans: Cisoide (común) y transoide (raro).
4. Comentario sobre el número de electrones p presentes en el resto ciclobutadieno de un complejo de ciclobutadieno metálico.
Ans: 6 π−electrones.
Resumen
El alilo, el 1,3−butadieno y el ciclobutadieno juntos constituyen una clase importante de ligandos σ-donador/n-aceptor que ocupan un lugar especial en la química organometálica. Los complejos de estos ligandos con metales son intermedios importantes en muchos ciclos catalíticos y, por lo tanto, la comprensión de su interacción con el metal es de importancia significativa. En este contexto, la síntesis, caracterización y las reactividades de los complejos organometálicos de estos ligandos se describen junto con las respectivas interacciones metal-ligando.


