9.6: Marcos de Coordinación
- Page ID
- 81551
Ligandos puente enlazan metales en complejos de coordinación multicéntricos
Algunos ligandos ambidentados y multidentados tienen la capacidad de unir dos centros metálicos. Por ejemplo, los ligandos ciano pueden puentear dos centros metálicos formando enlaces lineales del tipo
\[\ce{M-CN-M'} \nonumber \]
Vínculos como estos se pueden utilizar para puentear múltiples centros metálicos en un clúster o red sólida, este último de los cuales a veces se denomina marco de coordinación. Cuando el ligando ciano se combina con centros metálicos octaédricos que poseen 90 ángulos de enlace\(^{\circ}\) L-M-L, se obtiene una red de coordinación cúbica. Un ejemplo es el marco de coordinación Azul Prusiano, que posee la celda unitaria representada en la Figura\(\sf{\PageIndex{1A}}\).
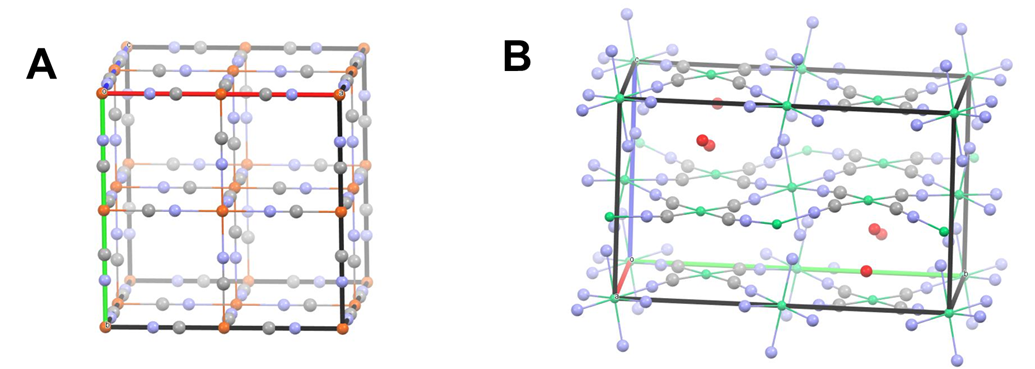
La red cúbica mostrada en la Figura\(\sf{\PageIndex{1A}}\) refleja la estructura 3D del octaedro, en la que los enlaces M-L apuntan a lo largo de los ejes x, y y z. Si se utiliza un centro metálico plano cuadrado, se produce en su lugar una red de coordinación 2D que comprende cuadrados entrelazados. Un ejemplo es el clatrato de Hofmann mostrado en la Figura\(\sf{\PageIndex{1B}}\), que representa un clatrato de Hofmann en el que las unidades planas cuadradas [Ni (CN) 4] 2- están unidas por unidades trans -Ni (NH 3) 2 2+ (que son octaédricas pero tienen un plano cuadrado de sitios de coordinación perpendiculares al eje NH 3 -Ni-NH 3).
Las estructuras de los poliedros de coordinación y los marcos reflejan geometrías de coordinación de ligandos y metales
Como se ilustra en las redes de coordinación de clatratos azul prusiano y Hofmann mostradas en la Figura\(\sf{\PageIndex{1}}\), las estructuras formadas cuando un ligando puente une múltiples centros metálicos depende de la geometría de los centros, el ligando y los enlaces metal-ligando formados. Debido a que la direccionalidad de la unión metal-ligando en muchos tipos de complejos está bien caracterizada y es predecible, es posible diseñar complejos metálicos y enlazadores que puedan servir como bloques de construcción para clústeres y redes. En particular
- complejos metálicos con combinaciones de ligandos lábiles (sustituibles) en topologías particulares. Estos aseguran que el ligando de enlace se dispondrá alrededor del centro metálico en esas direcciones definidas.
- Ligandos que poseen sitios de unión orientados en direcciones definidas para que unan los centros metálicos entre sí en topologías particulares.
En la Figura se dan ejemplos del tipo de centros metálicos que se pueden usar y ejemplos de ligandos de unión\(\sf{\PageIndex{2}}\).
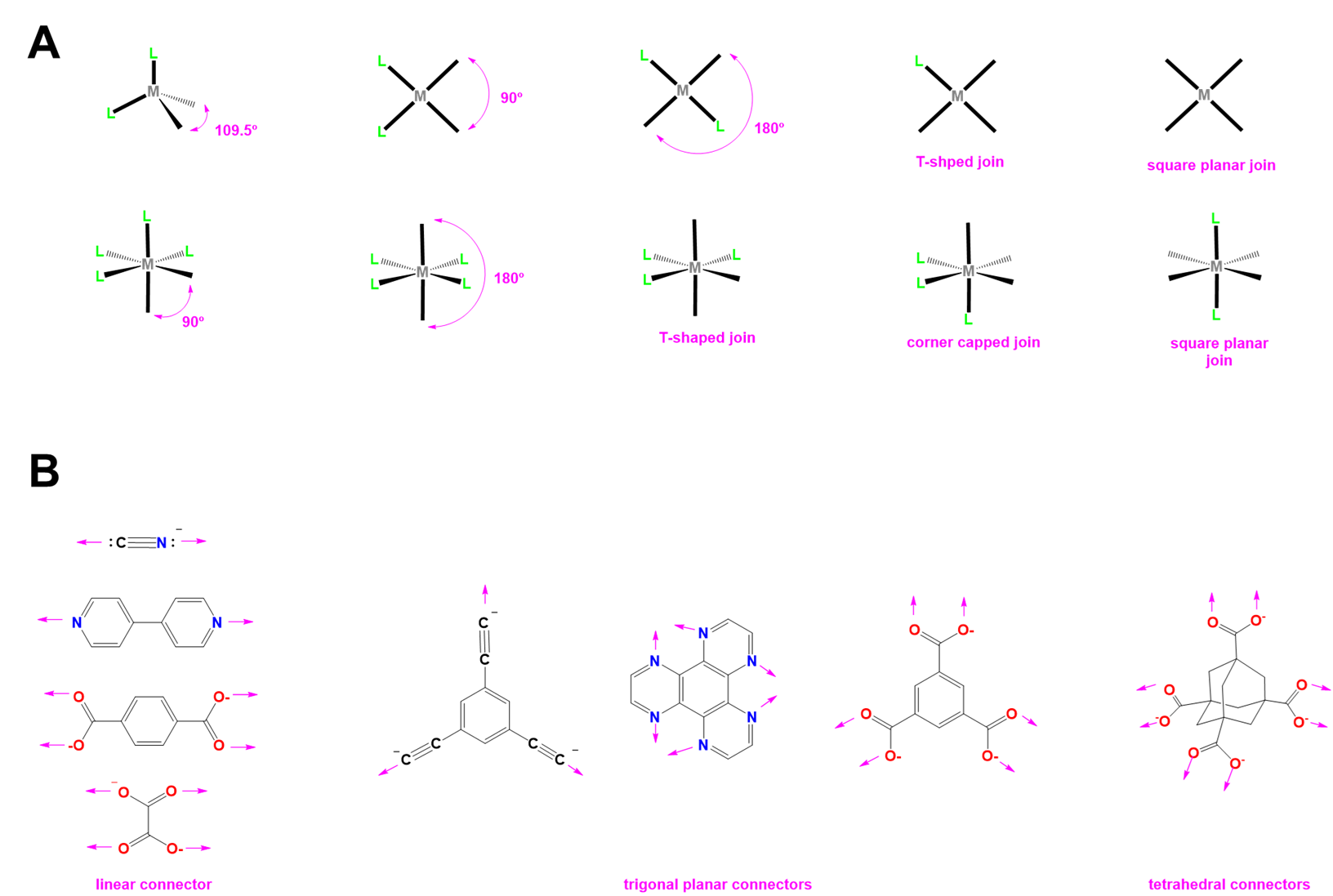
Ejemplos de cómo los bloques de construcción mostrados en la Figura\(\sf{\PageIndex{2}}\) podrían usarse para preparar poliedros moleculares y redes de coordinación se representan esquemáticamente como se muestra en la Figura\(\sf{\PageIndex{3}}\). Entre los ejemplos mostrados en la Figura\(\sf{\PageIndex{3}}\), los representados a la derecha esquematizan las redes de coordinación del clatrato Hofmann (arriba) y Azul Prusia (abajo) de la Figura\(\sf{\PageIndex{1}}\).
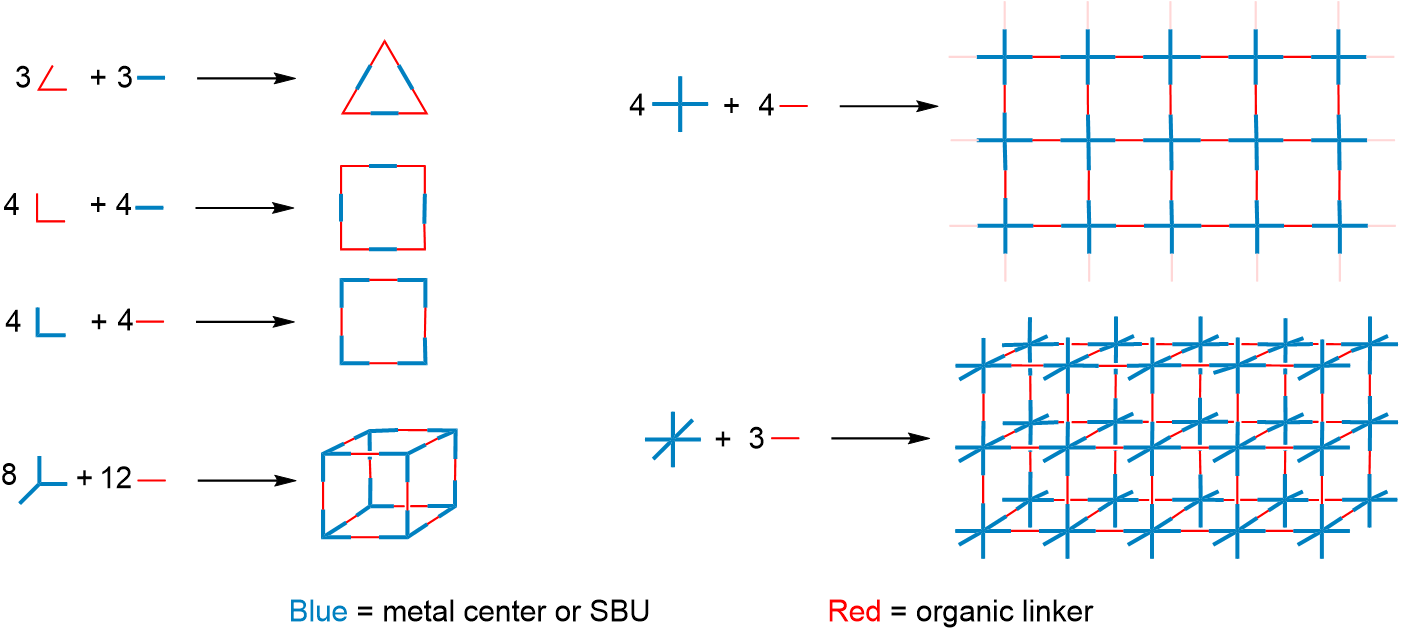
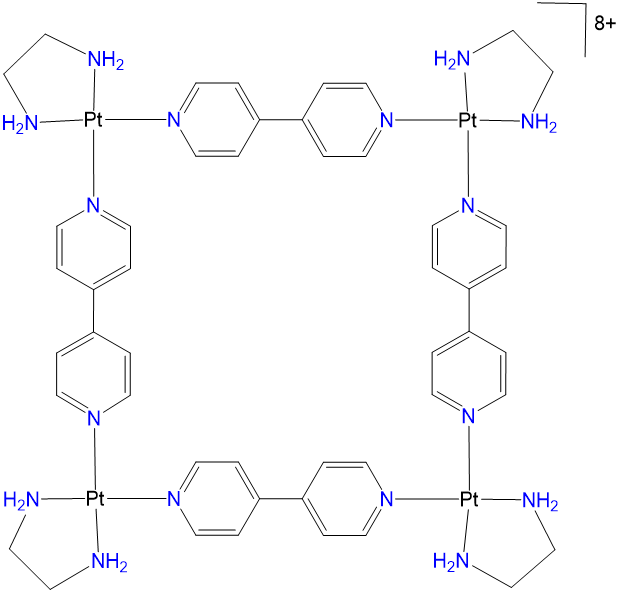
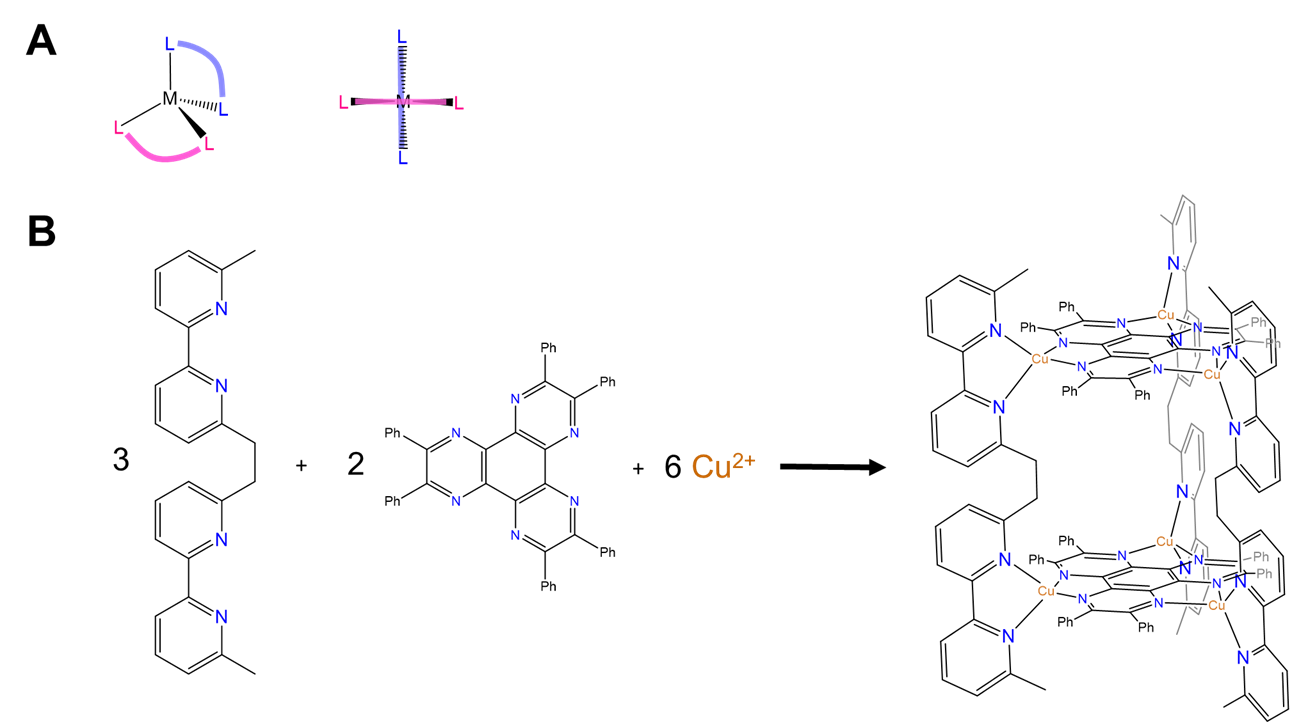
Es posible una variedad más amplia de estructuras que las insinuadas por los bloques de construcción y las estructuras que se muestran en las Figuras\(\sf{\PageIndex{2}}\) y\(\sf{\PageIndex{3}}\). Se pueden obtener más utilizando los principios de estructura molecular descritos en las secciones sobre geometría de coordinación, ligandos e isomería. De hecho, uno de los primeros poliedros de coordinación preparados involucró el reconocimiento de Jean-Marie Lehn de que los ligandos bidentados planos en un bis-quelato tetraédrico están orientados perpendiculares entre sí, como se muestra en las Figuras\(\sf{\PageIndex{5A}}\). Esto le permitió preparar un prisma molecular trigonal combinando una fuente de Cu 2 + con los enlazadores orgánicos trigonales planos y lineales capaces que unen el Cu 2 + de manera bidentada, como se muestra en la Figura\(\sf{\PageIndex{5B}}\).
Los marcos orgánicos metálicos (MOF) son polímeros porosos de coordinación en los que las “unidades de construcción” metálicas están conectadas por “puntales” de ligando orgánico rígido
Una clase de marcos de coordinación que ha recibido mucha atención en los últimos 25 años son los marcos orgánicos metálicos (MOF). Estos consisten en centros metálicos unidos por ligandos orgánicos rígidos para dar una estructura porosa similar a las de las zeolitas a base de aluminosilicato. La estructura de un MOF, llamado MIL-53, se da en la Figura\(\sf{\PageIndex{6A}}\).
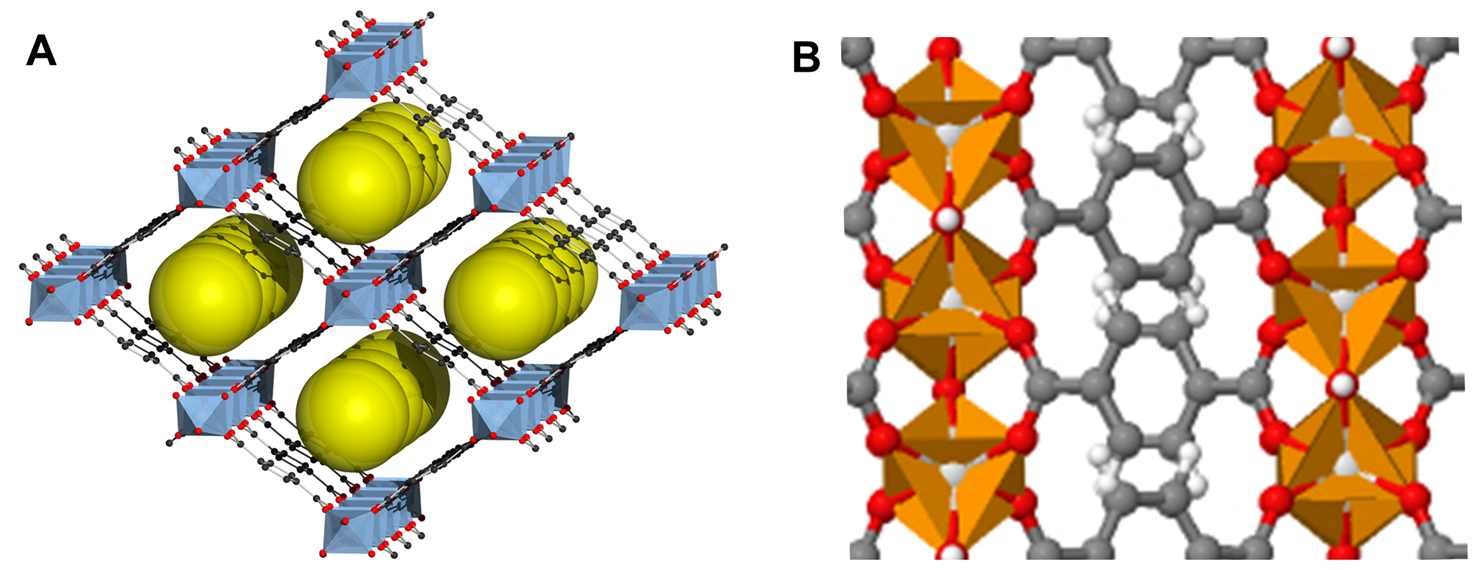
Como se puede observar a partir de la estructura general de MIL-53 representada en la Figura\(\sf{\PageIndex{6A}}\), la estructura posee grandes huecos prismáticos rómbos, representados por las esferas amarillas. Estos huecos pueden, en principio, estar ocupados por sustratos de moléculas pequeñas. Debido al potencial de MOF para unir y almacenar sustratos, existe un interés considerable en desarrollar MOF que sean útiles para almacenar y separar gases particulares.
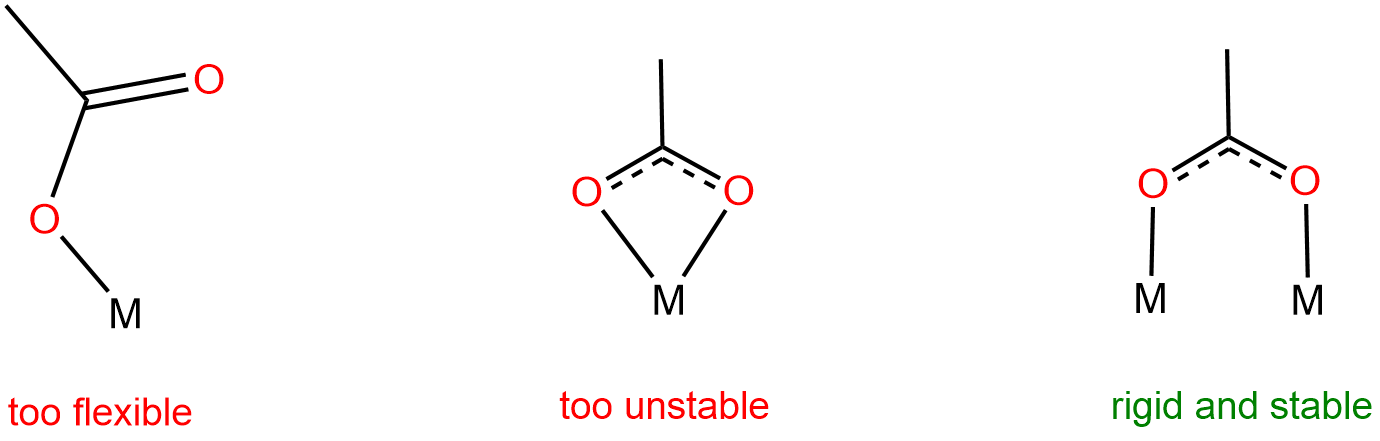
Una mirada más cercana a la estructura de MIL-53 revela que los oxígenos carboxilato en los enlazadores bencenodicarboxilato (BDU) abarcan dos centros metálicos diferentes en lugar de unirse a uno solo. Como se explica en la Figura\(\sf{\PageIndex{7}}\), este modo de unión permite la formación de redes rígidas estables, aunque requiere el uso de bloques de construcción metálicos en los que dos o más centros metálicos se mantienen en estrecha proximidad.
En MIL-53, los centros metálicos que coordinan los ligandos DBU son cadenas de centros metálicos octaédricos puenteados por ligandos\(\mu_2\) hidroxo. Estas cadenas se forman espontáneamente a medida que la red se forma bajo las condiciones de alta temperatura de su síntesis. En otros casos, se utilizan unidades de construcción secundarias metálicas (SBU) que contienen los ligandos de dicarboxilato puente necesarios. Una clase común de SBU metálicos utilizados son los carboxilatos de rueda de paletas que se muestran en la Figura\(\sf{\PageIndex{8A}}\). Estos consisten en dos metales abarcados por un plano cuadrado de cuatro carboxilatos en una disposición de rueda de paletas.
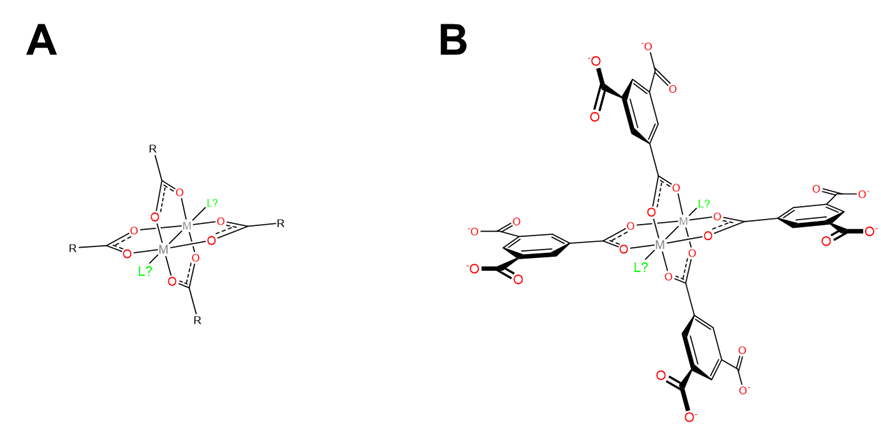
El uso de SBU de metal carboxilato de rueda de paletas y ligandos de carboxilato orgánico puente permite la construcción de marcos de coordinación como el de HKUST-1 que se muestra en la Figura\(\sf{\PageIndex{9}}\). La estructura de estas redes depende de la geometría del ligando de enlace. Por ejemplo, en HKUST-1 los ligandos de puente 1,3,5-bencenetricarboxilato enlazan cada uno tres SBU de rueda de paletas para dar la red cúbica que se muestra en la Figura\(\sf{\PageIndex{9}}\). Otros ligandos de carboxilato orgánicos dan diferentes topologías de red. Además, la capacidad de algunos carboxilatos de rueda de paletas para coordinar ligandos perpendiculares a los carboxilatos, representados por los ligandos marcados con L? en la Figura\(\sf{\PageIndex{8}}\), brinda oportunidades adicionales para usar estas redes para unir sustratos que puedan coordinar esos sitios.
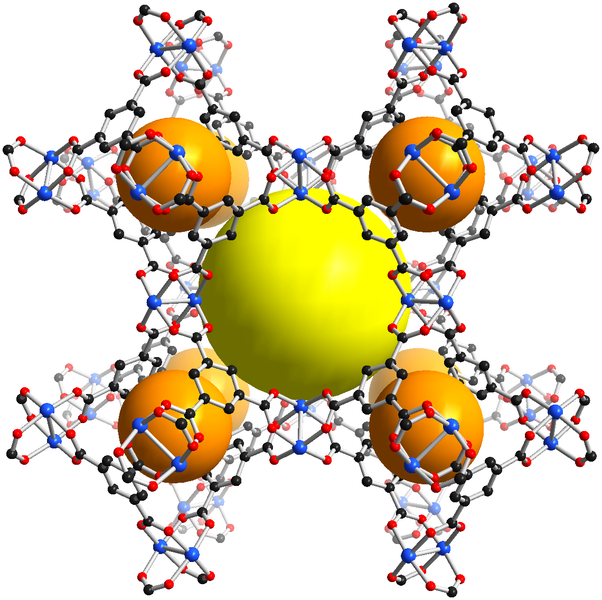
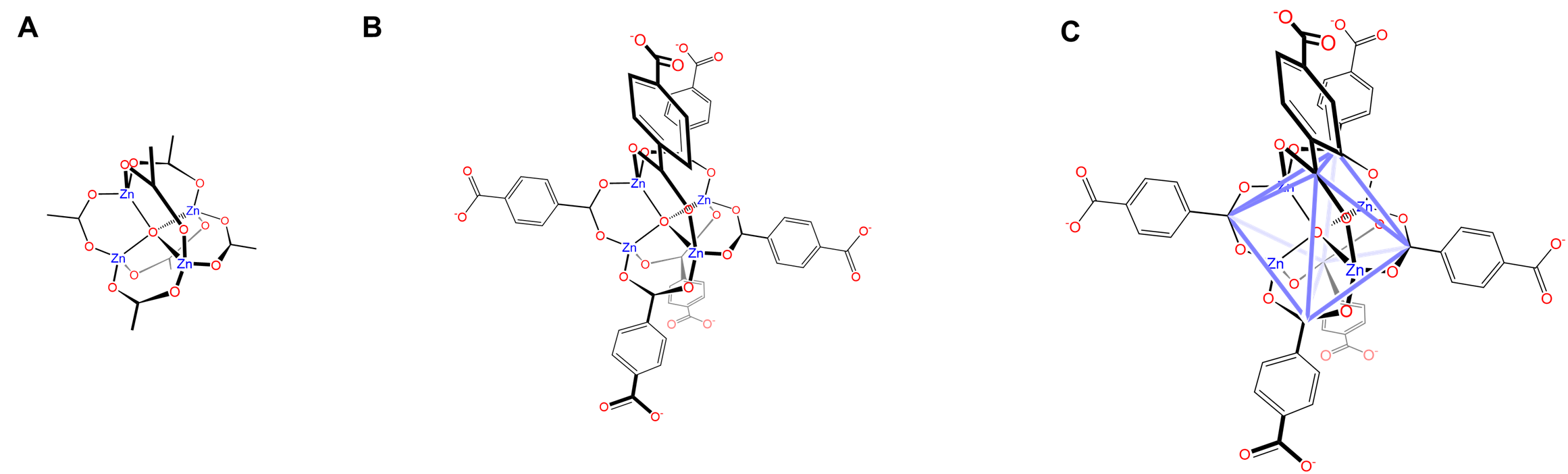
Otro SBU metálico común es la estructura básica de acetato de zinc que se muestra en la Figura\(\sf{\PageIndex{10}}\). Como se muestra en la Figura\(\sf{\PageIndex{10A}}\), la estructura es análoga a la de los acetatos básicos de berilio e implica un tetraedro OZn 4 en el que los Zn 2 + dispuestos tetraédricamente están conectados por ligandos carboxilato que abarcan los seis tetraedros. bordes. Cuando estos ligandos carboxilato son reemplazados por dicarboxilatos rígidos (Figura\(\sf{\PageIndex{10B}}\)), el resultado es que el núcleo de Zn 4 O está rodeado por una esfera de coordinación octaédrica de ligandos carboxilato (Figura\(\sf{\PageIndex{10C}}\)).
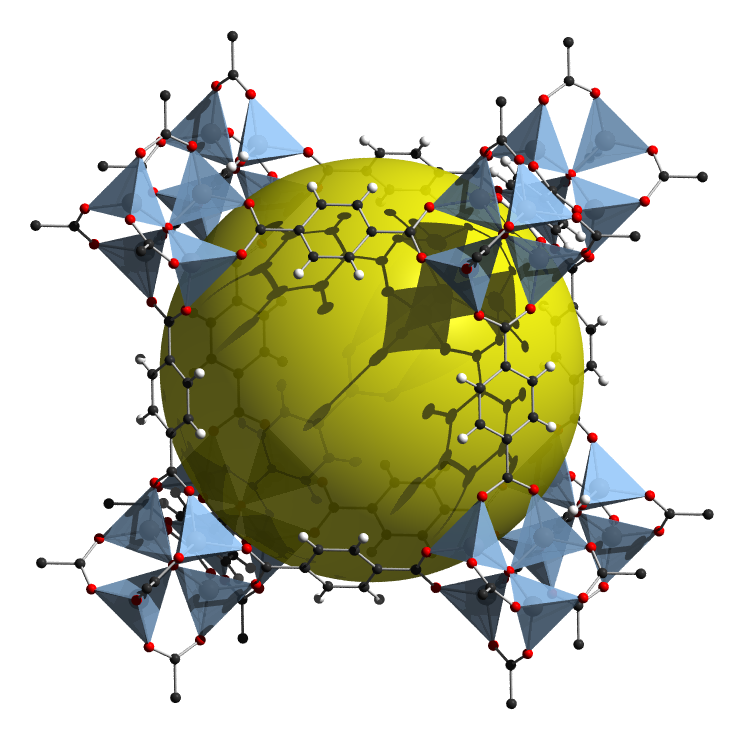
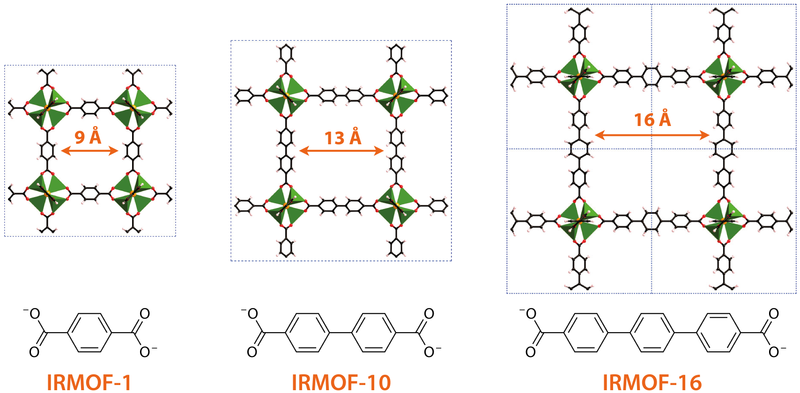
La estructura de MOF-5 también ilustra cómo se puede adaptar el tamaño de los poros en una estructura MOF alargando o acortando el enlazador orgánico. En particular, a partir de la Figura\(\sf{\PageIndex{11}}\) se puede observar que el tamaño de la celda unitaria cúbica del MOF-5 depende de la longitud de la porción orgánica del enlazador carboxilato. En MOF-5 este enlazador consiste en una sola unidad de benceno y da poros de 9 Angstrom, mientras que el uso de dos y tres anillos de benceno aumenta el tamaño de poro a 13 y 16 Angstroms, respectivamente, como se muestra en\(\sf{\PageIndex{12}}\).
Referencias
1. La estructura del azul prusiano se renderiza a partir de lo reportado en Bester, H. J.; Schwarzenbach, D.; Petter, W.; Ludi, A., The crystal structure of Prussian Blue: Fe 4 [Fe (CN) 6] 3 .xH 2 O. Inorganic Chemistry 1977, 16 (11), 2704-2710; a simplificar la representación del marco de coordinación, se eliminaron las moléculas de agua. La estructura del clatrato tipo Hofmann se obtiene a partir de lo reportado en Rayner, J. H.; Powell, H. M., 688. Estructura cristalina de un amoniato de cianuro de níquel hidratado. Revista de la Sociedad Química (reanudada) 1958, 3412-3418.
2. (a) Fujita, M.; Ogura, K., Ensamblaje dirigido por metales de transición de arquitecturas orgánicas bien definidas que poseen grandes vacíos: De macrociclos a [2] catenanos. Coordinación Química Revisiones 1996, 148, 249-264. (b) Leininger, S.; Olenyuk, B.; Stang, P. J., Autoensamblaje de Nanoestructuras Cíclicas Discretas Mediadas por Metales de Transición. Revisiones Químicas 2000, 100 (3), 853-908.
3. Machado, V. G.; Baxter, P. N. W.; Lehn, J.-M., Autoensamblaje en sistemas inorgánicos autoorganizados: una visión de arquitecturas metalosupramoleculares programadas. Revista de la Sociedad Química Brasileña 2001, 12, 431-462.
4. Yaghi, O. M.; O'Keeffe, M.; Ockwig, N. W.; Chae, H. K.; Eddaoudi, M.; Kim, J., Síntesis reticular y diseño de nuevos materiales. Naturaleza 2003, 423 (6941), 705-714.

