10.1: Radiación nuclear
- Page ID
- 77418
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Resultados de aprendizaje
- Definir la radiactividad.
- Describir un radioisótopo.
- Explicar cómo la radiactividad implica un cambio en el núcleo de un radioisótopo.
- Explicar las características de las formas de radiación.
- Describir y escribir ecuaciones para los tipos primarios de desintegración radiactiva.
Marie Curie (1867 - 1934) fue una científica polaca que fue pionera en la investigación sobre la radiación nuclear (Figura\(\PageIndex{1}\)). Fue galardonada con el Premio Nobel de Física en 1903 junto a su esposo Pierre y Antoine Henri Becquerel por su trabajo sobre radiactividad. Fue galardonada con un segundo premio Nobel en 1911, esta vez en química, por su continua investigación sobre elementos radiactivos. En esta lección, aprenderás sobre la radiactividad, las razones por las que ciertos elementos e isótopos son radiactivos, y los tipos más comunes de procesos de desintegración radiactiva.

Radiactividad
La radiactividad fue descubierta bastante por accidente. En 1896, Henri Becquerel estaba estudiando el efecto de ciertas sales de uranio en placas de película fotográfica. Creía que las sales tenían un efecto en la película sólo cuando habían sido expuestas a la luz solar. Accidentalmente encontró que las sales de uranio que no habían sido expuestas a la luz solar aún tenían un efecto en las placas fotográficas. Los Curies, asociados de Becquerel en su momento, mostraron que el uranio estaba emitiendo un tipo de rayo que interactuaba con la película. Marie Curie llamó a esto radiactividad. La radiactividad es la descomposición espontánea del núcleo de un átomo por la emisión de partículas y/o radiación. La radiación es la emisión de energía a través del espacio en forma de partículas y/o ondas.
Las reacciones nucleares son muy diferentes de las reacciones químicas. En las reacciones químicas, los átomos se vuelven más estables al participar en una transferencia de electrones o al compartir electrones con otros átomos. En las reacciones nucleares, es el núcleo del átomo el que gana estabilidad al sufrir algún cambio de algún tipo. Algunos elementos no tienen isótopos estables, lo que significa que cualquier átomo de ese elemento es radiactivo. Para algunos otros elementos, solo ciertos isótopos son radiactivos. Un radioisótopo es un isótopo de un elemento que es inestable y sufre desintegración radiactiva. Las energías que se liberan en las reacciones nucleares son muchos órdenes de magnitud mayores que las energías involucradas en las reacciones químicas. A diferencia de las reacciones químicas, las reacciones nucleares no se ven notablemente afectadas por los cambios en las condiciones ambientales, como la temperatura o la presión.
El descubrimiento de la radiactividad y sus efectos sobre los núcleos de los elementos desmintieron la suposición de Dalton de que los átomos son indivisibles. Un nucleido es un término para un átomo con un número específico de protones y neutrones en su núcleo. Como veremos, cuando los nucleidos de un tipo emiten radiación, se transforman en nucleidos diferentes. La desintegración radiactiva es espontánea y no requiere una entrada de energía para ocurrir. La estabilidad de un nucleido particular depende de la composición de su núcleo, incluyendo el número de protones, el número de neutrones y la relación protón-neutrón.
La banda de estabilidad
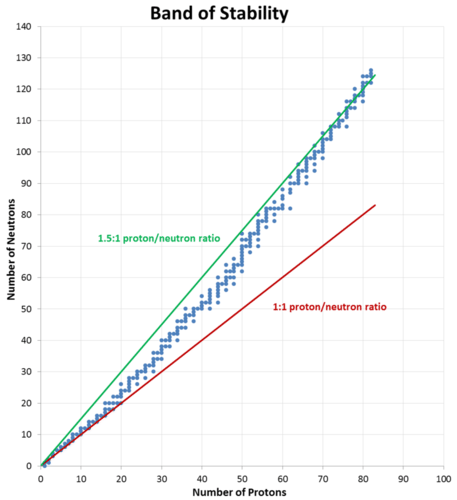
El carbono-12, con seis protones y seis neutrones, es un núcleo estable, lo que significa que no emite radiactividad espontáneamente. El carbono-14, con seis protones y ocho neutrones, es inestable y naturalmente radiactivo. Entre los átomos con números atómicos más bajos, la proporción ideal de neutrones a protones es aproximadamente 1:1. A medida que aumenta el número atómico, la relación estable neutrón-protón aumenta gradualmente a aproximadamente 1. 5:1 para los elementos más pesados conocidos. Por ejemplo, el plomo-206 es un núcleo estable que contiene 124 neutrones y 82 protones, una relación de 1.51 a 1.
Esta observación se muestra en la siguiente figura. La banda de estabilidad es el rango de núcleos estables en una gráfica que traza el número de neutrones en un nucleido frente al número de protones. Los nucleidos estables conocidos se muestran con puntos azules individuales, mientras que las relaciones 1:1 y 1. 5:1 se muestran con una línea roja continua y una línea verde, respectivamente.
Cabe señalar que el hecho de que un núcleo sea “inestable” (capaz de sufrir desintegración radiactiva espontánea) no significa que se descomponga rápidamente. Por ejemplo, el uranio-238 es inestable porque se descompone espontáneamente con el tiempo, pero si se permite que una muestra de uranio-238 se asiente durante 1000 años, solo\(0.0000155\%\) de la muestra habrá decaído. Sin embargo, otros núcleos inestables, como el berkelio-243, desaparecerá casi por completo (>\(99.9999\%\) decaído) en menos de un día.
Desintegración radiactiva
Los núcleos inestables emiten espontáneamente radiación en forma de partículas y energía. Esto generalmente cambia el número de protones y/o neutrones en el núcleo, resultando en un nucleido más estable. Una reacción nuclear es una reacción que afecta el núcleo de un átomo. Un tipo de reacción nuclear es la desintegración radiactiva, una reacción en la que un núcleo se desintegra espontáneamente en un núcleo ligeramente más ligero, acompañado de la emisión de partículas, energía, o ambos. A continuación se muestra un ejemplo, en el que el núcleo de un átomo de polonio se desintegra radioactivamente en un núcleo de plomo.
\[\ce{^{210}_{84}Po} \rightarrow \ce{^{206}_{82}Pb} + \ce{^4_2He}\]
Obsérvese que en una ecuación nuclear equilibrada, la suma de los números atómicos (subíndices) y la suma de los números de masa (superíndices) deben ser iguales en ambos lados de la ecuación. Recordemos el sistema de notación para isótopos, que muestra tanto el número atómico como el número másico junto con el símbolo químico.
Debido a que el número de protones cambia como consecuencia de esta reacción nuclear, la identidad del elemento cambia. La transmutación es un cambio en la identidad de un núcleo como consecuencia de un cambio en el número de protones. Existen varios tipos diferentes de desintegración radiactiva natural, y examinaremos cada uno por separado.
Decaimiento Alfa
Una partícula alfa\(\left( \alpha \right)\) es un núcleo de helio con dos protones y dos neutrones. Las partículas alfa se emiten durante algunos tipos de desintegración radiactiva. La carga neta de una partícula alfa es\(2+\), y su masa es aproximadamente\(4 \: \text{amu}\). El símbolo de una partícula alfa en una ecuación nuclear suele ser\(\ce{^4_2He}\), aunque a veces\(\alpha\) se usa. La desintegración alfa generalmente ocurre para núcleos muy pesados en los que los núcleos son inestables debido a la gran cantidad de nucleones. Para los núcleos que sufren desintegración alfa, su estabilidad se ve incrementada por la resta de dos protones y dos neutrones. Por ejemplo, el uranio-238 se desintegra en torio-234 por la emisión de una partícula alfa (ver figura a continuación).
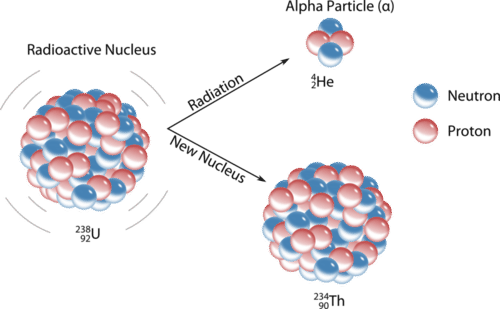
Decaimiento Beta
Los núcleos por encima de la banda de estabilidad son inestables debido a que su relación de neutrones a protones es demasiado alta. Para disminuir esa relación, un neutrón en el núcleo es capaz de convertirse en un protón y un electrón. El electrón es inmediatamente expulsado a alta velocidad del núcleo. Una partícula beta\(\left( \beta \right)\) es un electrón de alta velocidad emitido desde el núcleo de un átomo durante algunos tipos de desintegración radiactiva (ver figura a continuación). El símbolo para una partícula beta en una ecuación es\(\beta\) o\(\ce{^0_{-1}e}\). El carbono-14 sufre desintegración beta, transmutando en un núcleo de nitrógeno-14.
\[\ce{^{14}_6C} \rightarrow \ce{^{14}_7N} + \ce{^0_{-1}e}\]
Tenga en cuenta que la desintegración beta aumenta el número atómico en uno, pero el número de masa sigue siendo el mismo.

Emisión de positrones
Los núcleos por debajo de la banda de estabilidad son inestables debido a que su relación de neutrones a protones es demasiado baja. Una forma de aumentar esa proporción es que un protón en el núcleo se convierta en un neutrón y otra partícula llamada positrón. Un positrón es una partícula con la misma masa que un electrón, pero con una carga positiva. Al igual que la partícula beta, un positrón es expulsado inmediatamente del núcleo tras su formación. El símbolo para un positrón en una ecuación es\(\ce{^0_{+1}e}\). Por ejemplo, el potasio-38 emite un positrón, convirtiéndose en argón-38.
\[\ce{^{38}_{19}K} \rightarrow \ce{^{38}_{18}Ar} + \ce{^0_1e}\]
La emisión de positrones disminuye el número atómico en uno, pero el número de masa sigue siendo el mismo.
Captura de electrones
Una forma alternativa para que un nucleido aumente su relación de neutrones a protones es mediante un fenómeno llamado captura de electrones. En la captura de electrones, un electrón de un orbital interno es capturado por el núcleo del átomo y combinado con un protón para formar un neutrón. Por ejemplo, la plata-106 se somete a captura de electrones para convertirse en paladio-106.
\[\ce{^{106}_{47}Ag} + \ce{^0_{-1}e} \rightarrow \ce{^{106}_{46}Pd}\]
Tenga en cuenta que el resultado general de la captura de electrones es idéntico a la emisión de positrones. El número atómico disminuye en uno mientras que el número de masa sigue siendo el mismo.
Emisión de rayos gamma
Los rayos gamma\(\left( \gamma \right)\) son ondas electromagnéticas de muy alta energía emitidas desde un núcleo. Los rayos gamma son emitidos por un núcleo cuando las partículas nucleares experimentan transiciones entre los niveles de energía nuclear. Esto es análogo a la radiación electromagnética emitida cuando los electrones excitados caen de niveles de energía más altos a menores; la única diferencia es que las transiciones nucleares liberan radiación mucho más energética. La emisión de rayos gamma suele acompañar la descomposición de un nucleido por otros medios.
\[\ce{^{230}_{90}Th} \rightarrow \ce{^{226}_{88}Ra} + \ce{^4_2He} + \gamma\]
La emisión de radiación gamma no tiene ningún efecto sobre el número atómico o número másico de los productos, pero reduce su energía.
Resumen de Nuclear Radiation
La siguiente tabla resume los principales tipos de radiación nuclear, incluyendo carga, masa, símbolo y poder penetrante. El poder penetrante se refiere a la capacidad relativa de la radiación para pasar a través de materiales comunes. La radiación con alto poder de penetración es potencialmente más peligrosa porque puede pasar a través de la piel y causar daño celular.
| Tipo | Símbolo | Número de masa | Cargar | Poder de Penetración | Blindaje |
|---|---|---|---|---|---|
| Partícula alfa | \(\ce{^4_2He}\)o\( \alpha \) | 4 | \(2+\) | Bajo | Papel, piel |
| Partícula beta | \(\ce{^0_{-1}e}\)o\( \beta \) | 0 | \(1-\) | Moderado | Tela pesada, plástico |
| Positrón | \(\ce{^0_1e}\)o\( \beta^+ \) | 0 | \(1+\) | Moderado | Tela pesada, plástico |
| Rayos gamma | \(\gamma\)o\(^0_0\gamma\) | 0 | 0 | Alto | Plomo, hormigón |
| Neutrón | \(\ce{^1_0n}\) | 1 | 0 | Alto | Agua, plomo |

Recursos Suplementarios
- Revisión de estructura atómica: www.Sciencegeek.net/Chemistry... t1Numbers2.htm
- Equilibrio de ecuaciones nucleares: www.Sciencegeek.net/Chemistry... rEquations.htm
- Desintegración nuclear: www.Sciencegeek.net/Chemistry... cleardecay.htm
Colaboradores y Atribuciones
CK-12 Foundation by Sharon Bewick, Richard Parsons, Therese Forsythe, Shonna Robinson, and Jean Dupon.
Allison Soult, Ph.D. (Department of Chemistry, University of Kentucky)


