6.13: Elementos de transición
- Page ID
- 70541
¿Cuáles son las similitudes y diferencias entre estos dos autos?
Desde el exterior, los dos autos de abajo se ven iguales (excepto por el llamativo trabajo de pintura en el modelo de carreras). Son el mismo modelo del auto, pero uno es una edición stock para la conducción regular, mientras que el otro está construido para carreras de alta velocidad. Realmente no podemos decir mucho desde la vista externa. Para ver las diferencias, necesitamos ir bajo el capó, desarmar los motores y mirar los sistemas de frenado y suspensión para ver en qué se diferencian los dos autos.
Muchas configuraciones de electrones de elementos son simples y directas. Podemos mirar la capa exterior y entender fácilmente cómo reaccionará ese conjunto de elementos en términos de ganancia o pérdida de electrones. Sin embargo, hay conjuntos de elementos que son más complejos en su comportamiento. Uno de esos grupos son los elementos de transición.
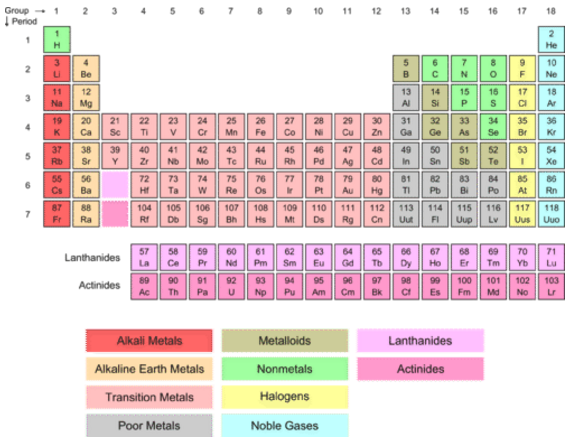
Los elementos de transición
Los elementos de transición son los elementos que se encuentran en los Grupos 3-12 (antiguos grupos IIA-IIB) en la tabla periódica (bloque color salmón en el centro de la tabla). El término se refiere al hecho de que el\(d\) subnivel, que se encuentra en proceso de ser llenado, se encuentra en un nivel de energía principal menor que el \(s\)subnivel llenado antes de él. Por ejemplo, la configuración electrónica del escandio, el primer elemento de transición, es\(\left[ \ce{Ar} \right] \: 3d^1 \: 4s^2\). Recuerde que la configuración se invierte desde la orden de llenado, los\(4s\) rellenos antes de que\(3d\) comience. Debido a que todos son metales, los elementos de transición a menudo se denominan metales de transición. Como grupo, presentan propiedades metálicas típicas y son menos reactivos que los metales de los Grupos 1 y 2. Algunos de los más familiares son tan poco reactivos que se pueden encontrar en la naturaleza en su estado libre o no combinado. Estos incluyen platino, oro y plata. Debido a este orden de llenado único, los elementos de transición a menudo se denominan elementos de "\(d\)-bloque”.

Los compuestos de muchos elementos de transición son distintivos por ser amplia y vívidamente coloreados. A medida que la luz visible pasa a través de un compuesto de metal de transición disuelto en agua, los\(d\) orbitales absorben luz de diversas energías. La luz visible de un determinado nivel de energía que no es absorbido produce una solución claramente coloreada.

Resumen
- Los elementos de transición se encuentran en los grupos IIA-IIB (nuevos grupos 3-12).
- Estos elementos se caracterizan por tener\(d\) subniveles sin llenar.
- En general, el siguiente\(s\) subnivel superior ya está lleno o le falta un electrón.
- Muchos compuestos de elementos de transición son de colores brillantes debido a las transiciones de\(d\) electrones de nivel interno.
Revisar
- Enumere cinco elementos de transición diferentes, dando su nombre, símbolo químico y número atómico.
- ¿Qué tienen de único los elementos de transición en términos de configuraciones de electrones?
- ¿Por qué estos elementos a menudo se denominan elementos “\(d\)-block”?
- ¿Por qué muchos compuestos de elementos de transición tienen colores brillantes?


